

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni2+ | 6.7 | 9.5 |
分析 (1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率,提高镍的浸出率;
(2)根据镍浸出率随时间变化图可知,70℃时,镍浸出率很大,从时间看,120min镍浸出率已经很高,再延长时间对浸出率提高幅度很小;
(3)溶液x中除Ni2+外,还含有Fe2+和Al3+,需要用NaOH溶液调节pH,使铁、铝元素转化为不溶物,同时要Ni2+防止沉淀;
(4)①“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4的水水溶液、便于烘干;
②烘干温度不超过110℃,如果温度过高,草酸镍晶体会失去结晶水.
解答 解:(1)把废镍催化剂粉碎,增大了反应的接触面积,加快反应速率,提高镍的浸出率,故答案为:增大接触面积,加快反应速率,提高镍的浸出率;
(2)根据镍浸出率随时间变化图可知,70℃时,镍浸出率很大,从时间看,120min时镍浸出率已经很高,再延长时间对镍浸出率没有实质性提高,选择70℃和120min为宜,故答案为:c;
(3)溶液x中除Ni2+外,还含有Fe2+和Al3+,需要用NaOH溶液调节pH,使铁、铝元素转化为不溶物,同时要Ni2+防止沉淀,根据图表可知Al3+完全沉淀时溶液的pH为5.0,Fe2+完全沉淀的pH为8.8,Fe3+完全沉淀的pH为3.2,Ni2+开始沉淀的pH为6.7,因此如控制pH完全沉淀Fe2+时溶液里的Ni2+也几乎沉淀完全,显然不行,可通过氧化Fe2+为Fe3+,通过调节pH使Fe3+完全沉淀,综合考虑调节pH为5.0≤pH<6.7即可使铝、铁元素完全沉淀,而Ni2+没有沉淀,故答案为:5.0≤pH<6.7;
(4)①乙醇易挥发且易与水混溶,“沉镍”工序生成了(NH4)2SO4,用乙醇洗涤,能洗去(NH4)2SO4水溶液、更容易烘干,同时也避免用水洗会溶解部分产品,降低产量,故答案为:洗去(NH4)2SO4杂质、便于烘干,减少产品损失;
②草酸镍晶体稳定性较差受热能分解,烘干温度不超过110℃,如果温度过高,草酸镍晶体会分解或失去结晶水,故答案为:防止温度过高,草酸镍晶体分解或失去结晶水.
点评 本题考查了物质分离的实验设计和方法应用,主要是利用溶液不同pH条件下离子沉淀的情况不同,控制溶液PH除去杂质离子,得到较纯净的硫酸镍溶液来制备硫酸镍晶体,同时考查了除杂原则不能引入新的杂质,题目难度大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 化学是一门“中心的、实用的、创造性的”科学,在能源、资源的合理开发和安全应用方面有重要的作用 | |
| B. | 胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有 | |
| C. | 借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有哪些非金属元素 | |
| D. | 提出原子结构模型的科学家按时间先后依次是:道尔顿、卢瑟福、汤姆生、玻尔 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
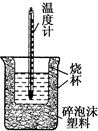 50mL 0.5mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.5mol•L-1盐酸与50mL 0.55mol•L-1 NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:| 温度 实验次数 | 起始温度T1/℃ | 终止温度T2/℃ | 温度差平均值(T2-T1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 30.1 | ||
| 2 | 27.0 | 27.4 | 33.3 | ||
| 3 | 25.9 | 25.9 | 29.8 | ||
| 4 | 26.4 | 26.2 | 30.4 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3 水解:Al3++3H2O═Al(OH)3 +3H+ | |
| B. | NaHCO3 电离:NaHCO3 ?Na++HCO3- | |
| C. | 固体Ca(OH)2 与NH4Cl共热:NH4++OH-═NH3+H2O | |
| D. | 过量的CO2 气体通入饱和石灰水中:CO2 +OH-═HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过量氯气通入溴化亚铁溶液中2Fe2++2Br-+2Cl2═Fe3++Br2+4Cl- | |
| B. | 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至中性2H++SO42-+2OH-+Ba2+=BaSO4↓+2H2O | |
| C. | 碳酸氢钙和过量的氢氧化钠溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| D. | 用FeCl3溶液腐蚀印刷电路板:Cu+Fe3+=Fe2++Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 浓烧碱溶液中加入铝片:A1+2OH-═A1O2-+H2↑ | |
| C. | NO2与水的反应:3NO2+H2O═2NO3-+NO+2H+ | |
| D. | 用KIO3 氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com