
����Ŀ��ʳ�����ճ�����ı���Ʒ��Ҳ����Ҫ�Ļ���ԭ�ϣ�
��ʳ�γ���������Ca2+��Mg2+��SO42�����������ӣ�ʵ�����ṩ���Լ����£�����Na2CO3��Һ������K2CO3��Һ��NaOH��Һ��BaCl2��Һ��Ba��NO3��2��Һ��75%�Ҵ������Ȼ�̼��ʵ�����ᴿNaCl��������ͼ1��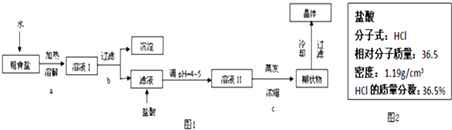
��1������ȥ��Һ���е�Ca2+��Mg2+��SO42�����ӣ���ʵ�����ṩ���Լ���ѡ�������μ�˳������Ϊ
��2����д�������Լ�����ʱ������Ӧ�����ӷ�Ӧ����ʽ��
�����Լ�i����
�����Լ�iii���� ��
��3��ϴ�ӳ�ȥNaCl������渽��������KCl��ѡ�õ��Լ�Ϊ �� �����ṩ���Լ���ѡ��
��4��ʵ�����õ�����������ʵ���Ũ��Ϊ0.400mol/L����ʵ����ijŨ�����Լ�ƿ�ϵ��й�������ͼ2��
����ͼ2������Ũ��������ʵ������Ũ�ȵ�ϡ����480mL��
��������Ҫ�IJ����������ձ�������������ͷ�ιܡ��������������ƣ�
������ȡ��Ũ��������Ϊ�� ��
���𰸡�
��1��NaOH��Һ��BaCl2��Һ������Na2CO3��Һ
��2��Mg2++2OH-=Mg��OH��2����Ba2++CO32��=BaCO3����Ca2++CO32��=CaCO3��
��3��75%�Ҵ�
��4��20mL��Ͳ��500mL����ƿ��16.8mL
���������⣺����Һ���п����μ����������ơ��Ȼ���������̼������Һ������������Һ�����Ȼ��ơ��������ƺ�̼���ƣ��������ᣬ������Һ��Ϊ�Ȼ��ƣ�����Ũ������ȴ�ᾧ�ɵõ��Ȼ��ƾ��壮��1������ȥ��Һ���е�Ca2+��Mg2+��Fe3+��SO42�����ӣ�Ӧ���ȼ���������������Ƴ�ȥþ���Ӻ����������ӣ�Ȼ�����������Ȼ������Գ�ȥ��������ӣ�����������ı���̼������Һ��ȥ�����ı����Ӻ����ӣ����Դ��ǣ�NaOH��Һ��BaCl2��Һ������Na2CO3��Һ����2�������������ƺ�������������þ���ӷ�Ӧ����������þ���������ӷ���ʽΪ��Mg2++2OH-=Mg��OH��2��������̼���ƺ�������̼������ӷ�Ӧ����̼��Ƴ��������ӷ���ʽΪ��Ba2++CO32��=BaCO3������������̼������ӷ�Ӧ����̼�ᱵ���������ӷ���ʽ��Ca2++CO32��=CaCO3�������Դ��ǣ�Mg2++2OH-=Mg��OH��2����Ba2++CO32��=BaCO3����Ca2++CO32��=CaCO3������3����ȥNaCl��������������KCl��Ӧѡ��75%���Ҵ�����ΪCCl4�ж���ͬʱKClҲ�����ܽ���CCl4�У����Դ��ǣ�75%�Ҵ�����4������Ũ��Һ����ϩ��Һ�IJ���Ϊ���������Ҫ��Ũ��������16.8mL����20mL��Ͳ��ȡ����Ҫ��Ũ�������������ձ���ϡ�ͣ�������Ͳ��ȡˮ�����ò��������裬��ȴ��ת�Ƶ�500mL����ƿ�У����ò�����������ϴ�Ӳ���ϴ��Һ��������ƿ�У�����ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμ�����Һ������̶���ˮƽ���У��Ǻ�ƿ����ҡ�ȣ����Ի���Ҫ�IJ��������У�20mL��Ͳ����ͷ�ιܡ����������ձ���500mL����ƿ�����Դ��ǣ�20mL��Ͳ��500mL����ƿ���ڴ�Ũ�����Լ�ƿ�ϵ��й����ݿ�֪������ܶ�Ϊ1.19g/mL����������Ϊ36.5%��Ħ������Ϊ36.5g/mol������C= ![]() ����Ũ��������ʵ���Ũ��Ϊ��C=
����Ũ��������ʵ���Ũ��Ϊ��C= ![]() mol/L=11.9mol/L��ϡ��ǰ����Һ���������Ȼ�������ʵ������䣬������Ũ��������ΪVmL����11.9mol/L��V=0.400mol/L��500mL�����V=16.8mL�����Դ��ǣ�16.8mL��
mol/L=11.9mol/L��ϡ��ǰ����Һ���������Ȼ�������ʵ������䣬������Ũ��������ΪVmL����11.9mol/L��V=0.400mol/L��500mL�����V=16.8mL�����Դ��ǣ�16.8mL��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�Dz��ֶ�����Ԫ�صĵ��ʼ��仯���������Һ����ת����ϵ����֪B��C��D��E�Ƿǽ����������ڳ��³�ѹ�¶������壻������G����ɫ��ӦΪ��ɫ��������I��Jͨ��״���³���̬����Ӧ���ǻ��������е�һ�̵ֹ���Ӧ�� 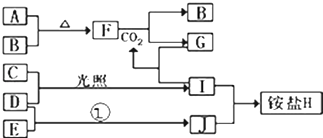
��1��H�Ļ�ѧʽ
��2���õ���ʽ��ʾCO2���γɹ��̣� ��
��3��д��D��E��Ӧ�Ļ�ѧ����ʽ��
��4��д��������G��I��Ӧ�����ӷ���ʽ
��5��F��CO2�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��C��D֮����û�ת����ϵ��ͼ��ʾ����A��DΪ���ʡ�����˵����ȷ����
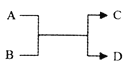
A. ��AΪFe��DΪH2����Bһ��Ϊ��
B. ��AΪ�ǽ������ʣ���D ��һ��Ϊ�ǽ�������
C. ��AΪ�������ʣ�DΪ�ǽ������ʣ���Dһ����H2
D. ��A��D��Ϊ�������ʣ������Ԫ�صĽ�����A��ǿ��D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ��Cl-�IJⶨ�����������ζ�����ʵ�鲽�輰�ⶨԭ�����£�
I��ˮ����Ԥ������
��1�����ˮ��������ɫ������Ҫ���������������崦���������˸ý����_______�ԡ�
��2�����ˮ�����������ߣ�����Ҫ���������ؾ��壬��к��ټ��������Ҵ������������и�����ر�����______�ԣ������Ҵ���Ŀ���ǣ�______��
II����Ʒ�IJⶨ��
������������ˮ��������ƿ�У�����������ϡK2CrO4��Һ��ָʾ������AgNO3 ����Һ�ζ���ש��ɫ������Ag2CrO4���պó��֣��Ұ���Ӳ���ʧʱ����Ϊ�ζ��յ㡣��֪Ksp(AgCl)=1.6 ��10-10��Ksp(Ag2CrO4)=9.0��10-12��Ksp(AgOH)=2.0��10-8��
��3��AgNO3 ����Һ������ɫ_______ʽ�ζ����С�
��4��ʵ�������ϸ����ˮ����pH��ָʾ�������������pH���ߣ���ʹ�ⶨ���_____����ƫ�ߡ�ƫ�ͻ䣬��ͬ�������pH ���ͣ���ʹָʾ��ת��Ϊ Cr2O72����ʧЧ�����ָʾ�������ʹ�ⶨ���________��
��5��ȡ50.00mLˮ������Ũ��Ϊcmol/ AgNO3����Һ�ζ�������ζ��յ�ʱ���ĵ����ΪVmL������Ʒ��Cl-�ĺ���Ϊ_____mg/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�ת���ڸ�����������ʵ�ֵ���
��FeS2 ![]() SO2
SO2![]() H2SO4 ��SiO2
H2SO4 ��SiO2![]() SiCl4
SiCl4![]() Si
Si
�۱���NaCl![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
��Al![]() NaAlO2
NaAlO2![]() AlCl3(aq)
AlCl3(aq) ![]() AlCl3(s)
AlCl3(s)
��CuSO4(aq)![]() Cu(OH)2
Cu(OH)2![]() Cu2O
Cu2O
A. �٢ۢ� B. �ڢۢ� C. �ڢܢ� D. �٢ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ϊ1L�ĺ����ܱ������У�����1 mol CO2��3 mol H2�����������·�����Ӧ:
CO2��g��+3H2��g��CH3OH��g��+H2O��g�������CO2��CH3OH��g����Ũ����ʱ��仯��ͼ��ʾ������˵����ȷ����

A. �û�ѧ��Ӧ��3 minʱ�ﵽƽ��״̬
B. ���������������䣬�����¶�ƽ��ʱc(CH3OH) =0.85mol��L-1����÷�Ӧ����H<0
C. ��ͬ�¶��£���ʼʱ�����������г���0.5 mol CO2��1.5 molH2��ƽ��ʱCO2��ת����С��75%
D. 12 minʱ���������������ٳ���0.25 mol CO2��0. 25 mol H2O(g)����ʱ��Ӧ�����淴Ӧ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�г���ͼ��ֱ�۵�������ѧ��Ӧ�Ľ��̻���������ͼ��������ȷ����
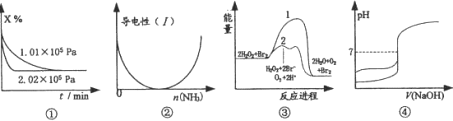
A. ͼ�ٱ�ʾ��ͬѹǿ�Է�Ӧ��ϵ3X(g) ![]() 2Y(g)+Z(s)��X���������Ӱ��
2Y(g)+Z(s)��X���������Ӱ��
B. ͼ�ڱ�ʾCH3COOH��Һ��ͨ��NH3�������Ĺ�������Һ�����Եı仯
C. ͼ���е�����2��ʾ���ȷ�Ӧ2H2O2=2H2O+O2�������Br2�ķ�Ӧ����
D. ͼ����ʾ��0.1000mol��L-lNaOH��Һ�ֱ�ζ�ͬŨ��ͬ�������ʹ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ɸ�������ɺ����ʽ��з��࣬�磺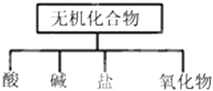
��1����ͼ��ʾ�����ʷ���������� ��
��2����Na��K��H��O��C��S��N���������ֻ�����Ԫ����ɺ��ʵ����ʣ��ֱ������±��ڢۢĺ��森
���� | �� | �� | �� | ������ |
��ѧʽ | ��HCl | �� | ��Na2CO3 | ��CO2 |
��3��д����ת��Ϊ�ݵĻ�ѧ����ʽ ��
��4��ʵ�����Ʊ����������ķ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йء���ѧ���������������ȷ����
A. �ӹ��������ˮ�Ե�ֲ����ά������ʳ������
B. ȥƤƻ�����ڿ����о��ñ����ֽ�ž��ñ�Ƶ�ԭ������ͬ
C. ���ˮ���İ�װ���з�����ݹ����Ը��������Һ�Ĺ��������ʵ�����
D. ��װʳƷ�����ϴ�Ϊ������ϩ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com