
| A£® | ¾ł“ęŌŚµēĄėĘ½ŗā | B£® | ŅõĄė×ÓŹżÄæĒ°Õß“óÓŚŗóÕß | ||
| C£® | c£ØOH-£©Ē°Õߊ”ÓŚŗóÕß | D£® | “ęŌŚµÄĮ£×ÓÖÖĄąĻąĶ¬ |
·ÖĪö A”¢ČĪŗĪČÜŅŗÖŠ¾ł“ęŌŚĖ®µÄµēĄėĘ½ŗā£¬ŌŚĖ®ČÜŅŗÖŠĢ¼ĖįĒāøł“ęŌŚµēĄėĘ½ŗāŗĶĖ®½āĘ½ŗā£»
B”¢CO32-µÄĖ®½ā»įµ¼ÖĀŅõĄė×ÓøöŹżŌö¶ą£»
C”¢Ģ¼ĖįøłµÄĖ®½ā³Ģ¶Č“óÓŚĢ¼ĖįĒāøł£¬Ė®½ā¹ęĀÉ£ŗĖĒæĻŌĖŠŌ£»
D”¢øł¾ŻČÜŅŗÖŠ“ęŌŚµÄĪ¢Į£Ą“»Ų“š£»
½ā“š ½ā£ŗA”¢Na2CO3ČÜŅŗÖŠ“ęŌŚĖ®µÄµēĄėĘ½ŗāŗĶĢ¼ĖįøłµÄĖ®½āĘ½ŗā£¬NaHCO3ŌŚĖ®ČÜŅŗÖŠ“ęŌŚĢ¼ĖįĒāøłµÄµēĄėĘ½ŗāŗĶĖ®½āĘ½ŗāŅŌ¼°Ė®µÄµēĄėĘ½ŗā£¬¹ŹAÕżČ·£»
B”¢Čē¹ū²»æ¼ĀĒĖ®½āµÄ»°£¬ŌņµČÅØ¶ČµÄNaHCO3ŗĶNa2CO3ČÜŅŗÖŠŅõĄė×ӵďżÄæĻąµČ£¬µ«CO32-µÄĖ®½ā»įµ¼ÖĀŅõĄė×ÓøöŹżŌö¶ą£¬¹ŹŅõĄė×ӵďżÄæŗóÕߓ󣬹ŹB“ķĪó£»
C”¢Ģ¼ĖįøłµÄĖ®½ā³Ģ¶Č“óÓŚĢ¼ĖįĒāøł£¬¶žÕßĖ®½ā¾łĻŌ¼īŠŌ£¬øś¾ŻĖ®½ā¹ęĀÉ£ŗĖĒæĻŌĖŠŌ£¬ĖłŅŌĢ¼ĖįÄĘÖŠµÄĒāŃõøłÅØ¶Č“óÓŚĢ¼ĖįĒāÄĘČÜŅŗÖŠµÄĒāŃõøłÅØ¶Č£¬¹ŹCÕżČ·£»
D”¢NaHCO3ŗĶNa2CO3ČÜŅŗÖŠ“ęŌŚµÄĪ¢Į£¾łĪŖ£ŗĢ¼Ėįøł”¢Ģ¼ĖįĒāøł”¢ĒāŃõøł”¢ĒāĄė×Ó”¢Ģ¼Ėį·Ö×Ó”¢Ė®·Ö×Ó£¬“ęŌŚµÄĮ£×ÓÖÖĄąĻąĶ¬£¬¹ŹDÕżČ·£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŃĪµÄĖ®½āµÄÓ¦ÓĆ£¬Ć÷Č·Ė®½āŌĄķ¼°ŃĪĄąĖ®½ā¹ęĀɵÄÓ¦ÓĆŹĒ½āĢāµÄ¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
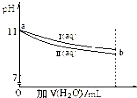
| A£® | I ŗĶ II ČÜŅŗÖŠ£¬Ąė×ÓÖÖĄąŹżĻąĶ¬ | |
| B£® | a µć“¦£¬I ČÜŅŗµÄÅضČĪŖ 10-3mol?L-1 | |
| C£® | a µć“¦£¬I”¢II ¶ŌĖ®µÄµēĄėĘ½ŗāÓ°ĻģĻąĶ¬ | |
| D£® | b “¦µÄ I”¢II ČÜŅŗ·Ö±šÓėŃĪĖį·“Ó¦£¬I ĻūŗÄ HCl ĪļÖŹµÄĮæ±Č II ¶ą |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “æ¼īČÜŅŗæÉČ„³żÓĶĪŪ | |
| B£® | ÓĆNaHCO3ČÜŅŗŗĶAl2£ØSO4£©3ČÜŅŗæÉŅŌÖĘ×÷ÅŻÄĆš»š¼Į | |
| C£® | TiCl4ČÜÓŚ“óĮæĖ®¼ÓČČÖʱøTiO2 | |
| D£® | ÓĆŠæĮ£ÓėĻ”ĮņĖį·“Ó¦ÖĘČ”ĒāĘųŹ±µĪ¼ÓÉŁĮæCuSO4ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĮņĖį”¢“æ¼ī”¢ĀČĖį¼Ų”¢Ńõ»ÆÄĘ·Ö±šŹōÓŚĖį”¢¼ī”¢ŃĪ”¢¼īŠŌŃõ»ÆĪļ | |
| B£® | ½«±„ŗĶFeCl3ČÜŅŗµĪČėNaOHČÜŅŗÖŠ£¬¼ÓČČÖó·Š£¬æÉÖʵĆFe£ØOH£©3½ŗĢå | |
| C£® | ·“Ó¦8NH3+3Cl2ØTN2+6NH4ClÖŠ£¬Ńõ»Æ¼ĮÓė»¹Ō¼ĮĪļÖŹµÄĮæÖ®±ČŹĒ3£ŗ2 | |
| D£® | ĀČĘųµÄĖ®ČÜŅŗÄܵ¼µē£¬Ņņ“ĖĀČĘųŹōÓŚµē½āÖŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½šøÕŹÆŗĶŹÆÄ« | B£® | ${\;}_{17}^{35}$CLŗĶ${\;}_{17}^{37}$CL | ||
| C£® | ŅŅĶéŗĶ±ūĶé | D£® | T2OŗĶD2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com