
室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中 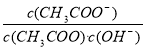 不变
不变
C.醋酸的电离程度增大,c(H+)也增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源:2017届湖北省高三上第四次质检化学试卷(解析版) 题型:填空题
CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品.
(1)CO与Cl2在催化剂的作用下合成光气(COCl2).某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g) COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
COCl2(g)△H=a kJ/mol反应过程中测定的部分数据如下表:
t/min | n (CO)/mol | n (Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
①反应0~2min末的平均速率v(COCl2)= mol/(L·min).
②在2min~4min间,v(Cl2)正 v(Cl2)逆 (填“>”、“=”或“<”),该温度下 K= .
K= .
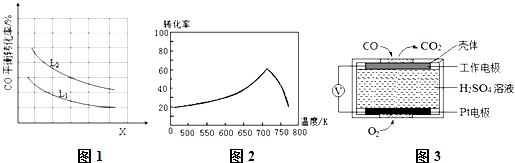
③已知X、L可分别代表温度或压强,图1表示L一定时,CO的转化率随X的变化关系.
X代表的物理量是 ;a 0 (填“>”,“=”,“<”).
(2)在催化剂作用下NO和CO转化为无毒气体,2CO(g)+2NO(g) 2CO2(g)+N2(g)△H=﹣748kJ·mol﹣1
2CO2(g)+N2(g)△H=﹣748kJ·mol﹣1
①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图2所示.温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是 .
②已知:测定空气中NO和CO含量常用的方法有两种,方法1:电化学气敏传感器法.其中CO传感器的工作原理如图3所示,则工作电极的反应式为 ;方法2:氧化还原滴定法.用H2O2溶液吸收尾气,将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸浓度.写出NO与H2O2溶液反应的离子方程式 .
(3)用CO和H2可以制备甲醇,反应为CO(g)+2H2(g) CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中K
CH3OH(g),以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)若电解质溶液中K OH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是 .
OH的物质的量为0.8mol,当有0.5mol甲醇参与反应时,电解质溶液中各种离子的物质的量浓度由大到小的顺序是 .
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:填空题
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
阳离子 | Na+、K+、Cu2+ |
阴离子 | SO42-、OH- |
在下图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极。接通电源,经过一段时间后,测得乙烧杯中c电极质量增加了16g。常温下各烧杯中溶液的pH与电解时间t的关系如图。据此回答下列问题:
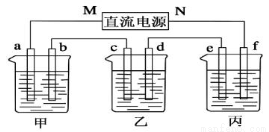
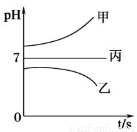
(1)M为电源的_______________极(填“正”或“负”),电极b上发生的电极反应为_____________。
(2)电极e上生成的气体在标准状态下的体积为________。
(3)写出乙烧杯中的电解池反应___________________。
(4)若电解过程中,乙烧杯中的B溶液中的金属离子全部析出,此时电解还能继续进行,原因是________________。
(5)若经过一段时间后,测得乙烧杯中c电极质量增加了16g,要使丙烧杯中的C溶液恢复到原来的状态,正确的操作是________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
在某一个容积为2L的密闭容器内,加入0.2mol的CO和0.2mol的H2O,在催化剂存在的条件下高温加热,发生如下反应:CO(g)+H2O(g)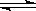 CO2(g)+H2(g)△H=akJ/mol(a>0)达到平衡后,测得c(CO):c(CO2)=3:2.下列说法正确的是
CO2(g)+H2(g)△H=akJ/mol(a>0)达到平衡后,测得c(CO):c(CO2)=3:2.下列说法正确的是
A.反应放出的热量为0.2akJ
B.平衡时H2O的转化率为40%
C.升高温度,v(正)加快v(逆)减慢,平衡正向移动
D.将容器的体积压缩为1L,该平衡正向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
室温时下列溶液中的粒子浓度关系正确的是
A.相同物质的量浓度的溶液:①(NH4)2SO4②NH4HCO3③NH4Cl④NH3·H2O中,c(NH4)由大到小的顺序是:①>③>②>④
B.将等体积的盐酸和氨水混合后pH=7:c(NH4+)>c(Cl-)
C.0.1mol·L-1Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
D.向硝酸钠溶液中滴加稀盐酸得到pH=5的混合溶液:c(Na+)=c(NO3-)+c(Cl-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
常温下,下列四种溶液中由电离生成的c(H+)之比(①∶②∶③∶④)为
①1mol/L的盐酸;②0.1mol/L盐酸;③0.01mol/L的NaOH溶液;④1mol/L的NaOH溶液.
A.1:10:100:1 B.1:10-1:10-12:10-14
C.14:13:12:14 D.1:2:12:14
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二上期中化学卷(解析版) 题型:选择题
为了测定酸碱反应的中和热,计算时至少需要的数据是
①酸溶液的浓度和体积 ; ②碱溶液的浓度和体积 ;③比热容;④反应后溶液的质量;⑤ 生成水的物质的量;⑥反应前后温度的变化; ⑦操作所需的时间。
A.①②③⑥ B.③④⑤⑥ C.①③④⑤ D.全部
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上月考二化学卷(解析版) 题型:选择题
将氨水滴加到盛有AgCl的试管中直至AgCl完全溶解,对上述过程的有关解释或叙述正确的是
A.所得溶液中c(Ag+ )· c(Cl-)>Ksp(AgCl)
B.上述实验说明Cl-与NH4+间有很强的结合力
C.所得溶液中形成了难电离的物质
D.上述过程中NH3·H2O的电离常数增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是
A.将纯水加热到95℃,KW变大,PH不变,水仍呈中性
B.向纯水中加入稀氨水,平衡逆向移动,c(OH-)降低
C.向水纯中加入少量固体硫酸氢钠,c(H+)增大,KW不变,影响水的电离平衡
D.向水纯中加入醋酸钠或盐酸,均可抑制水的电离,KW不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com