
”¾ĢāÄæ”æ”°±ä»Æ¹ŪÄīÓėĘ½ŗāĖ¼Ļė”±ŹĒ»ÆѧѧæʵÄŗĖŠÄĖŲŃų£¬ŹŅĪĀŹ±£¬0.1 mol”¤L1²ŻĖįÄĘČÜŅŗÖŠ“ęŌŚ¶ąøöĘ½ŗā£¬ĘäÖŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ[¼ŗÖŖŹŅĪĀŹ±£¬Ksp(CaC2O4)=2.4”Į109]
A. Čō½«ČÜŅŗ²»¶Ļ¼ÓĖ®Ļ”ŹĶ£¬ŌņĖ®µÄµēĄė³Ģ¶ČŌö“ó
B. ČÜŅŗÖŠø÷Ąė×ÓÅØ¶Č“óŠ”¹ŲĻµ£ŗc(Na+)> c(C2O42)> c(OH)> c(H+)> c(HC2O4)
C. ČōÓĆpH¼Ę²āµĆČÜŅŗµÄpH=9£¬ŌņH2C2O4µÄµŚ¶ž¼¶µēĄėĘ½ŗā³£ŹżKa2=105
D. ĻņČÜŅŗÖŠ¼ÓČėµČĢå»żCaCl2ČÜŅŗ£¬µ±¼ÓČėµÄCaCl2ČÜŅŗÅØ¶Č“óÓŚ2.4”Į108 mol”¤L1 Ź±¼“ÄܲśÉś³Įµķ
”¾“š°ø”æC
”¾½āĪö”æA”¢ČōĻņČÜŅŗÖŠ²»¶Ļ¼ÓĖ®Ļ”ŹĶ£¬ŃĪĄąĖ®½ā³Ģ¶ČŌö“󣬵«Ė®µÄµēĄė³Ģ¶Č¼õŠ”£¬¹ŹA“ķĪó£»B£®0.10mol/L²ŻĖįÄĘČÜŅŗÖŠ²ŻĖįøłĄė×Ó·Ö²½Ė®½āČÜŅŗĻŌ¼īŠŌ£¬ČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”ĪŖ£ŗc(Na+)£¾c(C2O42-)£¾c(OH-)£¾c(HC2O4-)£¾c(H+)£¬¹ŹB“ķĪó£»C£®ČōÓĆpH¼Ę²āµĆČÜŅŗµÄpH=9£¬c(OH-)=c(HC2O4-)=10-14+9mol/L£¬C2O42-+H2O![]() HC2O4-+OH-£¬Kh=
HC2O4-+OH-£¬Kh=![]() =
=![]() ”Į
”Į![]() =
=![]() =
=![]() £¬Ka2=10-5£¬¹ŹCÕżČ·£»D£®ksp(CaC2O4)=c(Ca2+)c(C2O42-)=2.4”Į10-9£¬c(Ca2+)=
£¬Ka2=10-5£¬¹ŹCÕżČ·£»D£®ksp(CaC2O4)=c(Ca2+)c(C2O42-)=2.4”Į10-9£¬c(Ca2+)=![]() =4.8”Į10-8mol/L£¬¹ŹD“ķĪó£»¹ŹŃ”C”£
=4.8”Į10-8mol/L£¬¹ŹD“ķĪó£»¹ŹŃ”C”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹÖ³Ö¼¼ŹõŹĒ»łÓŚŹż¾Ż²É¼ÆĘ÷”¢“«øŠĘ÷ŗĶ¶ąĆ½Ģå¼ĘĖ滜¹¹³ÉµÄŅ»ÖÖŠĀŠĖÕĘÉĻŹŌŃéĻµĶ³£¬¾ßÓŠŹµŹ±”¢¶ØĮ攢ֱ¹ŪµČĢŲµć£¬ĻĀĶ¼ŹĒĄūÓĆŹÖ³Ö¼¼ŹõµĆµ½µÄĪ¢Į£ĪļÖŹµÄĮæ±ä»ÆĶ¼£¬³£ĪĀĻĀĻņ![]() ČÜŅŗÖŠµĪ¼Ó
ČÜŅŗÖŠµĪ¼Ó![]() ČÜŅŗ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
ČÜŅŗ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ![]()

A.![]() AŌŚĖ®ÖŠµÄµēĄė·½³ĢŹ½ŹĒ£ŗ
AŌŚĖ®ÖŠµÄµēĄė·½³ĢŹ½ŹĒ£ŗ![]()
![]()
![]() £»HA
£»HA![]()
B.µ±![]() Ź±£¬ŌņÓŠ£ŗ
Ź±£¬ŌņÓŠ£ŗ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
C.µ±![]() Ź±£¬ŌņÓŠ£ŗ
Ź±£¬ŌņÓŠ£ŗ![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
D.µ±![]() Ź±£¬ĘäČÜŅŗÖŠĖ®µÄµēĄėŹÜµ½ŅÖÖĘ
Ź±£¬ĘäČÜŅŗÖŠĖ®µÄµēĄėŹÜµ½ŅÖÖĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓƵēµ¼ĀŹ“«øŠĘ÷æÉ»ęÖʵēµ¼ĀŹĒśĻßĶ¼£¬ĻĀĶ¼ĪŖÓĆ0.1mol/LNaOHČÜŅŗµĪ¶Ø10mL0.lmol/LŃĪĖį¹ż³ĢÖŠµÄµēµ¼ĀŹĒśĻß”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ

A. µēµ¼ĀŹ“«øŠĘ÷ÄÜÓĆÓŚÅŠ¶ĻĖį¼īÖŠŗĶµĪ¶ØµÄÖÕµć
B. a”¢b”¢c µćµÄČÜŅŗÖŠ£¬Ąė×ÓÅضČÓɓ󵽊”Ė³ŠņĪŖa>b>c
C. dµćĖłŹ¾ČÜŅŗÖŠ“ęŌŚ£ŗc(Cl-) +c(OH-) =c(H+) +c(Na+)
D. Cµćµēµ¼ĀŹ×īŠ”ŹĒŅņĪŖ“ĖŹ±ČÜŅŗÖŠµ¼µēĪ¢Į£ŹżÄæ×īÉŁ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ![]() µÄX”¢Y”¢ZČżÖÖĖįµÄĖ®ČÜŅŗø÷1mL£¬·Ö±š¼ÓĖ®Ļ”ŹĶµ½1000mL£¬ĘäpHÓėČÜŅŗĢå»ż
µÄX”¢Y”¢ZČżÖÖĖįµÄĖ®ČÜŅŗø÷1mL£¬·Ö±š¼ÓĖ®Ļ”ŹĶµ½1000mL£¬ĘäpHÓėČÜŅŗĢå»ż![]() µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬X”¢Z²»ĪŖĘ½ŠŠĻß”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬X”¢Z²»ĪŖĘ½ŠŠĻß”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A.ŌČÜŅŗ¶¼ŹĒĻ”ČÜŅŗ
B.ŌČÜŅŗµÄÅØ¶Č“óŠ”ĪŖ![]()
C.ZŹĒĒæĖį£¬YŗĶXŹĒČõĖį
D.![]() ČÜŅŗÖŠĪ¢Į£ÅضČ
ČÜŅŗÖŠĪ¢Į£ÅضČ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬![]() ŗĶ
ŗĶ![]() Į½ÖÖĖįČÜŅŗ£¬ĘšŹ¼Ź±ČÜŅŗĢå»ż¾łĪŖ
Į½ÖÖĖįČÜŅŗ£¬ĘšŹ¼Ź±ČÜŅŗĢå»ż¾łĪŖ![]() ”£·Ö±šĻņĮ½ČÜŅŗÖŠ¼ÓĖ®½ųŠŠĻ”ŹĶ£¬Ļ”ŹĶŗóČÜŅŗµÄĢå»żĪŖV£¬ČÜŅŗpHĖę
”£·Ö±šĻņĮ½ČÜŅŗÖŠ¼ÓĖ®½ųŠŠĻ”ŹĶ£¬Ļ”ŹĶŗóČÜŅŗµÄĢå»żĪŖV£¬ČÜŅŗpHĖę![]() µÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
µÄ±ä»ÆČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A.µČĪļÖŹµÄĮæÅØ¶ČµÄ![]() ŗĶ
ŗĶ![]() ČÜŅŗÖŠ£¬ŗóÕßĖ®µÄµēĄė³Ģ¶Č“ó
ČÜŅŗÖŠ£¬ŗóÕßĖ®µÄµēĄė³Ģ¶Č“ó
B.µ±Ļ”ŹĶÖĮ![]() Ź±£¬µČĢå»żµÄĮ½ÖÖĖįÖŠŗĶ
Ź±£¬µČĢå»żµÄĮ½ÖÖĖįÖŠŗĶ![]()
C.µ±Į½ČÜŅŗ¾łĻ”ŹĶÖĮ![]() Ź±£¬ČÜŅŗÖŠ£ŗ
Ź±£¬ČÜŅŗÖŠ£ŗ![]()
D.![]() µÄµēĄė·½³ĢŹ½£ŗ
µÄµēĄė·½³ĢŹ½£ŗ![]()
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ![]() £¬
£¬![]() ”£ĻĀĮŠ¹ŲÓŚÄŃČÜĪļÖ®¼ä×Ŗ»ÆµÄĖµ·ØÖŠ“ķĪóµÄŹĒ
”£ĻĀĮŠ¹ŲÓŚÄŃČÜĪļÖ®¼ä×Ŗ»ÆµÄĖµ·ØÖŠ“ķĪóµÄŹĒ
A.AgCl²»ČÜÓŚĖ®£¬²»ÄÜ×Ŗ»ÆĪŖAgI
B.Į½ÖÖÄŃČÜĪļµÄ![]() Ļą²īŌ½“ó£¬ÄŃČÜĪļ¾ĶŌ½ČŻŅ××Ŗ»ÆĪŖøüÄŃČܵÄĪļÖŹ
Ļą²īŌ½“ó£¬ÄŃČÜĪļ¾ĶŌ½ČŻŅ××Ŗ»ÆĪŖøüÄŃČܵÄĪļÖŹ
C.AgI±ČAgCløüÄŃČÜÓŚĖ®£¬ĖłŅŌAgClæÉŅŌ×Ŗ»ÆĪŖAgI
D.³£ĪĀĻĀ£¬AgClČōŅŖŌŚNaIČÜŅŗÖŠæŖŹ¼×Ŗ»ÆĪŖAgI£¬ŌņNaIµÄÅØ¶Č±ŲŠė²»µĶÓŚ![]() ”Į10-11
”Į10-11
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æt”ꏱ£¬Ā±»ÆŅų£ØAgX£¬X=Cl£¬Br£©µÄ2ĢõČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬ŅŃÖŖAgCl£¬AgBrµÄKspŅĄ“Ī¼õŠ”£¬ĒŅp(Ag+)=-lgc(Ag+)£¬p(X-)=-lgc(X-)£¬ĄūÓĆpX-pAgµÄ×ų±źĻµæɱķŹ¾³öAgXµÄČܶȻżÓėČÜŅŗÖŠµÄc(Ag+)ŗĶc(X-)µÄĻą»„¹ŲĻµ£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
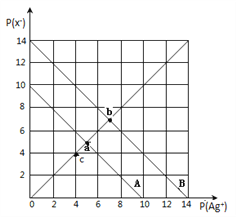
A. t”ꏱ£¬cµćæɱķŹ¾AgClµÄ²»±„ŗĶČÜŅŗ
B. BĻß±ķŹ¾µÄŹĒAgBr
C. Č”a”¢bĮ½µć“¦ČÜŅŗµČĢå»ż»ģŗĻ£¬Ī¬³Öt”ę²»±ä£¬»ģŗĻČÜŅŗÖŠŅ»¶ØĪŽ°×É«³ĮµķÉś³É
D. ŌŚt”ꏱ,AgCl(s)+Br-(aq)![]() AgBr(s)+Cl-(aq)Ę½ŗā³£ŹżK”Ö104
AgBr(s)+Cl-(aq)Ę½ŗā³£ŹżK”Ö104
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææÉÄę·“Ó¦£ŗ2NO2(g)![]() 2NO(g)+O2(g)ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ( )
2NO(g)+O2(g)ŌŚĆܱÕČŻĘ÷ÖŠ·“Ó¦£¬“ļµ½Ę½ŗāדĢ¬µÄ±źÖ¾ŹĒ( )
¢Łµ„Ī»Ź±¼äÄŚÉś³Én mol O2µÄĶ¬Ź±Éś³É2n mol NO2
¢Śµ„Ī»Ź±¼äÄŚÉś³Én mol O2µÄĶ¬Ź±£¬Éś³É2n mol NO
¢ŪÓĆNO2”¢NO”¢O2µÄĪļÖŹµÄĮæÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹµÄ±ČĪŖ2:2:1µÄדĢ¬
¢Ü»ģŗĻĘųĢåµÄŃÕÉ«²»ŌŁøıäµÄדĢ¬
¢Ż»ģŗĻĘųĢåµÄĆÜ¶Č²»ŌŁøıäµÄדĢ¬
¢Ž»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»ŌŁøıäµÄדĢ¬
A. ¢Ł¢Ü¢ŽB. ¢Ś¢Ū¢ŻC. ¢Ł¢Ū¢ÜD. ¢Ł¢Ś¢Ū¢Ü¢Ż¢Ž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ŌĖ®ŃłÖŠČÜÖŹMµÄ·Ö½āĖŁĀŹÓ°ĻģŅņĖŲ½ųŠŠŃŠ¾æ”£ŌŚĻąĶ¬ĪĀ¶ČĻĀ£¬MµÄĪļÖŹµÄĮæÅضČ(mol”¤L-1)Ėꏱ¼ä(min)±ä»ÆµÄÓŠ¹ŲŹµŃ鏿¾Ż¼ūĻĀ±ķ”£
Ź±¼ä Ė®Ńł | 0 | 5 | 10 | 15 | 20 | 25 |
¢ń(pH£½2) | 0.40 | 0.28 | 0.19 | 0.13 | 0.10 | 0.09 |
¢ņ(pH£½4) | 0.40 | 0.31 | 0.24 | 0.20 | 0.18 | 0.16 |
¢ó(pH£½4) | 0.20 | 0.15 | 0.12 | 0.09 | 0.07 | 0.05 |
¢ō(pH£½4£¬ŗ¬Cu2+) | 0.20 | 0.09 | 0.05 | 0.03 | 0.01 | 0 |
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A. ŌŚ0”«20minÄŚ£¬IÖŠMµÄ·Ö½āĖŁĀŹĪŖ0.015 mol”¤L-1”¤min-1
p>B. Ė®ŃłĖįŠŌŌ½Ē棬MµÄ·Ö½āĖŁĀŹŌ½æģC. ŌŚ0”«25minÄŚ£¬IIIÖŠMµÄ·Ö½ā°Ł·ÖĀŹ±ČII“ó
D. ÓÉÓŚCu2+“ęŌŚ£¬IVÖŠMµÄ·Ö½āĖŁĀŹ±ČIæģ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com