
”¾ĢāÄæ”æĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼ĖłŹ¾£¬X”¢YµÄŗĖĶāµē×ÓŹżÖ®ŗĶµČÓŚWµÄŗĖĶāµē×ÓŹż£¬ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
![]()
A.X”¢Y”¢ZČżÖÖŌŖĖŲµÄ×īøßÕż¼ŪŅĄ“ĪŌö“ó
B.Y”¢ZŠĪ³ÉµÄ¼ņµ„Ēā»ÆĪļ£¬ŗóÕßĪČ¶ØŠŌĒæ
C.Y”¢ZŠĪ³ÉµÄ¼ņµ„ŅõĄė×Ó£¬ŗóÕß°ė¾¶Š”
D.¹¤ŅµÉĻÓƵē½āWŗĶZŠĪ³ÉµÄ»ÆŗĻĪļÖʱøµ„ÖŹW
”¾“š°ø”æA
”¾½āĪö”æ
øł¾Ż³£¼ūŌŖĖŲŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆ¼°ŌŖĖŲÖÜĘŚ±ķµÄ½į¹¹ÖŖ£¬X”¢Y”¢ZĪ»ÓŚµŚ¶žÖÜĘŚ£¬WĪ»ÓŚµŚČżÖÜĘŚ£¬X”¢YµÄŗĖĶāµē×ÓŹżÖ®ŗĶµČÓŚWµÄŗĖĶāµē×ÓŹż£¬ŌņXĪŖCŌŖĖŲ£¬YĪŖNŌŖĖŲ£¬ZĪŖOŌŖĖŲ£¬WĪŖAlŌŖĖŲ”£
A. ÓÉ·ÖĪöæÉÖŖ£¬XĪŖCŌŖĖŲ£¬YĪŖNŌŖĖŲ£¬ZĪŖOŌŖĖŲ£¬OŌŖĖŲƻӊ×īøßÕż¼Ū£¬¹ŹA“ķĪó£»
B. ÓÉ·ÖĪöæÉÖŖ£¬Y”¢ZŠĪ³ÉµÄ¼ņµ„Ēā»ÆĪļĪŖNH3ŗĶH2O£¬µŖ£¬ŃõŌŖĖŲÖŠŃõµÄµēøŗŠŌ×ī“ó£¬ŃõÓėĒāÖ®¼äµÄ¹²¼Ū¼ü×īĄĪ¹Ģ£¬ĖłŅŌŃõµÄĒā»ÆĪļH2OøüĪČ¶Ø£¬¹ŹBÕżČ·£»
C. µē×Ó²ć½į¹¹ĻąĶ¬µÄĄė×Ó£¬ŗĖµēŗÉŹżŌ½“󣬰ė¾¶Ō½Š”£¬ŃõµÄŗĖµēŗÉŹż“óÓŚµŖŌŖĖŲ£¬ĖłŅŌŗóÕß°ė¾¶Š”£¬¹ŹCÕżČ·£»
D. ¹¤ŅµÉĻÓƵē½āAlŗĶOŠĪ³ÉµÄ»ÆŗĻĪļAl2O3Öʱøµ„ÖŹAl£¬¹ŹDÕżČ·£»
ĢāÄæŅŖĒóŃ”“ķĪóĻī£¬¹ŹŃ”A”£


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£Øb£©![]() ”¢£Ød£©
”¢£Ød£©![]() ”¢£Øp£©
”¢£Øp£©![]() µÄ·Ö×ÓŹ½¾łĪŖC6H6£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
µÄ·Ö×ÓŹ½¾łĪŖC6H6£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. bµÄĶ¬·ÖŅģ¹¹ĢåÖ»ÓŠdŗĶpĮ½ÖÖB. b”¢d”¢pµÄ¶žĀČ“śĪļ¾łÖ»ÓŠČżÖÖ
C. b”¢d”¢p¾łæÉÓėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ·“Ó¦D. b”¢d”¢pÖŠÖ»ÓŠbµÄĖłÓŠŌ×Ó“¦ÓŚĶ¬Ņ»Ę½Ćę
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚĢå»żĻąĶ¬µÄĮ½øöĆܱÕČŻĘ÷ÖŠ·Ö±š³äĀśC2H4ŗĶC3H6ĘųĢ壬µ±ÕāĮ½øöĆܱÕČŻĘ÷ÖŠĪĀ¶ČŗĶĘųĢåĆܶČĻąµČŹ±£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. Į½ÖÖĘųĢåµÄ·Ö×ÓŹżĻąµČ B. C£²H£“±ČC£³H£¶µÄÖŹĮ抔
C. Į½ÖÖĘųĢåµÄŃ¹ĒæĻąµČ D. Į½ÖÖĘųĢåµÄŌ×ÓŹżĻąµČ£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ450”ꏱ£¬ŌŚÄ³ŗćČŻĆܱÕČŻĘ÷ÖŠ“ęŌŚ·“Ó¦£ŗC(s)£«2NO(g)![]() N2(g)£«CO2(g)£¬ĻĀĮŠĖµ·ØÄÜ×÷ ĪŖÅŠ¶ĻøĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬±źÖ¾µÄŹĒ
N2(g)£«CO2(g)£¬ĻĀĮŠĖµ·ØÄÜ×÷ ĪŖÅŠ¶ĻøĆ·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬±źÖ¾µÄŹĒ
A. ČŻĘ÷ÄŚŃ¹Ēæ±£³Ö²»±äB. vÕż(N2)=2vÄę(NO)
C. N2ÓėCO2µÄĪļÖŹµÄĮæÖ®±ČĪŖ1”Ć1D. ČŻĘ÷ÄŚ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A.2,2¶ž¼×»ł¶”ĶéµÄ1HNMRÉĻÓŠ4øö·å
B.![]() ÖŠĖłÓŠŌ×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
ÖŠĖłÓŠŌ×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęÉĻ
C.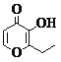 ÓŠ»śĪļµÄŅ»ÖÖ·¼Ļć×åĶ¬·ÖŅģ¹¹ĢåÄÜ·¢ÉśŅų¾µ·“Ó¦
ÓŠ»śĪļµÄŅ»ÖÖ·¼Ļć×åĶ¬·ÖŅģ¹¹ĢåÄÜ·¢ÉśŅų¾µ·“Ó¦
D.¼×±½ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬ĖµĆ÷±½»·Óė¼×»łĻąĮ¬µÄĢ¼Ģ¼µ„¼ü±ä»īĘĆ£¬±»KMnO4Ńõ»Æ¶ų¶ĻĮŃ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ŅŖĒóĶź³ÉĻĀĮŠĢāÄæ£ŗ
(1)Š“³öÓĆNa2O2ÓėĖ®µÄ»Æѧ·½³ĢŹ½£ŗ__________________________________
(2)Š“³öFeŌŚCl2ÖŠČ¼ÉÕ»Æѧ·½³ĢŹ½£ŗ__________________________________
(3)Š“³öÓĆCl2ÓėNaOHÖĘĻū¶¾ŅŗµÄĄė×Ó·½³ĢŹ½£ŗ______________________________
(4)Š“³öNaHCO3µēĄė·½³ĢŹ½£ŗ___________________________________
(5)Š“³öĒāŃõ»ÆÄĘČÜŅŗÓėĻ”ĮņĖį·“Ó¦µÄĄė×Ó·½³ĢŹ½__________________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØŃ¹ĒæĻĀ£¬Ļņ10 LĆܱÕČŻĘ÷ÖŠ³äČė1 mol S2Cl2ŗĶ1 mol Cl2£¬·¢Éś·“Ó¦S2Cl2(g)£«Cl2(g) ![]() 2SCl2(g)”£Cl2ÓėSCl2µÄĻūŗÄĖŁĀŹ(v)ÓėĪĀ¶Č(T)µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŅŌĻĀĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø £©
2SCl2(g)”£Cl2ÓėSCl2µÄĻūŗÄĖŁĀŹ(v)ÓėĪĀ¶Č(T)µÄ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŅŌĻĀĖµ·ØÖŠ²»ÕżČ·µÄŹĒ£Ø £©
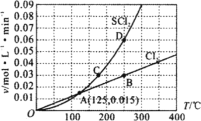
A.Õż·“Ó¦µÄ»ī»ÆÄÜ“óÓŚÄę·“Ó¦µÄ»ī»ÆÄÜ
B.“ļµ½Ę½ŗāŗóŌŁ¼ÓČČ£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅʶÆ
C.A”¢B”¢C”¢DĖĵć¶ŌӦדĢ¬ĻĀ£¬“ļµ½Ę½ŗāדĢ¬µÄĪŖB”¢D
D.Ņ»¶ØĪĀ¶ČĻĀ£¬ŌŚŗćČŻĆܱÕČŻĘ÷ÖŠ£¬“ļµ½Ę½ŗāŗóĖõŠ”ČŻĘ÷Ģå»ż£¬ÖŲŠĀ“ļµ½Ę½ŗāŗó£¬Cl2µÄĘ½ŗā×Ŗ»ÆĀŹ²»±ä
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗĻ³É°±ŹĒČĖĄąæĘѧ¼¼Źõ·¢Õ¹Ź·ÉĻµÄŅ»ĻīÖŲ“óĶ»ĘĘ£¬ŃŠ¾æ±ķĆ÷Ņŗ°±ŹĒŅ»ÖÖĮ¼ŗƵē¢ĒāĪļÖŹ”£
(1) °±Ęų·Ö½ā·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ2NH3(g) ![]() N2(g)£«3H2(g)””¦¤H
N2(g)£«3H2(g)””¦¤H
Čō£ŗN”ŌN¼ü”¢H£H¼üŗĶN£H¼üµÄ¼üÄÜ·Ö±š¼Ē×÷a”¢bŗĶc(µ„Ī»£ŗkJ”¤mol1)ŌņÉĻŹö·“Ó¦µÄ¦¤H£½________kJ”¤mol1”£
(2) ŃŠ¾æ±ķĆ÷½šŹō“߻ƼĮæɼÓĖŁ°±ĘųµÄ·Ö½ā”£ĻĀ±ķĪŖijĪĀ¶ČĻĀµČÖŹĮæµÄ²»Ķ¬½šŹō·Ö±š“߻ƵČÅØ¶Č°±Ęų·Ö½āÉś³ÉĒāĘųµÄ³õŹ¼ĖŁĀŹ(mmol”¤min1)”£
“߻ƼĮ | Ru | Rh | Ni | Pt | Pd | Fe |
³õŹ¼ĖŁĀŹ | 7.9 | 4.0 | 3.0 | 2.2 | 1.8 | 0.5 |
¢Ł²»Ķ¬“߻ƼĮ“ęŌŚĻĀ£¬°±Ęų·Ö½ā·“Ó¦»ī»ÆÄÜ×ī“óµÄŹĒ________(ĢīŠ““߻ƼĮµÄ»ÆѧŹ½)”£
¢ŚĪĀ¶ČĪŖT£¬ŌŚŅ»Ģå»ż¹Ģ¶ØµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė2 mol NH3£¬“ĖŹ±Ń¹ĒæĪŖP0£¬ÓĆRu“߻ư±Ęų·Ö½ā£¬ČōĘ½ŗāŹ±°±Ęų·Ö½āµÄ×Ŗ»ÆĀŹĪŖ50%£¬ŌņøĆĪĀ¶ČĻĀ·“Ó¦2NH3(g) ![]() N2(g)£«3H2(g)ÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č±ķŹ¾µÄ»ÆŃ§Ę½ŗā³£ŹżKp£½________”£[ŅŃÖŖ£ŗĘųĢå·ÖŃ¹(p·Ö)£½ĘųĢå×ÜŃ¹(p×Ü)”ĮĢå»ż·ÖŹż]
N2(g)£«3H2(g)ÓĆĘ½ŗā·ÖŃ¹“śĢęĘ½ŗāÅØ¶Č±ķŹ¾µÄ»ÆŃ§Ę½ŗā³£ŹżKp£½________”£[ŅŃÖŖ£ŗĘųĢå·ÖŃ¹(p·Ö)£½ĘųĢå×ÜŃ¹(p×Ü)”ĮĢå»ż·ÖŹż]
(3) ¹ŲÓŚŗĻ³É°±¹¤ŅÕµÄĄķ½ā£¬ĻĀĮŠÕżČ·µÄŹĒ________”£
A£®ŗĻ³É°±¹¤Ņµ³£²ÉÓƵķ“Ó¦ĪĀ¶ČĪŖ500”ę×óÓŅ£¬æÉÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶ
B£®Ź¹ÓĆ³õŹ¼·“Ó¦ĖŁĀŹøüæģµÄ“߻ƼĮRu£¬²»ÄÜĢįøßĘ½ŗāŹ±NH3µÄ²śĮæĪ
C£®ŗĻ³É°±¹¤Ņµ²ÉÓĆ10 MPa”«30 MPa£¬ŹĒŅņ³£Ń¹ĻĀN2ŗĶH2µÄ×Ŗ»ÆĀŹ²»øß
D£®²ÉÓĆĄäĖ®½µĪĀµÄ·½·Øæɽ«ŗĻ³Éŗó»ģŗĻĘųĢåÖŠµÄ°±Ņŗ»Æ
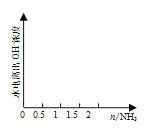
(4) ŌŚ1 L 1 mol”¤L1µÄŃĪĖįÖŠ»ŗ»ŗĶØČė2 mol°±Ęų£¬ĒėŌŚĶ¼ÖŠ»³öČÜŅŗÖŠĖ®µēĄė³öµÄOHÅضČĖę°±ĘųĶØČė±ä»ÆµÄĒ÷ŹĘĶ¼”£______________________________
(5) µē»Æѧ·ØŅ²æÉŗĻ³É°±”£ĻĀĶ¼ŹĒÓƵĶĪĀ¹ĢĢåÖŹ×Óµ¼Ģå×÷ĪŖµē½āÖŹ£¬ÓĆPtC3N4×÷Ņõ¼«“߻ƼĮµē½āH2(g)ŗĶN2(g)ŗĻ³ÉNH3µÄŌĄķŹ¾ŅāĶ¼£ŗ
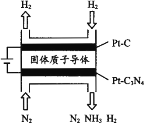
¢ŁPtC3N4µē¼«·“Ó¦²śÉśNH3µÄµē¼«·“Ó¦Ź½________”£
¢ŚŹµŃéŃŠ¾æ±ķĆ÷£¬µ±Ķā¼ÓµēŃ¹³¬¹żŅ»¶ØÖµŅŌŗ󣬷¢ĻÖŅõ¼«²śĪļÖŠ°±ĘųµÄĢå»ż·ÖŹżĖę×ŵēŃ¹µÄŌö“ó¶ų¼õŠ”£¬·ÖĪöĘäæÉÄÜŌŅņ________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»ÖÖ“Ó·ĻĘśīŃĖįļ®µē¼«²ÄĮĻ£Ūŗ¬Li4Ti5O12”¢ĀĮ²”¢Ģ¼·Ū”¢PVDF£Ø¾ŪĘ«¶ž·śŅŅĻ©£©£ŻÖŠ»ŲŹÕijŠ©×ŹŌ“µÄĮ÷³ĢČēĻĀ£ŗ
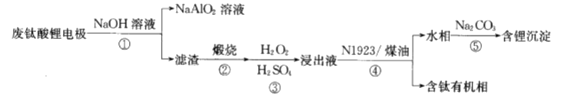
ŅŃÖŖ£ŗLi4Ti5O12+7H2SO4+5H2O2=2Li2SO4+5£ŪTiO£ØH2O2£©£ŻSO4+7H2O£¬ĻĀĮŠŠšŹö“ķĪóµÄŹĒ£Ø£©
A.²½ÖčµÄÄæµÄŹĒ³żČ„Ģ¼·ŪÓėPVDF
B.²½ÖčH2O2µÄ×÷ÓĆŹĒŃõ»Æ¼Į
C.“ÓøƵē¼«²ÄĮĻÖŠæÉ»ŲŹÕµÄ½šŹōŌŖĖŲÓŠAl”¢Ti”¢Li
D.ŗĻĄķ“¦Ąķ·Ļ¾Éµē³Ų£¬ÓŠĄūÓŚ»·¾³±£»¤ŗĶ׏Ō“ŌŁĄūÓĆ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com