
”¾ĢāÄæ”æŗćĪĀĢõ¼žĻĀµÄæÉÄę·“Ó¦£ŗA(s)+2B(g) ![]() 2C(g)+D(g) ”÷H<0£¬ŌŚ¼×ČŻĘ÷³äČė2molA”¢2molB²¢±£³ÖŃ¹Ēæ²»±ä£¬ŅŅČŻĘ÷³äČė2molC”¢ 1mol D²¢±£³ÖĢå»ż²»±ä£¬ĘšŹ¼Ź±¼×”¢ŅŅĮ½ČŻĘ÷ĘųĢåĢå»żĻąµČ”£ĪŖŹ¹Ę½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬ĻĀĮŠ“ėŹ©²»æÉŠŠµÄŹĒ
2C(g)+D(g) ”÷H<0£¬ŌŚ¼×ČŻĘ÷³äČė2molA”¢2molB²¢±£³ÖŃ¹Ēæ²»±ä£¬ŅŅČŻĘ÷³äČė2molC”¢ 1mol D²¢±£³ÖĢå»ż²»±ä£¬ĘšŹ¼Ź±¼×”¢ŅŅĮ½ČŻĘ÷ĘųĢåĢå»żĻąµČ”£ĪŖŹ¹Ę½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬ĻĀĮŠ“ėŹ©²»æÉŠŠµÄŹĒ
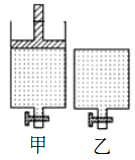
A. ŅŅČŻĘ÷ÖŠ·ÖĄė³öŅ»¶ØĮæµÄDĘųĢå
B. Ļņ¼×¹ČĘ÷ÖŠŌŁ³äČėŅ»¶ØĮæµÄBĘųĢå
C. ½«¼×µÄ»īČūĶłĻĀŃ¹ÖĮ·“Ó¦Ē°µÄĪ»ÖĆ
D. ŹŹµ±½µµĶŅŅČŻĘ÷µÄĪĀ¶Č
”¾“š°ø”æB
”¾½āĪö”æ
ŌŚ¼×ČŻĘ÷³äČė2molA”¢2molB£¬ŅŅČŻĘ÷³äČė2molC”¢ 1mol D£»ÓÉÓŚA³Ź¹ĢĢ¬£¬Čō¼×”¢ŅŅŹĒŗćĪĀŗćČŻČŻĘ÷£¬Ōņ“ļµ½Ę½ŗāŹ±¼×”¢ŅŅÖŠBµÄÅضČĻąµČ£¬¶ų¼×ŹĒŗćĪĀŗćŃ¹ČŻĘ÷£¬Ę½ŗāŹ±µÄĢå»ż“óÓŚĘšŹ¼Ź±µÄĢå»ż£¬¼×Ļąµ±ÓŚŌŚŗćĪĀŗćČŻµÄ»ł“”ÉĻ¼õŠ”Ń¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬Ę½ŗāŹ±¼×ÖŠBµÄÅØ¶ČŠ”ÓŚŅŅ£»ŅŖĻė±£³ÖĘ½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬æÉŅŌ²ÉČ”¼õŠ”ŅŅČŻĘ÷ÄŚDĘųĢåµÄÅØ¶Č£¬ŹŹµ±½µµĶŅŅČŻĘ÷ÄŚµÄĪĀ¶Č£¬Ź¹Ę½ŗāĻņÓŅŅĘ£¬¼õŠ”BµÄÅØ¶Č£»»ņÕß°Ń¼×µÄ»īČūĶłĻĀŃ¹ÖĮ·“Ó¦Ē°µÄĪ»ÖĆ£¬ĖõŠ”Ģå»ż£¬Ōö“ó¼×ČŻĘ÷ÄŚBµÄÅØ¶Č£»¾ŻŅŌÉĻ·ÖĪö½ā“š”£
ŌŚ¼×ČŻĘ÷³äČė2molA”¢2molB£¬ŅŅČŻĘ÷³äČė2molC”¢ 1mol D£»ÓÉÓŚA³Ź¹ĢĢ¬£¬Čō¼×”¢ŅŅŹĒŗćĪĀŗćČŻČŻĘ÷£¬Ōņ“ļµ½Ę½ŗāŹ±¼×”¢ŅŅÖŠBµÄÅضČĻąµČ£¬¶ų¼×ŹĒŗćĪĀŗćŃ¹ČŻĘ÷£¬Ę½ŗāŹ±µÄĢå»ż“óÓŚĘšŹ¼Ź±µÄĢå»ż£¬¼×Ļąµ±ÓŚŌŚŗćĪĀŗćČŻµÄ»ł“”ÉĻ¼õŠ”Ń¹Ēæ£¬Ę½ŗāÕżĻņŅĘ¶Æ£¬Ę½ŗāŹ±¼×ÖŠBµÄÅØ¶ČŠ”ÓŚŅŅ£»
AĻī£¬ŅŖĻė±£³ÖĘ½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬æÉŅŌ“ÓŅŅČŻĘ÷ÖŠ·ÖĄė³öŅ»¶ØĮæµÄDĘųĢ壬¼õŠ”Éś³ÉĪļÅØ¶Č£¬Ę½ŗāÓŅŅĘ£¬æÉŅŌŹ¹Ę½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬AÕżČ·£»
BĻī£¬Õė¶ŌÓŚ¼×ČŻĘ÷£ŗŹōÓŚµČĪĀµČŃ¹£¬ČōĻņ¼×ČŻĘ÷ÖŠŌŁ³äČėŅ»¶ØĮæµÄBĘųĢ壬ÓėŌ¼×ÖŠĘ½ŗāµČŠ§£¬BĘųĢåµÄÅØ¶Č²»±ä£¬²»ÄÜŹ¹Ę½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬B“ķĪó£»
CĻī£¬øł¾ŻÉĻŹö·ÖĪö£¬æÉŅŌ½«¼×µÄ»īČūĶłĻĀŃ¹ÖĮ·“Ó¦Ē°µÄĪ»ÖĆ£¬“ĖŹ±ÓėŅŅĪŖŗćĪĀŗćČŻĻĀµÄµČŠ§Ę½ŗā£¬Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬CÕżČ·£»
DĻī£¬øĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£¬ÓÉÓŚ¼×ÖŠBµÄÅØ¶ČŠ”ÓŚŅŅÖŠBµÄÅØ¶Č£¬ĖłŅŌŹŹµ±½µµĶŅŅČŻĘ÷µÄĪĀ¶Č£¬Ę½ŗāÓŅŅĘ£¬æÉŅŌŹ¹Ę½ŗāŹ±Į½ČŻĘ÷ÖŠBµÄÅضČĻąµČ£¬DÕżČ·£»
×ŪÉĻĖłŹö£¬±¾ĢāŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©½«ĻĀĮŠĻÖĻóÖŠĮņĖį±ķĻÖ³öĄ“µÄŠŌÖŹĢīŠ“ŌŚæÕøńÄŚ£ŗ³ØæŚ·ÅÖƵÄÅØĮņĖį£¬ČÜŅŗÖŹĮæŌö¼Ó_________________£»ÅØĮņĖįÓėÕįĢĒ·Å³ö“óĮæČČ£¬²¢³öĻÖŗŚÉ«¹ĢĢå____________£»
£Ø2£©½«Ņ»Ę涞Ńõ»ÆĮņŗĶŅ»ĘæĮņ»ÆĒāĘųĢåĘææŚ¶Ō½Ó½ųŠŠ»ģŗĻ£¬Ęæ±ŚÉĻÄܹŪ²ģµ½ÓŠ_________________ŗĶ_________________Éś³É£¬Ęä»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ____________________________ £¬ “Ė·“Ó¦ÖŠSO2×÷____________¼Į£¬ 1 mol ¶žŃõ»ÆĮņŗĶĮņ»ÆĒāĶźČ«·“Ó¦Ź±£¬ÓŠ_________molµē×Ó·¢Éś×ŖŅĘ”£
£Ø3£©µ±ÓźĖ®µÄpH________Ź±£¬ĪŅĆĒ³ĘÖ®ĪŖ”°ĖįÓź”±”£Ä³»·±£Š”×é²ā¶Øij“ĪÓźĖ®ÖŠĮņĖįµÄĪļÖŹµÄĮæÅضČĪŖ5”Į10-6 mol/L£¬Õā“ĪÓź__________ĖįÓź£ØŃ”Ģī”°ŹōÓŚ”±»ņ”°²»ŹōÓŚ”±£©”£³£ĪĀĻĀČō°Ń0.1mol/LµÄŃĪĖįČÜŅŗĻ”ŹĶ100±¶£¬“ĖŹ±µÄČÜŅŗµÄpH=__________”£
£Ø4£©½«Ņ»³äĀś°±ĘųµÄ“óŹŌ¹Üµ¹Į¢ŌŚĖ®²ŪÖŠ£¬æÉŅŌ擵½ĻÖĻó_________________£¬ĖµĆ÷_______________£¬ČōŌŚ“ĖČÜŅŗÖŠµĪČė·ÓĢŖŹŌŅŗ£¬ČÜŅŗ³Ź_______É«£¬ĘäµēĄė·½³ĢŹ½___________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¢ń£®ĻĀĮŠø÷×éĮ£×Ó£¬ŹōÓŚĶ¬ÖÖŗĖĖŲµÄŹĒ___________(Ģī±ąŗÅ£¬ĻĀĶ¬)£¬»„ĪŖĶ¬Ī»ĖŲµÄŹĒ___________£¬»„ĪŖĶ¬ĖŲŅģŠĪĢåµÄŹĒ___________£¬»„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄŹĒ___________£¬ŹōÓŚĶ¬ÖÖĪļÖŹµÄŹĒ_____________£¬»„ĪŖĶ¬ĻµĪļµÄŹĒ__________”£
¢Ł16O2ŗĶ18O3 ¢Ś CH4 ŗĶC3H8 ¢Ū H”¢D”¢T¢Ü 3015RŗĶ £ØŗĖÄŚ15øöÖŠ×Ó£©¢ŻCH3CH2OHŗĶCH3OCH3¢Ž
£ØŗĖÄŚ15øöÖŠ×Ó£©¢ŻCH3CH2OHŗĶCH3OCH3¢Ž ŗĶ
ŗĶ
¢ņ£®ÄÜŌ“ŹĒĻÖ“śÉē»į·¢Õ¹µÄÖ§ÖłÖ®Ņ»”£
¢Å»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ£¬Ö÷ŅŖ±ķĻÖĪŖČČĮæµÄ±ä»Æ”£
¢ŁĻĀĮŠ·“Ó¦ÖŠ£¬ŹōÓŚ·ÅČČ·“Ó¦µÄŹĒ_________(Ģī×ÖÄø)”£
A£®Ba(OH)2”¤8H2OÓėNH4Cl»ģŗĻ½Į°č B£®øßĪĀģŃÉÕŹÆ»ŅŹÆ
C£®ĀĮÓėŃĪĖį·“Ó¦ D£®C+H2O(g)=CO+ H2
¢Ś²šæŖ1mol H©H¼ü£¬1mol N©H¼ü£¬1mol N”ŌN¼ü·Ö±šŠčŅŖĪüŹÕµÄÄÜĮæ
ĪŖa kJ£¬b kJ£¬c kJ£¬Ōņ1molN2ŗĶH2ĶźČ«·“Ӧɜ³É2mol NH3ŠčŅŖ·Å³öµÄČČĮæĪŖ____________kJ”£
¢ĘµēÄÜŹĒĻÖ“śÉē»įÓ¦ÓĆ×ī¹ć·ŗµÄÄÜŌ“Ö®Ņ»”£

ČēĻĀĶ¼ĖłŹ¾µÄŌµē³Ų×°ÖĆÖŠ£¬øŗ¼«ŹĒ_______£¬Õż¼«ÉĻÄܹ»¹Ū²ģµ½µÄĻÖĻóŹĒ_______________________£¬Õż¼«µÄµē¼«·“Ó¦Ź½ŹĒ_____________________”£Ōµē³Ų¹¤×÷Ņ»¶ĪŹ±¼äŗó£¬ČōĻūŗÄŠæ6.5 g£¬Ōņ·Å³öĘųĢå________g”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŠšŹö“ķĪóµÄŹĒ( )
A.¾§Ģå¹čæÉÖĘ×÷Ģ«ŃōÄܵē³ŲµÄŠ¾Ę¬B.Ļ”ĻõĖįæÉŅŌÓĆĀĮ²ŪĄ“ŌĖŹä
C.Ńõ»ÆĢśæÉÓĆĄ“ÖĘ×÷ŗģÉ«ÓĶĘįŗĶĶæĮĻD.ÓĆĆ¾ĀĮŗĻ½šæÉ×÷·É»śÖĘŌģ²ÄĮĻ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆŅ»Ö§ŹŌ¹Ü·Ö±š×ö¼×Ķ锢ŃõĘų»ģŗĻµćČ¼ŹµŃ飬ŹµŃéÖŠĻģÉł×ī“óµÄŹĒĻĀĆęÄÄŅ»ÖÖĢå»ż±ČµÄ»ģŗĻĪļ
A.1:1B.1:2C.1:3D.3:1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£Źż£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A. ³£ĪĀ³£Ń¹ĻĀ£¬1.8g¼×»ł(”ŖCD3)ÖŠŗ¬ÓŠµÄÖŠ×ÓŹżĪŖNA
B. ±ź×¼×“æöĻĀ£¬11.2LŅŅĻ©ŗĶ»·±ūĶé(C3H6)µÄ»ģŗĻĘųĢåÖŠ£¬¹²ÓƵē×Ó¶ŌµÄŹżÄæĪŖ3NA
C. 2.8g µÄ¾ŪŅŅĻ©ÖŠŗ¬ÓŠµÄĢ¼Ō×ÓŹżĪŖ0.2 NA
D. 1mol ±½ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼üµÄŹżÄæĪŖ3 NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“óĘų”¢Ė®ĢåĪŪČ¾µÄÖĪĄķŹĒ»Æѧ¹¤×÷ÕßŃŠ¾æµÄÖŲŅŖæĪĢā£¬Č¼ĆŗµÄŃĢµĄĘųŗĶĘū³µĪ²ĘųŹĒŌģ³ÉĪķö²ĢģĘųĪŪČ¾µÄŌŅņÖ®Ņ»”£
(1)ÓĆCH4“߻ƻ¹ŌµŖŃõ»ÆĪļ£¬ŅŃÖŖCH4(g)+2O2(g)=CO2(g)+2H2O(l) ”÷H1= a kJ/mol£¬Óū¼ĘĖć·“Ó¦CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(1)µÄģŹ±ä”÷H2£¬Ōņ»¹ŠčŅŖ²éÕŅij»ÆŗĻ·“Ó¦µÄģŹ±ä”÷H3£¬øĆ»ÆŗĻ·“Ó¦ÖŠø÷ĪļÖŹ»Æѧ¼ĘĮæŹżÖ®±ČĪŖ×ī¼ņÕūŹż±ČŹ±”÷H3=bkJ/mol£¬ŌņøĆ»ÆŗĻ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ____________________”£¾Ż“Ė¼ĘĖć³ö”÷H2=__________kJ/mol(ÓĆŗ¬aŗĶbµÄŹ½×Ó±ķŹ¾)”£
(2)Ęū³µĪ²Ęų×Ŗ»ÆµÄ·“Ó¦Ö®Ņ»£ŗ2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ”÷H=£746.5kJ/mol”£ŌŚÄ³ĪĀ¶ČŹ±£¬æÉ°“ĻĀĮŠĮ÷³ĢĢ½¾æijÖ֓߻ƼĮ×÷ÓĆĻĀµÄ·“Ó¦ĖŁĀŹ£¬ÓĆĘųĢå“«øŠĘ÷²āµĆ²»Ķ¬Ź±¼äµÄNOŗĶCOÅضČČēĻĀ±ķ£ŗ
N2(g)+2CO2(g) ”÷H=£746.5kJ/mol”£ŌŚÄ³ĪĀ¶ČŹ±£¬æÉ°“ĻĀĮŠĮ÷³ĢĢ½¾æijÖ֓߻ƼĮ×÷ÓĆĻĀµÄ·“Ó¦ĖŁĀŹ£¬ÓĆĘųĢå“«øŠĘ÷²āµĆ²»Ķ¬Ź±¼äµÄNOŗĶCOÅضČČēĻĀ±ķ£ŗ

Ēė»Ų“šĻĀĮŠĪŹĢā(¾ł²»æ¼ĀĒĪĀ¶Č±ä»Æ¶Ō“߻ƼĮ“߻Ɗ§ĀŹµÄÓ°Ļģ)£ŗ
¢ŁĒ°2sÄŚµÄĘ½¾ł·“Ó¦ĖŁĀŹ¦Ō(N2)=______________________________”£
¢ŚŌŚøĆĪĀ¶ČĻĀ£¬·“Ó¦µÄĘ½ŗā³£ŹżK=___________(Ö»Š“³ö¼ĘĖć½į¹ū)”£
¢Ū¶ŌÓŚøĆæÉÄę·“Ó¦£¬Ķعż×ŪŗĻ·ÖĪöŅŌÉĻŠÅĻ¢£¬ÖĮÉŁæÉŅŌĖµĆ÷___________(Ģī×ÖÄø)”£
A.øĆ·“Ó¦µÄ·“Ó¦Īļ»ģŗĻŗóŗܲ»ĪȶØ
B.ŌŚ“߻ƼĮµÄ×÷ÓĆĻĀ£¬øĆ·“Ó¦Ņ»µ©·¢Éś½«ŌŚ½Ļ¶ĢµÄŹ±¼äÄŚĶź³É
C.øĆ·“Ó¦ĢåĻµ“ļµ½Ę½ŗāŹ±ÖĮÉŁÓŠŅ»ÖÖ·“Ó¦ĪļµÄ°Ł·Öŗ¬Įæ½ĻŠ”
D.øĆ·“Ó¦ŌŚŅ»¶ØĢõ¼žĻĀÄÜ×Ō·¢½ųŠŠ
E.øĆ·“Ó¦Ź¹ÓĆ“ß»Æ¼ĮŅāŅå²»“ó
(3)Ķعżµ÷½ŚČÜŅŗpH£¬ŌŚČõ¼īŠŌĢõ¼žĻĀ£¬ÓĆĘÆ°×·ŪČÜŅŗæɽ«·ĻĖ®ÖŠµÄCN£×Ŗ»ÆĪŖĢ¼ĖįŃĪŗĶN2¶ų³żČ„”£Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________”£
(4)·ĻĖ®ÖŠµÄÖŲ½šŹōĄė×ÓĶس£ÓĆ³Įµķ·Ø³żČ„”£ŅŃÖŖKsp(NiS)=1.1”Į10£21£¬Ksp(CuS)=1.3”Į10£36£¬¹ś¼Ņ¹ę¶ØµÄÅŷűź»“£ŗÄųµĶÓŚ1.1”Į10£5mol”¤L£1£¬ĶµĶÓŚ7.8”Į10£5mol”¤L£l”£ŌņŠčŅŖæŲÖĘČÜŅŗÖŠS2£µÄÅØ¶Č²»µĶÓŚ__mol”¤L£1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ±ä»ÆÖŠ£¬±ŲŠė¼ÓČėŃõ»Æ¼Į²ÅÄÜ·¢ÉśµÄŹĒ
A. SO2”śS B. SO32”Ŗ”śSO2 C. I”Ŗ”śI2 D. HCO3”Ŗ”śCO32”Ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗ2CrO42£+2H+![]() Cr2O72£+H2O”£25”ꏱ£¬µ÷½Ś³õŹ¼ÅضČĪŖ1.0 molL£1 µÄNa2CrO4ČÜŅŗµÄpH£¬²ā¶ØĘ½ŗāŹ±ČÜŅŗÖŠc(Cr2O72£)ŗĶc(H+)£¬»ńµĆČēĶ¼ĖłŹ¾µÄĒśĻß”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
Cr2O72£+H2O”£25”ꏱ£¬µ÷½Ś³õŹ¼ÅضČĪŖ1.0 molL£1 µÄNa2CrO4ČÜŅŗµÄpH£¬²ā¶ØĘ½ŗāŹ±ČÜŅŗÖŠc(Cr2O72£)ŗĶc(H+)£¬»ńµĆČēĶ¼ĖłŹ¾µÄĒśĻß”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A. Ę½ŗāŹ±£¬pHŌ½Š”£¬c(Cr2O72£)Ō½Š”
B. AµćCrO42£×Ŗ»ÆĪŖCr2O72£·“Ó¦µÄĘ½ŗā³£ŹżµÄŹżĮ漶ĪŖ1014
C. CµćCrO42£µÄĘ½ŗā×Ŗ»ÆĀŹĪŖ40%
D. Ę½ŗāŹ±£¬ČōČÜŅŗÖŠc(Cr2O72£)=c(CrO42£)£¬Ōņc(H+)£¾2.0”Į10-7 molL£1
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com