
分析 (1)氯化铜与铁反应生成氯化亚铁和铜,过滤可以除去铜;
(2)碳酸钠溶液与二氧化碳反应生成碳酸氢钠;
(3)铝与氢氧化钠反应生成可溶性偏铝酸钠溶液,过滤得到铁.
解答 解:(1)氯化铜与铁反应生成氯化亚铁和铜,过滤可以除去铜,离子方程式为Fe+Cu2+=Fe2++Cu,
故答案为:Fe粉;Fe+Cu2+=Fe2++Cu;
(2)碳酸钠溶液与二氧化碳反应生成碳酸氢钠,所以通入过量二氧化碳可以除去碳酸氢钠中的碳酸钠,离子方程式为CO32-+H2O+CO2=2HCO3-;
故答案为:CO2;CO32-+H2O+CO2=2HCO3-;
(3)铝与氢氧化钠反应生成可溶性偏铝酸钠溶液,过滤得到铁,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:NaOH;2Al+2OH-+2H2O=2AlO2-+3H2↑.
点评 本题考查了物质的提纯,明确物质除杂的原则及离子方程式书写方法是解题关键,题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
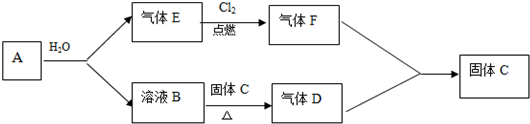
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HF能用于刻蚀玻璃,制作玻璃量筒刻度 | |
| B. | SiO2是制光导纤维的主要原料 | |
| C. | 硅酸可由SiO2直接制得 | |
| D. | SiO2是酸性氧化物,一定条件下可与碱性氧化物或碱反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
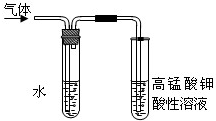 实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:
实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
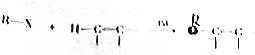
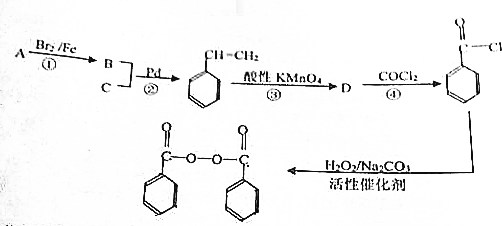
 ,物质D中含有的官能团的名称为羧基.
,物质D中含有的官能团的名称为羧基. ;
;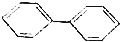 );
);查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含磷洗涤剂中的Na5P3O10中磷的化合价为+7价 | |
| B. | 有多少种元素就一定有多少种单质 | |
| C. | 金刚石、石墨和C60全部以游离态存在 | |
| D. | 含多种元素的物质一定是混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com