
一定条件下,对于可逆反应X(g)+3Y(g)  2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol·
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol· L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是
L-1、0.3 mol·L-1、0.08 mol·L-1,则下列判断正确的是
A.c1∶c2=3∶1 
B.平衡时,Y和Z的生成速率之比为2∶3
C.X、Y的转化率不相等
D.c1的取值范围为0 mol·L-1<c1<0.14 mol·L-1
科目:高中化学 来源:2015-2016学年湖南省高二上第二次月考化学试卷(解析版) 题型:选择题
一些科学家采用高质子导电性的SCY陶瓷(能传递H+),实现了氨的电化学合成。该过程N2和H2的转化率远高于现在工业上使用的氨合成法。对于电化学合成氨的有关叙述正确的是
A.N2在阴极上被氧化
B.可选用铁作为阳极材料
C.阳极的电极反应式是N2+6e-+6H+ = 2NH3
D.该过程的总反应式是N2+3H2 2NH3
2NH3
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省盐城市高二上学期期中考试化学试卷(解析版) 题型:选择题
我国政府规定在2006年7月1日后含有铜、铬、镉、汞、多溴联苯等材料的电子产品禁止投放市场。下列有关电子垃圾的说法中不正确的是
A.将电子垃圾在火上焚烧,熔下其中的金属再回收利用
B.电子垃圾应在无污染的条件下回收,使之成为有用的资源
C.电子垃圾的任意抛弃会严重污染地下水源
D.各国的电子垃圾应在本国境内处理,严禁向其他国家输出
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第二次月考化学试卷(解析版) 题型:选择题
完全燃烧CO和H2的混合气体共50mL,需要同温同压下的氧气
A.20mL B.25mL C.50mL D.无法计算
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南宁远一中、祁阳一中高二上第二次联考化学试卷(解析版) 题型:填空题
铁是当代社会中用量最大的金属之一。磁铁矿是工业上冶炼铁的原料之一,发生的主要反应为:Fe3O4(s)+4CO 3Fe(s)+4CO2
3Fe(s)+4CO2
(1)已知:①Fe3O4(s)+4C(石墨) 3Fe(s)+4CO(g) ΔH=+646.0 kJ/mol
3Fe(s)+4CO(g) ΔH=+646.0 kJ/mol
②C(石墨)+CO2(g) 2CO(g) ΔH=+172.5 kJ/mol
2CO(g) ΔH=+172.5 kJ/mol
由Fe3O4(s)与CO反应生成Fe(s)的热化学方程式是 。
(2)T℃时,在 2L恒容密闭容器中,加入Fe3O4、CO各1.0 mol ,10 min反应达到平衡时,容器中CO2的浓度是0.4 mol /L。
①能证明该反应达到化学平衡的是 (选填字母)。
a.容器内压强不再变化
b.容器内CO、CO2物质的量比为1 : 1
c.容器内气体的质量不再变化
d.生成CO2的速率与消耗CO的速率相等
②CO的平衡转化率是 。
③l0 min内,反应的平均反应速率v (CO2)= 。
④欲提高该反应中CO的平衡转化率,可采取的措施是 (选填字母)。
a.提高反应温度 b.移出部分CO2
c.加入合适的催化剂 d.减小容器的容积
⑤T℃时,该反应的平衡常数K= 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南宁远一中、祁阳一中高二上第二次联考化学试卷(解析版) 题型:选择题
已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6KJ/mol。有关键能数据如下表:
化学键 | H—H | O=O |
键能/KJ?mol-1 | 436 | 498 |
则水分子中O—H键键能 为
为
A.463.4KJ/mol B.926.8KJ/mol
C.221.6KJ/mol D.413KJ/mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:计算题
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是 。
(2)将2.4mol某金属投入某酸溶液中,恰好完全反应,并产生7.2g氢气,则此金属化合价为 。
(3)某同学为探究铜铁合金中铁的质量分数,先后进行了三次实验,实验数据如下:
实验次数 项目 | 第一次 | 第二次 | 第三次 |
所取合金的质量/g | 20 | 20 | 40 |
所加稀硫酸的质量/g | 100 | 120 | 80 |
生成氢气的质量/g | 0.4 | 0.4 | 0.4 |
①该合金中铁的质量分数是 %(结果精确到1%)。
②本实验中所加稀硫酸的溶质的质量分数为 %(结果精确到0.1%)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省枣阳市高一上学期期中考试化学试卷(解析版) 题型:选择题
下列各物质的物质的量不能肯定是1 mol的是
A.23 g金属钠所含的钠原子数
B.标准状况下,17 g氨气
C.22.4 L CO2气体
D.标准状况下10 L氧气和12.4 L氮气的混合物
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三上半期考试理综化学试卷(解析版) 题型:填空题
CO是水煤气的主要成份之一,是一种无色剧毒气体,根据信息完成下列各题
Ⅰ、已知下列热化学方程式
2C(s) + O2(g) = 2CO(g) △H = -221kJ/mol
C(s) + O2(g) = CO2(g) △H = -393kJ/mol
24g单质碳在不足量的O2中燃烧时,生成等物质的量的CO和CO2气体,则和24g单质碳完全燃烧生成CO2相比较,损失热量_________kJ
Ⅱ、850℃时,在10L体积不变的容器中投入2molCO和3molH2O,发生如下反应:
CO(g) + H2O(g)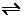 CO2(g) + H2(g),当CO的转化率达60%时,反应达平衡
CO2(g) + H2(g),当CO的转化率达60%时,反应达平衡
(1)850℃时,该反应的平衡常数为_________
(2)该条件下,将CO和H2O都改为投入2mol,达平衡时,H2的浓度为_________mol/L,下列情况能说明该反应一定达平衡的是_________
A.V正(CO) = V逆(CO2)
B.气体的密度不再随时间改变
C.CO的体积分数不再随时间改变
D.气体的平均摩尔质量不再随时间改变
Ⅲ、为防止CO使人中毒,一种CO分析仪的工作原理如图所示,该装置中电解质为氧化钇——氧化钠,其中O2-可以在固体ZASICON中自由移动,则:

(1)该原电池中通入CO的电极为_________极,该电极的电极反应式为___________________
(2)通空气一极的电极反应式为____________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com