
【题目】下列实验操作不能达到相应实验目的的是
选项 | 实验操作 | 实验目的 |
A | 向苯与液溴的混合液中加入铁粉,将产生的气体直接通入AgNO3溶液中 | 验证液溴与苯发生取代反应 |
B | 向5mL浓度为0.5mol·L-1的KI溶液中滴加少量氯化铁溶液,再加入少量淀粉溶液,振荡 | 比较I-、Fe2+的还原性强弱 |
C | 向5mL浓度为0.2mol·L-1的MgCl2溶液中滴加少量NaOH溶液,待有白色沉淀生成后,再滴加0.2mol·L-1的CuCl2溶液 | 比较Cu(OH)2、Mg(OH)2溶度积的大小 |
D | 向 | 验证与H+的结合能力: |
A.AB.BC.CD.D
【答案】A
【解析】
A. 液溴易挥发,向苯与液溴的混合液中加入铁粉发生反应过程中,除了产生HBr以外,还有挥发的溴蒸气,若将混合气体直接通入AgNO3溶液中,会观察到有淡黄色沉淀生成,但不能说明液溴与苯发生的是取代反应,溴蒸气会干扰实验的检验,符合题意,故A选;
B. 向5mL浓度为0.5mol·L-1的KI溶液中滴加少量氯化铁溶液,会发生化学反应:2Fe3++2I-![]() 2Fe2++I2,再加入少量淀粉溶液,振荡后溶液变蓝,则可证明还原性:I->Fe2+,能达到实验目的,不符合题意,故B不选;
2Fe2++I2,再加入少量淀粉溶液,振荡后溶液变蓝,则可证明还原性:I->Fe2+,能达到实验目的,不符合题意,故B不选;
C. 向5mL浓度为0.2mol·L-1的MgCl2溶液中滴加少量NaOH溶液,生成Mg(OH)2白色沉淀,再滴加0.2mol·L-1的CuCl2溶液,白色沉淀变成蓝色沉淀,实现了沉淀的转化,又Cu(OH)2、Mg(OH)2属于同一类型,则可通过实验比较Cu(OH)2、Mg(OH)2溶度积的大小,不符合题意,故C不选;
D. 向![]() 乳浊液中加入足量的Na2CO3溶液,会发生反应:
乳浊液中加入足量的Na2CO3溶液,会发生反应:![]() +CO32-=HCO3- +
+CO32-=HCO3- +![]() ,乳浊液变澄清,可证明与H+的结合能力:
,乳浊液变澄清,可证明与H+的结合能力:![]() >
>![]() ,不符合题意,故D不选;
,不符合题意,故D不选;
答案选A。


科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是
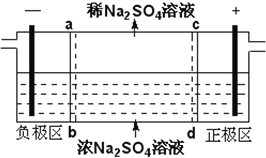
A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O–4e–=O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程中的能量变化如图所示(图中 E1 表示无催化剂时正反应的活化能,E2 表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
2SO3(g)反应过程中的能量变化如图所示(图中 E1 表示无催化剂时正反应的活化能,E2 表示无催化剂时逆反应的活化能)。下列有关叙述不正确的是
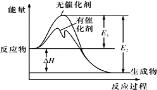
A.该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数
B.该反应中,反应物的总键能大于生成物的总键能
C.500℃、101kPa 下,将 1molSO2(g)和 0.5molO2(g)置于密闭容器中充分反应生成 SO3(g)放热 akJ,其热化学方程式为 2SO2(g) + O2(g)![]() 2SO3(g) ΔH<-2a kJ·mol-l
2SO3(g) ΔH<-2a kJ·mol-l
D.ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞是我国自主研发的一类用于治疗急性缺血性脑卒的新药。合成丁苯酞(J)的一种路线如下:
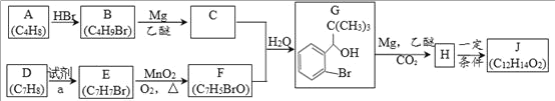
已知:R-Br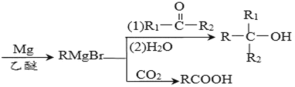
(1) A 的名称是_____,A分子中最多有_____个原子共平面。
(2) B 生成 A 的化学方程式_____。
(3) D 生成 E 的反应类型为_____
(4) F 的结构简式_____。
(5) J是一种酯,分子中除苯环外还含有一个五元环。写出 H 生成 J 的化学方程式_____(注明反应条件)。
(6)E![]()
![]() X,X 的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有_____种,写出其中核磁共振氢谱有五组吸收峰的结构简式_____。
X,X 的同分异构体中:①能发生银镜反应;②能与氯化铁溶液发生显色反应。满足上述条件的X的同分异构体共有_____种,写出其中核磁共振氢谱有五组吸收峰的结构简式_____。
(7)利用题中信息和所学知识,写出以甲烷和化合物 D 为原料,合成![]() 的路线流程图_____(其它试剂自选)
的路线流程图_____(其它试剂自选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用含多糖淀粉的物质可以生产醋酸。下面是生产醋酸的流程,根据流程回答下列问题:
![]()
![]()
![]() ―→
―→![]() ―→
―→![]() ―→
―→![]()
B是日常生活中常见的有特殊香味的有机物,在有些饮料中含有B。
(1)写出淀粉的分子式___,C中官能团的名称是__。
(2)B→C的反应类型是___(填字母)。
A.取代反应 B.加成反应 C.氧化反应 D.还原反应
(3)写出C完全燃烧的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示:
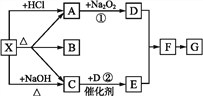
图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,请填写下列空白:
(1)物质X可以是______,C是_________, F是______。
(2)反应①的化学方程式是_________,反应②的化学方程式是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸(H2C2O4)为二元弱酸,25℃时,Ka1(H2C2O4)=5.9×10-2,Ka2(H2C2O4)=6.4×10-5。用NaOH溶液滴定草酸氢钾(KHC2O4)溶液,混合溶液的相对导电能力随加入NaOH体积的变化如图所示(忽略混合时溶液温度的变化),其中N点为反应终点。下列有关描述中正确的是
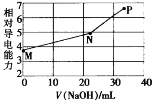
A.M点粒子浓度:c(K+)>c(![]() )>c(
)>c(![]() )>c(H2C2O4)
)>c(H2C2O4)
B.N点时存在:c(Na+)+c(K+)<2c(![]() )+2c(
)+2c(![]() )
)
C.从N点到P点的过程中溶液中一定存在:c(Na+)+c(H2C2O4)>c(![]() )
)
D.水的电离程度大小顺序:P>N>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、M、N六种主族元素,它们在周期表中位置如图所示,下列说法正确的是( )
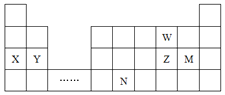
A.原子半径:![]() 简单离子半径:
简单离子半径:![]()
B.单质的还原性:![]() 简单氢化物的沸点:
简单氢化物的沸点:![]()
C.溴与元素M同主族,最高价氧化物的水化物的酸性比M的强
D.元素N位于金属与非金属的分界线附近,可以推断N的单质可作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氯气,将多余的氯气用100 mL 1.7mol/L的NaOH溶液完全吸收。对吸收后的溶液进行分析化验,测知c(OH-)=0.1mol/L (不考虑反应前后溶液的体积变化) 。ClO-和ClO3-的物质的量浓度之比为5∶1。请回答:
(1)吸收氯气消耗的NaOH的物质的量为_______________mol。
(2)被氧化的氯气的物质的量为_______________mol,被还原的氯气的物质的量为 _______________mol。
(3)若采用二氧化锰和浓盐酸共热的方法制氯气,制备尾气中的氯气所消耗的二氧化锰的质量为_______________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com