
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g) CH3OH(g)+H2O(g)达到平衡状态的是______
CH3OH(g)+H2O(g)达到平衡状态的是______ CH3OH(g)+H2O(g)进行过程中能量的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是______.
CH3OH(g)+H2O(g)进行过程中能量的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是______.



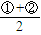 可得CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g),
可得CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g),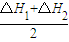 =-867 kJ/mol,
=-867 kJ/mol, CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)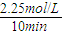 =0.225mol?L-1?min-1,故B错误;
=0.225mol?L-1?min-1,故B错误;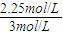 ×100%=75%,故C正确;
×100%=75%,故C正确;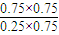 =3,故D错误;
=3,故D错误; NH3?H2O+H+,
NH3?H2O+H+, NH3?H2O+H+;小于.
NH3?H2O+H+;小于.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
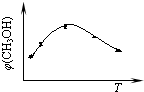
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)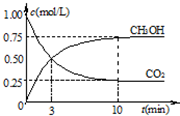 随时间变化如图所示.下列说法正确的是
随时间变化如图所示.下列说法正确的是 CH3OH(g)+H2O(g)达到平衡状态的是
CH3OH(g)+H2O(g)达到平衡状态的是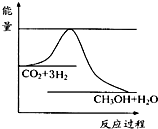
 CH3OH(g)+H2O(g)进行过程中能量(单位为kJ?mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是
CH3OH(g)+H2O(g)进行过程中能量(单位为kJ?mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,达到平衡后,采取下列措施中能使c(CH3OH)增大的是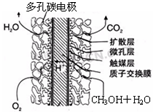
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
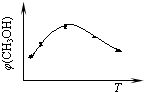

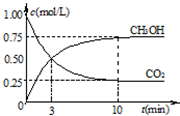

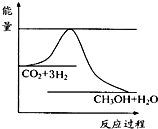

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com