
下列说法正确的是 ( )
A. 乙烯和乙烷都能发生加聚反应
乙烯和乙烷都能发生加聚反应
B.蛋白质水解的最终产物是多肽
C.米酒变酸的过程涉及了氧化反应
D.石油裂解和油脂皂化都有高分子生成小分子的过程
 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
常温下,0.1mol·L-1CH3COONa溶液中,微粒浓度间关系正确的是
A.c(Na+)=c(CH3COO-) >c(OH-)=c(H+)
B.c(OH-)=c(H+)+ c(CH3COOH)
C.c(Na+) + c(H+)= c(CH3COO-) +c(OH-)
D.c(CH3COOH) + c(CH3COO-) = c(Na+)+ c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.煤是复杂的混合物,含有苯、甲苯、二甲苯等一系列重要的化工原料
B.石油分馏得到的汽油、煤油、柴油等都有固定的熔沸点
C.石油炼制的目的是为了获得轻质油和重要化工原料(乙烯、丙烯等)
D.天然气和沼气的主要成分是乙烯,它们都属于不可再生能源
查看答案和解析>>
科目:高中化学 来源: 题型:
现有6种短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| W | 周期表中原子半径最小的元素 |
| U | 地壳中含量最多的金属元素 |
| R | 单质占空气体积的1/5 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
完成下列空白(涉及W、U、R、T、X、Y、Z代表的元素时,用相应的元素符号表示):
⑴.元素T的原子核外共有________个电子;元素X的一种核素其中子数比质子数多2,这种核素的符号是__________。
⑵.用离子方程式表示:
①.元素Y与元素W形成的离子YW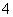 与NaOH溶液共热
与NaOH溶液共热
。
②.元素U的单质与NaOH溶液反应:_______________________________________。
⑶.元素Z与元素T相比,非金属性较强的是________,下列表述中能证明这一事实的是________(填字母)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
⑷.探寻物质的性质差异是学习的重要方法之一。在T、X、Y、Z四种元素的最高价氧化物的水化物中,化学性质明显不同于其他三种的是________(用分子式表示),理由是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是( )
A.A和B最简式一定相同 B.A和B不可能是同系物
C.A和B一定是同分异构体 D.A和B的化学性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
由乙醛和乙酸乙酯组成的混合物中,若含碳的质量分数为A%,则此混合物中含氢的质量分数为 ( )
A.6A% B.A/6% C.10A% D.(100-7A/6)%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述的乙炔的结构和性质中,既不同于乙烯,也不同于乙烷的是
A.存在不饱和键
B.不易发生取代反应,易发生加成反应
C.分子中的所有原子都处在同一条直线上
D.能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
根据已学知识,请你回答下列问题:
(1)含有8个质子,10个中子的原子的化学符号__________。
(2)最外层电子排布为4s24p1的原子的核电荷数为__________。
(3)某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是_________。
(4)根据VSEPR模型,H3O+的分子立体结构为: ,SO2的立体结构为: 。
(5)周期表中最活泼的非金属元素原子的轨道表示式为__________ 。
( 6 ) 三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为________。
( 7 ) 某元素核外有三个电子层,最外层电子数是核外电子总数的1/6,写出该元素原子的电子排布式是__________。
( 8 )写出铬元素在周期表中的位置__________,它位于__________区。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com