
| A. | 次氟酸的结构式为H-F-O | B. | CH4分子的球棍模型: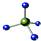 | ||
| C. | 1H、3H2、D互为同位素 | D. | CO2电子式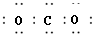 |
分析 A.次氟酸的中心原子为O,分子中不存在H-F键;
B.甲烷分子中含有4个碳氢键,为正四面体结构;
C.同位素的研究对象为原子,不是分子;
D.二氧化碳分子中含有两个碳氧双键,不是碳氧单键.
解答 解:A.次氟酸中存在1个H-O键和1个O-F键,其正确的结构式为:H-O-F,故A错误;
B.甲烷为正四面体结构,CH4分子的球棍模型为: ,故B正确;
,故B正确;
C.1H、D互为同位素,3H2不是,同位素研究的对象是原子,故C错误;
D.CO2是共价化合物,其结构式为O=C=O,碳原子和氧原子之间有2对电子,其电子式为 ,故D错误;
,故D错误;
故选B.
点评 本题考查了常见化学用语的表示方法,题目难度不大,涉及电子式、球棍模型、结构式、同位素等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
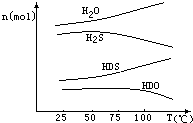 我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg•L-1.其工业提取法有:
我国有较长的海岸线,浩瀚的海洋是一个巨大的物质资源和能量的宝库.目前,世界各国都在研究如何充分利用海洋资源.全球海水中的溴的储量丰富,约占地球溴总储量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg•L-1.其工业提取法有:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3-CH2OH | B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | ||
| C. | CH4$\stackrel{高温}{→}$C+2H2 | D. | CH≡CH+HCl$→_{△}^{催化剂}$CH2═CHCl |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石不如石墨稳定 | |
| C. | 等质量的石墨与金刚石完全燃烧,金刚石放出的能量少 | |
| D. | 等质量的石墨与金刚石完全燃烧,二者放出的热量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
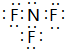 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$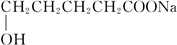 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.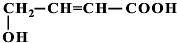 、
、 、
、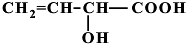 (提示:羟基不能连在碳碳双键上).
(提示:羟基不能连在碳碳双键上).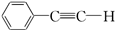 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com