
| A. | 分液、蒸馏 | B. | 萃取、蒸馏 | C. | 分液、萃取 | D. | 蒸馏、萃取 |
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | a |
| c(CO2) | 3 | 1 | 0.8 | 1 |
| c(H2) | 2 | 1 | 0.8 | 1 |
| c(CO) | 1 | 2 | 3 | 0.5 |
| c(H2O) | 2 | 2 | 3 | 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠(碳酸氢钠):加热,直到质量不再减少为止 | |
| B. | 溴苯(溴):加入氢氧化钠溶液洗涤,分液 | |
| C. | 乙醇(乙醛):加入新制氢氧化铜煮沸,过滤 | |
| D. | 乙酸丁酯(乙酸):加入碳酸钠溶液洗涤,分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2是氧化剂,CO2是还原剂 | |
| B. | Na2CO3是还原产物,O2是氧化产物 | |
| C. | 每转移4摩尔电子,有1摩尔氧气生成 | |
| D. | 1摩尔CO2参加反应就会产生11.2LO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
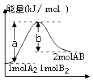
| A. | 该反应是放热反应 | |
| B. | 加入催化剂,(b-a)的差值减小 | |
| C. | 每生成2molAB分子吸收bkJ热量 | |
| D. | 若反应生成AB为液态,吸收的热量小于(a-b)kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
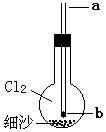 如图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠.从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾.不正确的说法是( )
如图烧瓶内充满氯气,底部有层细沙(不参与反应),b处塞有小块钠.从a口用细铁丝把钠送下去,再从a口滴下一滴水,恰好滴在钠块上,立即剧烈反应,烧瓶内产生大量白色烟雾.不正确的说法是( )| A. | 水可能参与二个氧化还原反应 | |
| B. | Cl2可能参与四个氧化还原反应 | |
| C. | 氧元素参与的反应一定是氧化还原反应 | |
| D. | 氢元素参与的反应包含被氧化与被还原过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
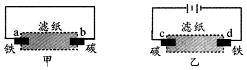
| A. | 甲是原电池,乙是电解池 | |
| B. | 甲中铁棒比乙中铁棒更易腐蚀 | |
| C. | d电极上的电极反应是:Fe-2e→Fe2+ | |
| D. | b电极上的电极反应是:O2+2H2O+4e→4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 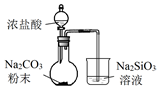 验证H2CO3酸性强于H2SiO3 | B. | 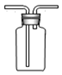 收集CO2或NH3 | ||
| C. | 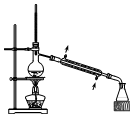 分离Na2CO3溶液与CH3COOC2H5 | D. | 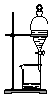 分离CH3CH2OH与CH3COOC2H5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com