
分类是化学学习和研究中的常有用手段,下列分类依据和结论都正确的是()
A. 浓HCl、浓H2SO4、浓HNO3均具有氧化性,都属氧化性酸
B. Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质
C. NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物
D. 金刚石、二氧化硅、碳化硅晶体中的原子均能共价键结合,都属原子晶体
考点: 酸、碱、盐、氧化物的概念及其相互联系;电解质与非电解质.
专题: 物质的分类专题.
分析: A.浓HCl没有强氧化性,不是氧化性酸;
B.SO2是非电解质;
C.HNO3是共价化合物在熔融状态不导电;
D.原子晶体中原子间都是以共价键结合的.
解答: 解:A.浓HCl没有强氧化性,不是氧化性酸,浓H2SO4、浓HNO3均具有氧化性,属氧化性酸,故A错误;
B.SO2是非电解质,在水中与水反应生成亚硫酸,亚硫酸是电解质,故B错误;
C.HNO3是共价化合物在熔融状态不导电,NaOH、NaNO3在水溶液中和熔融状态都能电离出离子,属离子化合物,故C错误;
D.原子晶体中原子间都是以共价键结合的,金刚石、二氧化硅、碳化硅晶体中的原子均能共价键结合,都属原子晶体,故D正确;
故选:D.
点评: 本题考查了几个常见的概念,要注意对概念的准确把握,题目难度不大.


 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案科目:高中化学 来源: 题型:
FeBr2是一种黄绿色鳞片状的固体,某研究性学习小组为了探究它的还原性,进行了如下实验:
I.实验需要90mL 0.1mol/L FeBr2溶液
(1)配制FeBr2溶液除烧杯、量筒、胶头滴管外还需的玻璃仪器是 、
(2)下列有关配制过程中说法错误的是 (填序号).
a.用电子天平称量质量为1.944g的FeBr2
b.将称量的FeBr2放入容量瓶中,加90nL蒸馏水溶解
c.洗涤溶解FeBr2的烧杯,并将洗涤液转移至容量瓶中
d.容量瓶贴签存放配好的FeBr2溶液
e.定容时,仰视容量瓶刻度线会使配制的FeBr2溶液浓度偏高
II.探究FeBr2的还原性
取10mL上述FeBr2溶液,向其中滴加少量新制的氯水,振荡后溶液呈黄色.某同学对产生黄色的原因提出了假设:
假设1:Br﹣被C12氧化成Br2溶解在溶液中; 假设2:Fe2+被C12氧化成Fe3+.
(1)请你完成表格,验证假设:
实验步骤、预期现象 结论
①溶液中加入适量四氯化碳 假设1正确
②向溶液中加入 假设2正确
若假设1正确,从实验①中分离出Br2的实验操作名称是 ;
(2)实验证明:还原性Fe2+>Br﹣,请用一个离子方程式来证明: ;
(3)若在50mL上述FeBr2溶液中通入5×10﹣3molCl2,反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
为预防“H1N1”甲型流感,同学们每天用“84”消毒液(NaClO溶液)消毒,下列说法不正确的是()
A. NaClO溶液的消毒原理是使蛋白质变性
B. 1 mol Cl2与足量NaOH溶液反应转移2 mol电子
C. NaClO溶液的漂白原理与Na2O2相同,与SO2不同
D. “84”消毒液与“洁厕灵”(盐酸)混合使用可能会产生有毒的氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是()
A. 0.1 mol.L﹣1 NaOH溶液:K+、Na+、SO42﹣、CO32﹣
B. 0.1 mol•L﹣1 Na2CO3溶液:K+、Ba2+、NO3﹣、Cl﹣
C. 0.1 mol•L﹣1 FeCl3溶液:K+、NH4+、I﹣、SCN﹣
D. 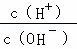 =1×l014的溶液:Ca2+、Na+、ClO﹣、NO3﹣
=1×l014的溶液:Ca2+、Na+、ClO﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:Sn(s)+Pb2+(aq)Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示.下列判断正确的是()
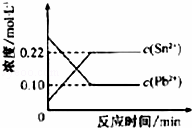
A. 往平衡体系中加入金属铅后,c(Pb2+)增大
B. 往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小
C. 升高温度,平衡体系中c(Pb2+)增大,说明该反应为吸热反应
D. 25℃时,该反应的平衡常数K=2.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com