
下列离子方程式正确的是( )
A.铜片插入到硝酸银溶液中:Cu+Ag+=Cu2++Ag
B.硫酸镁跟氢氧化钡反应:Ba2++SO42-=BaSO4↓
C.铁片插入盐酸中:2Fe+6H+=2Fe3++3H2↑
D.氢氧化钠溶液和硫酸溶液反应:H++OH-=H2O
科目:高中化学 来源:2016-2017学年江西省宜春市高一上月考二化学卷(解析版) 题型:选择题
下列物质中,属于电解质但 不能导电的是( )
不能导电的是( )
A.四氯化碳 B.熔融的氯化铝 C.液态氯化钠 D.石墨
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省饶阳县高一上期中化学试卷(解析版) 题型:选择题
下列可以大量共存且溶液是无色的离子组是( )。
A.H+、Na+、NO3-、Cu2+ B.Ba2+、Mg2+、Cl-、SO42-
C.H+、K+、OH-、NO3- D.NO3-、SO42-、K+、Mg2+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:推断题
某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+中的几种阳离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是________。
(2)取少量原溶液加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,白色沉淀不消失,原溶液中肯定有的离子是_______,离子反应方程式为 。
(3)取(2)的滤液加入过量NaOH,出现白色沉淀,说明原溶液中肯定存在的离子有 。
(4)原溶液中可能大量存在的阴离子是下列A~D中的(填序号)________。
A.Cl- B.NO3- C.CO3 2- D.OH-
2- D.OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:选择题
在2H2S+SO2=2H2O+3S中,氧化剂与还原剂的分子个数比为 ( )
A.2∶1 B.1∶2 C.1∶1 D.16∶17
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一上期中化学卷(解析版) 题型:选择题
下列说法正确的是 ( )
A.硫酸、纯碱、碳酸氢钠和生石灰分别属于酸、碱、盐和氧化物
B.用丁达尔效应区别FeCl3溶液和Fe(OH)3胶体
C.生石灰与水混合的过程只发生物理变化
D.H2O、CH3COOH、Cu(NH3)4SO4均含有氧,都是氧化物
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高二上期中化学卷(解析版) 题型:填空题
氨气是重要的化工原料
(1)已知: N2(g)+O2(g)= 2NO(g) △H = +180.5kJ·mol-1
4NH3(g)+5O2(g)= 4NO(g)+6H2O(g) △H = -905kJ·mol-1
2H2(g)+O2(g)= 2H2O(g) △H = -483.6kJ·mol-1
写出氨气在高温高压催化剂条件下生成氮气和氢气的热化学方程式:
;如果在1L密闭容器中,3mol NH3 在等温条件下充分反应,2min后达到平衡,平衡时的反应热为92.4kJ ,则在这段时间内v(H2)= ;保持温度不变,将起始NH3的物质的量调整为8mol,平衡时NH3的转化率为  。
。
(2)一定条件下,某密闭容器中发生反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
4NO(g)+6H2O(g)。在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 (填字母代号)。
A.增大压强 B.适当升高温度 C.增大O2的浓度 D.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长株潭岳益五市十校高三12月联考化学卷(解析版) 题型:实验题
化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:①该牙膏摩擦剂由碳酸钙、氢氧化铝组成;
②牙膏中其它成分遇到盐酸时无气体产生。
实验内容:Ⅰ.摩擦剂中氢氧化铝的定性检验。
取适量牙膏样品,加水充分搅拌、过滤,往滤渣中加入过量NaOH溶液。
(1)该过程涉及主要反应的离子方程式是 。
Ⅱ.牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的沉淀质量,以确定碳酸钙的质量分数。
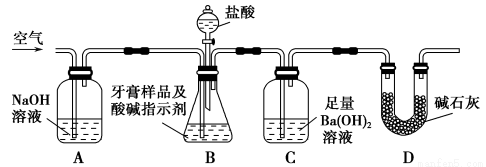
依据实验过程回答下列问题:
(2)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:_________________________。
(3)C中反应生成沉淀的化学方程式是_____________________。
(4)下列各项措施中,能提高测定准确度的是________(填标号)。
a.滴加盐酸不宜过快
b.在A~B之间增添盛有浓硫酸的洗气装置
c.在加入盐酸之前,应排净装置内的CO2气体
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)实验中准确称取10.00 g样品三份,进行三次测定,测得C中产生沉淀平均质量为3.94 g。则样品中碳酸钙的质量分数为________。
(6)有人认为只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是______________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省分校高一上期中化学卷(解析版) 题型:实验题
某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42ˉ。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2),设计了如图所示的流程图:
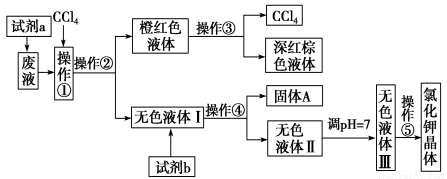
可供试剂a、试剂b(试剂b代表一组试剂)选择的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、KOH溶液、BaCl2溶液、Ba(NO3)2溶液、H2O2溶液、酸性KMnO4溶液、稀盐酸。
请根据流程图,回答相关问题:
(1) 操作①②③④⑤的名称是_____________
①_______②________③________④________⑤________
(2) 除去无色液体Ⅰ中的Ca2+、Mg2+、SO42ˉ, 选出试剂b所代表的试剂,按滴加顺序依次是________________(填化学式)。
选出试剂b所代表的试剂,按滴加顺序依次是________________(填化学式)。
(3)调节pH的目的是____________________,操作方法是_______________________。
(4)操作⑤中用到的瓷质仪器名称是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com