
【题目】对于以下反应:A(s)+3B(g) ![]() 2C(g)+D(g),在一定温度、压强下,在体积可变的某容器中,当下列物理量不再发生变化时就可确定一定达到平衡状态的是
2C(g)+D(g),在一定温度、压强下,在体积可变的某容器中,当下列物理量不再发生变化时就可确定一定达到平衡状态的是
A. 混合气体的密度不随时间变化而变化 B. 3v正(B)=v逆(D)
C. 混合气体的压强保持不变 D. B、C、D的分子数之比为3:2:1
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
【题目】下列实验装置或操作设计正确、且能达到目的的是( )
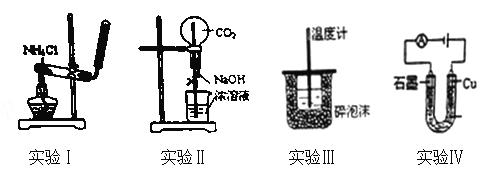
A. 实验Ⅰ:实验室制备氨气
B. 实验Ⅱ:用二氧化碳作喷泉实验
C. 实验Ⅲ:进行中和热的测定
D. 实验Ⅳ:电解氯化铜溶液得到铜和氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业含铜废料含有Cu、CuO、CuS、CuSO4等成分,利用该含铜废料可生产硝酸铜晶体[Cu(NO3)2 3H2O],其生产工艺流程如图所示:
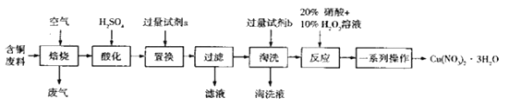
回答下列问题:
(1)“焙烧”过程中生成SO2的化学方程式为___________________。
(2)“酸化”过程的离子方程式为__________________________。
(3)试剂a可以是__________________。
(4)“淘洗”的目的是___________,图中的淘洗液与滤液溶质的阴离子相同,則试剂b是__________,淘洗液的溶质是__________。
(5)“反应”中使用20%硝酸和10% H2O2溶液,硝酸起酸的作用,则“反应”的化学方程式为______________。若该步骤只使用20%硝酸,随着反应的进行,温度升高,出现大量红棕色气体,则生成红棕色气体时反应中还原剂与氧化剂的物质的量之比为___________。
(6)“一系列操作”是指化学实验操作,这些操作需要用到的玻璃仪器有_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由反应物 X 分别转化为 Y 和 Z 的能量变化如图所示。下列说法正确的是( )

A.由 X→Z 反应的 ΔH<0 B.由 X→Y 反应的 ΔH=E5-E2
C.增大压强有利于提高 Y 的产率 D.升高温度有利于提高 Z 的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙可以用于改善地表水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。实验室可用工业碳酸钙(含MgCO3、FeCO3等杂质)制取纯净的碳酸钙,然后再用纯的碳酸钙制取过氧化钙,其主要流程如下:
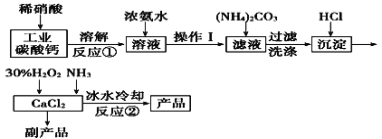
已知:CaO2·8H2O呈白色微溶于水。
(1)写出反应①中氧化还原反应的离子方程式: ______________。
(2)向反应①后的溶液中加浓氨水的目的是: __________________。
(3)反应②常用冰水控制温度在0℃左右,其可能原因是(写出两种):
①__________________;②______________。
(4)测定产品中CaO2的含量的实验步骤是
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴滴入浓度为c mol·L-1的Na2S2O3标准溶液至反应终点,消耗Na2S2O3溶液V mL。
已知:I2+2S2O![]() ===2I-+S4O
===2I-+S4O![]() 。
。
①滴定终点的现象为____________,产品中CaO2的质量分数为_________________
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________ (填“不受影响”“偏低”或“偏高”),原因是_____________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx会引起光化学烟雾等环境问题,在催化剂存在条件下,以NH3或尿素将尾气中NOx
还原为N2的技术,即NH3或尿素-SCR技术,是去除NOx最为有效且应用最广的技术之一,其中最重要的催化剂体系是钒基催化剂。
(1)NH3去除尾气中的NOx,当v(NO):v(NO2)=l:1时称为“快速SCR 反应”,该反应化学方程式为___________。
(2)不同钒含量的催化剂(V2O5/TiO2)添加WO3对NO去除率的影响如下图,从图中可以得出其它条件相同时添加WO3,对NO去除率的影响是_____(填“增大”、“减小”或“无影响”)。根据图中所示,随着温度升高NO去除率的变化趋势为_____,该变化趋势的一种可能原因是___________。

(3)在制备钒基催化剂时,添加的各种成型助剂中碱金属或碱土金属(如Na、K、Ca)能够使催化剂中毒(催化性能下降), K、Ca的毒化作用与Na相似。下列适合做成型助剂有_____。
A.Li B.Mg C.酸性铝溶胶 D.酸性硅溶胶
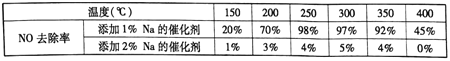
请设计实验研究添加金属K对催化剂活性的影响(只需写出实验思路,不需要具体实验
操作)_____________。
(4)在NOx催化去除过程中,NH3储罐存在危险性,更多应用为尿素-SCR技术。在该技术过程中,发生如下两个反应:
① CO(NH2)2=NH3+HNCO
② HNCO(g)+H20(g)====NH3(g)+CO2(g)
在此过程中一分子尿素可以生成两分子NH3,因此尿素被视为是NH3的有效储存源。反应②的平衡常数表达式为_______。目前商用的尿素溶液浓度为32.5%(密度为1.05g/mL),常称为“Ad Blue ”。1L该商用尿素溶液发生“快速SCR反应”, 理论上最多可消除NO和NO2在标准状况下的体积为______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞中的化合物的叙述中正确的是
A. 细胞中大多数无机盐以化合物的形式存在
B. 核糖核苷酸链一定不含氢键
C. 变性后的蛋白质不能与双缩脲发生紫色反应
D. 纤维素、淀粉和糖原进行彻底水解得到的产物相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别与其他分散系的本质特征是( )
A.能发生丁达尔现象
B.胶体粒子能通过滤纸空隙
C.胶体在一定条件下能稳定存在
D.胶体分散质粒子直径在1nm~100nm之间
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com