
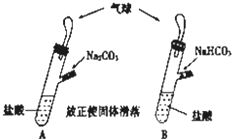
 有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06g Na2CO3和0.84gNaHCO3,A、B中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
有A、B两个完全相同的装置,某学生分别在它们的侧管中装入1.06g Na2CO3和0.84gNaHCO3,A、B中分别有10mL相同浓度的盐酸,将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )| A. | A装置的气球膨胀速度比B快 | |
| B. | 若最终两气球体积相同,则盐酸的浓度一定大于或等于2 mol/L | |
| C. | 若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol/L | |
| D. | 最终两试管中Na+、Cl-的物质的量一定相同 |
分析 A.碳酸氢钠反应生成二氧化碳的速率更快;
B.最终两气球体积相同,说明生成二氧化碳的体积相同,则盐酸必须足量,保证碳酸钠和碳酸氢钠完全反应;
C.最终两气球体积不相同,生成二氧化碳的体积不相同,则盐酸不足;
D.Na2CO3和NaHCO3的物质的量相同,两试管中钠离子的物质的量不同.
解答 解:A.碳酸钠和酸反应分步进行,先生成碳酸氢钠,后碳酸氢钠和酸反应生成二氧化碳,碳酸氢钠反应生成二氧化碳的速率更快,所以A装置的气球膨胀速度比B慢,故A错误;
B.1.06g Na2CO3和0.84gNaHCO3的物质的量均为0.01mol,若最终两气球体积相同,说明生成二氧化碳物质的量相等,则盐完全反应,则氯化氢的物质的量大于或等于0.02mol,其浓度大于或等于2mol/L,故B正确;
C.碳酸钠和酸反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2 ↑+H2O,碳酸氢钠和酸反应的离子方程式为HCO3-+H+=CO2 ↑+H2O,若最终两气球体积不同,所需酸的物质的量范围是:0<n(HCl)<0.02mol,所以其浓度小于2mol/L,故C错误;
D.两试管中氯离子物质的量相等,而Na2CO3和NaHCO3的物质的量均为0.01mol,所以Na2CO3和 NaHCO3中钠离子的物质的量不同,故最终两试管中Na+的物质的量一定不相同,故D错误.
故选B.
点评 本题考查了碳酸钠和碳酸氢钠的性质,试题培养了学生的分析能力及灵活应用能力,注意碳酸钠和盐酸的反应分步进行,先生成碳酸氢钠,后碳酸氢钠和酸反应生成二氧化碳,


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 过滤、结晶、灼烧、萃取、分液和蒸馏等都是常用的分离有机混合物的方法 | |
| B. | 在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度,充分反应后再读出并记录反应体系的最高温度 | |
| C. | 实验室用已知浓度的醋酸溶液滴定未知浓度的氢氧化钠溶液时,选用酚酞做指示剂比用甲基橙做指示剂时带来的误差要小一些 | |
| D. | 溶液配制、中和滴定实验中,容量瓶、锥形瓶用蒸馏水洗净后即可使用;而滴定管、移液管用蒸馏水洗净后,须再用待盛液润洗2~3次后方可使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气有氧化性,作用于正常细胞而癌化 | |
| B. | 氯水中的次氯酸具有杀菌性,氧化了正常细胞,异化为癌细胞 | |
| C. | 氯气有毒,杀死正常细胞,不杀灭癌细胞 | |
| D. | 氯气作用于水中有机物,生成有机氯化合物而致癌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ② | C. | ③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | N2O | B. | NO2 | C. | N2O5 | D. | NaNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸保存在无色的玻璃瓶中 | |
| B. | 氯水应保存在带橡胶塞的棕色细口瓶中 | |
| C. | 金属钠应保存在汽油中防止被氧化 | |
| D. | 保存硫酸亚铁溶液时可向里面加少量铁屑 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com