
| A.硫铁矿燃烧前需将矿粒粉碎,这样易于向沸腾炉中投料 |
| B.炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应 |
| C.SO2氧化为SO3时需使用催化剂,这样可提高SO2的转化率 |
| D.接触室的反应温度控制在400~500 ℃,因为在该温度范围内催化剂的活性较高 |
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) ΔH<0,下列说法正确的是( )。
2NH3(g) ΔH<0,下列说法正确的是( )。| A.达到平衡时反应物和生成物浓度一定相等 |
| B.达到平衡后加入氨气,重新达到平衡时,氨气的浓度比原平衡时大 |
| C.达到平衡时,升高温度加快了吸热反应的速率,降低了放热反应的速率,所以平衡向逆反应的方向移动 |
| D.加入催化剂可以缩短到达平衡的时间,这是因为加快了正反应的速率,而减慢了逆反应的速率 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
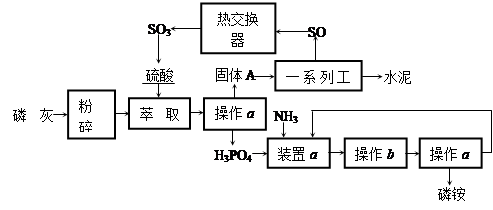
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
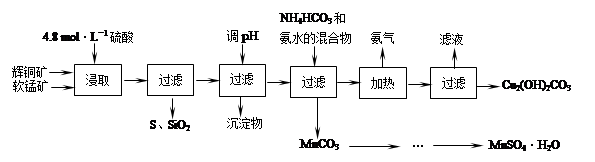
| | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
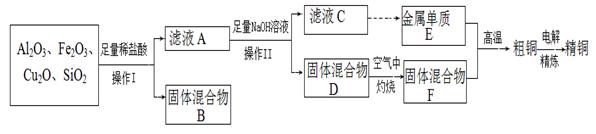
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电解法制金属钠时,负极反应式:Na++e-=Na |
| B.电解法生产铝时,需对铝土矿进行提纯,在提纯过程中应用了氧化铝或氢氧化铝的两性 |
| C.在氯碱工业中,电解池中的阴极产生的是H2 , NaOH 在阳极附近产生 |
| D.氯碱工业和金属钠的冶炼都用到了NaCl ,在电解时它们的阴极都是 C1一失电子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;常温时Ksp[Fe(OH)3]=c(Fe3+).c3(OH-)=1.0×10-38。试回答:
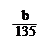 mol
mol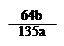 ×100℅
×100℅ 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2 NH3 (g); △H <0, 该反应应采取的适宜条件是( )
2 NH3 (g); △H <0, 该反应应采取的适宜条件是( )| A.低温、高压、催化剂 | B.适宜的温度、高压、催化剂 |
| C.低温、常压、催化剂 | D.适宜的温度和压强、催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com