
| A、溶液的导电能力比盐酸弱 |
| B、1mol/L醋酸溶液中c(H+)=0.01 mol?L-1 |
| C、醋酸能与水任何比例互溶 |
| D、与等物质的量的NaOH恰好完全反应 |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| MrX |
| VN |
A、以g为单位
| ||
| B、以g为单位1L该气体的质量 | ||
| C、1L该气体中所含的分子数 | ||
| D、以L为单位1mol该气体的体积 |
查看答案和解析>>
科目:高中化学 来源: 题型:
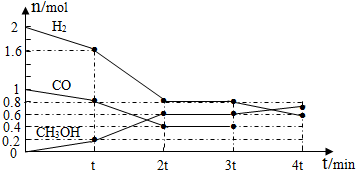
 由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.
由碳元素构成的各种单质和化合物始终都是科学家研究的重要对象.| 1 |
| 2 |
| 容器编号 | c(CO)/mol?L-1 | c(O2)/mol?L-1 | c(CO2)/mol?L-1 | v(正)和v(逆)比较 |
| Ⅰ | 2.0×10-4 | 4.0×10-4 | 4.0×10-2 | v(正)=v(逆) |
| Ⅱ | 3.0×10-4 | 4.0×10-4 | 5.0×10-2 | v(正) |


查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
元素 | 各电子层的电子数 | ||||
| K | L | M | N | ||
| A | 2 | 7 | |||
| B | 2 | 8 | 1 | ||
| C | 2 | 8 | 18 | 7 | |
| D | 2 | 8 | 2 | ||
| E | 2 | 8 | 7 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
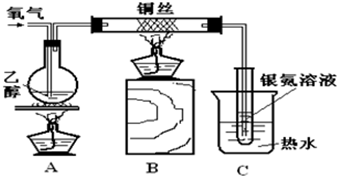
 某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.
某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com