
| A. | 溶解时有少量液体溅出 | B. | 洗涤液未全部转移到容量瓶中 | ||
| C. | 容量瓶使用前未干燥 | D. | 定容时液面未到刻度线 |
科目:高中化学 来源: 题型:选择题
| A. | 1mol的  与足量的NaOH溶液反应,能消耗3mol NaOH 与足量的NaOH溶液反应,能消耗3mol NaOH | |
| B. | 可用氢氧化钠溶液除去乙酸乙酯中残留的乙酸 | |
| C. | 间二甲苯也叫1,5-二甲苯 | |
| D. | 乙二醇和丙三醇互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种定香剂,以芳香醇A为原料合成H的一种流程如图:
)是一种定香剂,以芳香醇A为原料合成H的一种流程如图:
 +H2O(R1、R表示氢原子或烃基)
+H2O(R1、R表示氢原子或烃基) ;H的官能团名称是碳碳双键、酯基.
;H的官能团名称是碳碳双键、酯基. .
. (写一种即可).
(写一种即可).查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 柠檬酸分子式为C6H9O7 | |
| B. | 使用食品添加剂属于违法行为 | |
| C. | 柠檬酸可用作食品抗氧化剂,说明其有较强氧化性 | |
| D. | 柠檬酸分子含三个羧基(-COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 金属钠和水反应 | B. | 生石灰变成熟石灰的反应 | ||
| C. | Al和Fe2O3的铝热反应 | D. | CaCO3受热分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量二氧化碳通入“水玻璃”中:CO2+SiO32-+H2O═CO32-+H2SiO3↓ | |
| B. | 碳酸钙与稀盐酸混合:CO32-+2H+═CO2↑+H2O | |
| C. | 铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ | |
| D. | Al2O3溶于NaOH溶液中:Al2O3+2OH-═2[Al(OH)4]- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验现象 | 原因分析 |
| A | 久置的浓硝酸呈黄色 | 浓硝酸不稳定,分解生成的NO2 溶解在其中 |
| B | 铝片先用砂纸打磨,再加入到浓硝酸中,无明显现象 | 浓硝酸具有强氧化性,常温下,铝被浓硝酸钝化 |
| C | SO2通入酸性高锰酸钾溶液中,溶液紫红色褪去 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
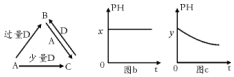
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com