
| A. | 为了防止富脂食品氧化变质,延长食品的保质期,常在包装袋中放入生石灰 | |
| B. | 海水中含有丰富的碘元素,因此碘被称为“海洋元素” | |
| C. | 工业生产玻璃、水泥、漂白粉,均需要用石灰石为原料 | |
| D. | 可以利用氯化铁溶液的酸性清除铜镜表面的铜锈 |
分析 A.生石灰不能防止食品被氧化;
B.溴被称为“海洋元素”,不是碘;
C.制玻璃的原料:石英砂、石灰石、长石、纯碱、硼酸等;制水泥的原料:石灰石和黏土;制漂白粉的原料:用石灰石可以制得氧化钙进而得到消石灰,用氯气与消石灰反应得到漂白粉;
D.氯化铁水解后溶液呈酸性,表面的铜锈与酸反应后铁离子再与铜反应.
解答 解:A.生石灰具有吸水性,可用作干燥剂,不能防止食品被氧化,故A错误;
B.溴是海水中重要的非金属元素,地球上99%的溴元素存在于海水中,所以人们也把溴称为“海洋元素”,故B错误;
C.制玻璃的原料:石英砂、石灰石、长石、纯碱、硼酸等;制水泥的原料:石灰石和黏土;制漂白粉的原料:用石灰石可以制得氧化钙进而得到消石灰,用氯气与消石灰反应得到漂白粉,因此工业上生产玻璃、水泥、漂白粉,均需要用石灰石为原料,故C正确;
D.氯化铁水解生成氢氧化铁和盐酸,生成的盐酸与铜锈反应,露出的铜再与三价铁反应,故D错误;
故选C.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、性质与用途的关系为解答的关键,侧重分析与应用能力的考查,注意化学与生活的关系,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 14g 分子式为CnH2n的链烃中含有的C-H键的数目为2NA | |
| B. | Na2O2与H2O的反应中每生成0.1molO2,转移电子数目为0.4NA | |
| C. | 常温常压下,1.7g NH3所含电子数为0.8NA | |
| D. | 标准状况下,11.2L NO与11.2LO2混合,原子总数小于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12.0gNaHSO4晶体中阳离子数为0.2NA个 | |
| B. | 0.1 mol Cu与足量热的浓硫酸反应生成SO2的体积约为22.4 L | |
| C. | T℃时,1L pH=6的纯水中,含1×10-6NA个H+ | |
| D. | 标准状况下,1 L pH=13的NaOH溶液中OH-为0.1NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 现象 | 结论 | |
| A. | 向2 mL 0.1FeCl 3的溶液中加足量铁粉,震荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
| B. | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
| C. | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
| D. | 向2支盛有2 mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液 | 一只试管中产生黄色沉淀,另一支中无明显现象 | Ksp(AgI)<Ksp(AgCl) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

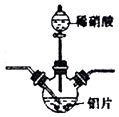
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
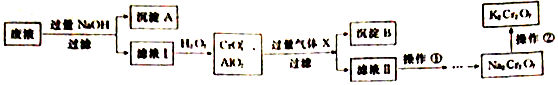
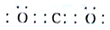 (填电子式)
(填电子式)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )
支持海港码头基础的防腐技术,常用外加电流的阴极保护法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极.下列有关表述不正确的是( )| A. | 通入保护电流使钢管桩表面腐蚀电流接近于零 | |
| B. | 通电后外电路电子被强制从高硅铸铁流向钢管桩 | |
| C. | 高硅铸铁的作用是作为损耗阳极材料和传递电流 | |
| D. | 通入的保护电流应该根据环境条件变化进行调整 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
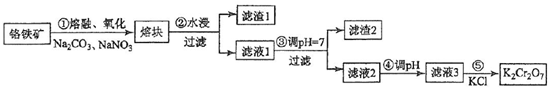
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升温 | B. | 增大反应器的体积 | ||
| C. | 增大c(A) | D. | 降温 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com