
已知H2(g)+Cl2(g)=2HCl(g),ΔH = —184.6 kJ·mol-1
则反应HCl(g)= 1/2H2(g)+1/2Cl2(g)的ΔH是
A.+184.6kJ·mol-1 B.—369.2 kJ·mol-1
C.+92.3 kJ·mol-1 D.—92.3 kJ·mol-1
科目:高中化学 来源: 题型:
对已达化学平衡的下列反应 2X(g)+Y(g)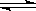 2Z(g)减小压强时,对反应产生的影响是( )
2Z(g)减小压强时,对反应产生的影响是( )
A 逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B 逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C 正、逆反应速率都减小,平衡向逆反应方向移动
D 正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3(g)燃烧生成NO2 (g)和H2O(g),已知
(1)2H2(g)+ O2 (g)=2H2O(g) △H =-483.6 kJ/mol
(2)N2 (g)+2O2 (g)=2NO2 (g) △H = + 67.8 kJ/mol
(3)N2 (g)+ 3H2 (g)=2NH3(g) △H =-92.0 kJ/mol
试计算后写出NH3(g)燃烧的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中,正确的是
A.在气体反应中,增大压强能使反应物中活化分子数和活化分子百分数同时增加
B.活化分子间的碰撞一定是有效碰撞
C.不同化学反应需要的活化能有可能差别很大
D.反应的活化能大小不会影响化学反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
现有pH=3的醋酸和pH=3的硫酸两种溶液,下列说法正确的是
A.加水稀释100倍后两溶液的pH仍相同
B.两溶液中分别加入足量的锌片放出H2的体积相同
C.醋酸中的c (CH3COO—)和硫酸中的c(SO42—) 相同
D.两溶液中水电离出的c(H+)=1×10—11mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
二氧化氮在加热条件下能够分解成一氧化氮和氧气。该反应进行到45秒时,达到平衡(NO2浓度约为0.0125 mol/L)。下图中的曲线表示二氧化氮分解反应在前25秒内的反应进程。

(1)请计算前20秒内氧气的平均生成速率为_______________。
(2) 若反应延续至70秒,请在图中用实线画出25秒至70秒的反应进程曲线。
(3) 若在反应开始时加入催化剂(其他条件都不变),请在图上用虚线画出加入催化剂后的反应进程曲线。
(4)写出该反应的化学平衡常数表达式K=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示甲~丁四种物质均含有同一种元素,甲可以是单质也可以是气态氢化物,丁是该元素最高价氧化物对应的水化物,则甲、乙、丙、丁四种物质中共同含有的元素可能是( )

A.Cl B.Fe C.C D.N
查看答案和解析>>
科目:高中化学 来源: 题型:
部分弱酸的电离平衡常数如下表所示:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列选项正确的是( )
A.2CN-+H2O+CO2===2HCN+CO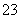
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C.物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)<c(K+)-c(CN-)
D.c(NH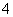 )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  △H3
△H3
回答下列问题:
化学键 | H-H | C-O | C | H-O | C-H |
E/(kJ.mol-1) | 436 | 343 | 1076 | 465 | 413 |
(1)已知反应①中的相关的化学键键能数据如下:
由此计算△H1= kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3= kJ.mol-1
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是  。
。
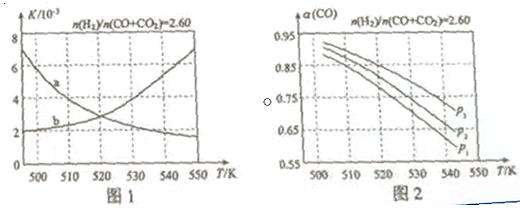
(3)合成气的组成n(H2)/n(CO+CO2)=2.60时体系中的CO平衡转化率(a)与温度和压强的关系如图2所示。a(CO)值随温度升高而 (填“增大”或“减小”),其原因是 。图2中的压强由大到小为_____,其判断理由是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com