
【题目】从海水里可以提取溴,主要反应为2Br﹣+Cl2=2Cl﹣+Br2,下列说法正确的是( )
A.溴离子具有氧化性B.氯气是还原剂
C.该反应属于复分解反应D.Br2是氧化产物
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】有甲、乙两位学生利用原电池反应检测金属的活动性顺序,两人都使用镁片与铝片作电极,但甲同学将电极放入6 mol·L-1硫酸溶液中,乙同学将电极放入6 mol·L-1的氢氧化钠溶液中,如下图所示。
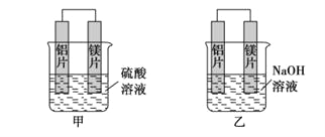
(1)写出甲池中正极的电极反应式_______________________________________。
(2)写出乙池中负极的电极反应式________________________________________。
(3)写出乙池中总反应的离子方程式_______________________________________。
(4)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________活动性更强,而乙会判断出________活动性更强(填写元素符号)。
(5)由此实验,可得到如下哪些结论正确(____)
A.利用原电池反应判断金属活动顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
(6)上述实验也反过来证明了“直接利用金属活动顺序判断原电池中的正负极”这种做法________(可靠或不可靠)。如不可靠,请你提出另一个判断原电池正负极的可行实验方案________________(如可靠,此空可不填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间有如下转化关系: 下列有关物质的推断不正确的是 ( )
下列有关物质的推断不正确的是 ( )
A. 若甲为AlC13溶液,则丁可能是NaOH溶液 B. 若甲为N2,则丁可能是O2
C. 若甲为Fe,则丁可能是稀硝酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修3:物质结构与性质]
(1)丙酮(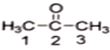 )分子中2号碳原子的杂化方式为__________;
)分子中2号碳原子的杂化方式为__________;
(2)写出镍原子的电子排布式_____________;
(3)H2O分子的键角比NH3分子的键角小,原因是_____________________________________ ;
(4)N、P、As属于同族元素,它们的简单氢化物沸点由大到小的顺序为_________________(用化学式表示),其原因是 ____________________________________;
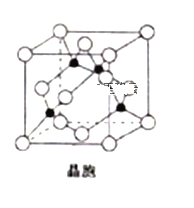
(5)由铜与氯形成的一种化合物的晶胞结构如图所示(黑点代表铜原子)。
①将晶胞内的4个黑点相互连接所形成的立体构型是______________;
②晶体中与一个氯原子距离最近的氯原子有___________个;
③已知该晶体的密度为ρg.cm-3,阿伏加德罗常数的值为NA,则该晶体中铜原子和氯原子之间的最短距离为____________pm(列出计算式即可);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着原子序数的递増,八种短周期元素(用字母x、y、z…表示)的原子半径的相对大小、最高正价或最低负价的变化如下图所示。请根据判断出的元素回答下列问题

(1)f在元素周期表中的位置是第三周期第____族。
(2)比较d、e常见离子的半径大小:_______(用化学符号表示且用“>”连接,下同)。比较g、h的最高价氧化物对应的水化物的酸性强弱:_______
(3)写出x与z形成的常见四原子共价化合物的电子式_______
(4)物质A是一种常用的比水轻的有机溶剂,其仅由x、y两种元素组成,且y元素与x元素的质量比为12:1,A的相对分子质量为78。A与浓硫酸、浓硝酸在50~60℃下发生反应的化学方程式为__________,反应类型为__________。
(5)f的最高价氧化物对应的水化物可以与e的最高价氧化物对应的水化物反应,请写出该反应的离子方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
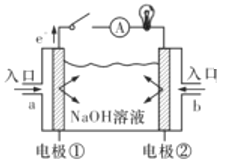
(1)若该燃料电池为氢氧燃料电池。
①a极通入的物质为_____(填物质名称),电解质溶液中的OH—移向______极(填”负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:______________。
(2)若该燃料电池为甲烷燃料电池。已知电池的总反应为CH4+2O2+2OH-=CO32-+3H2O
①下列有关说法正确的是___________(填字母代号)。
A.燃料电池将电能转变为化学能
B.负极的电极反应式为CH4+10OH--8e-=CO32-+7H2O
C.正极的电极反应式为O2+4H++4e-=2H2O
D.通入甲烷的电极发生还原反应
②当消耗甲烷33.6L(标准状况下)时,假设电池的能量转化效率为80%,则导线中转移的电子的物质的量为______mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处于平衡状态的反应2 H2 S(g) ![]() 2H2(g)+S2(g)
2H2(g)+S2(g) ![]() H>0,不改变其他条件的情况下合理的说法是
H>0,不改变其他条件的情况下合理的说法是
A.加入催化剂,反应途径将发生改变,![]() H也将随之改变
H也将随之改变
B.升高温度,正逆反应速率都增大,H2S分解率也增大
C.增大压强,平衡向逆反应方向移动,将引起体系温度降低
D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①NaCl、②干冰、③冰、④Na2O2、⑤白磷(P4)、⑥金刚石、⑦Na2CO3、⑧钠。以上物质中属于离子晶体的是____________;属于分子晶体的是____________(填序号)。氯化钡是无色晶体,溶于水,水溶液能导电,熔点1 560 ℃。它可能属于____________晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com