
| A、78gNa2O2固体中含有的阴离子数为NA |
| B、标准状况下,2.24L氖气所含原子数为0.2NA |
| C、1L 0.1 mol/L醋酸溶液中含有的氢离子数为0.1NA |
| D、标准状况下,2.24L己烷含有分子的数目为0.1NA |
| 78g |
| 78g/mol |
| 2.24L |
| 22.4L/mol |


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、为了加快过滤速度,可用玻璃棒搅拌过滤器中的液体 |
| B、为了防止蒸馏时温度过高,可将温度计插入液面以下 |
| C、为了使制取氢气的速率加快,可向稀硫酸中加入少量硫酸铜溶液 |
| D、为了使配制的FeCl3溶液不产生浑浊,可加入盐酸和铁片 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无色溶液:Ca2+、H+、Cl-、HSO3- | ||
| B、能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- | ||
| C、AlCl3溶液:K+、Na+、SO42-、AlO2- | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
| B、CuSO4溶液中加入过量Ba(OH)2溶液:Ba2++SO42-═BaSO4↓ |
| C、铜与AgNO3溶液反应:Cu+2Ag+═Cu2++2Ag |
| D、碳酸钙与过量盐酸的反应:CO32-+H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
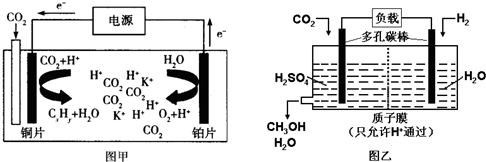
| A、甲中铜片作阴极,K+向铜片电极移动 |
| B、乙中正极发生的电极反应为CO2+6e-+6H+═CH3OH+H2O |
| C、甲中若CxHy为C2H4,则生成1mol C2H4的同时生成2mol O2 |
| D、乙中H2SO4的作用是增强溶液的导电性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S2- NO3- NH4+ K+ |
| B、OH- Na+ Cl- K+ |
| C、NO3- Fe3+ Cl- SO42- |
| D、SO32- H+ K+ NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 mL |
| B、15mL |
| C、大于15mL |
| D、大于10 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
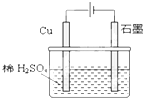
| A、电解过程中,铜电极上没有H2产生 | ||||
B、电解初期,主反应方程式为:Cu+H2SO4
| ||||
| C、电解一定时间后,石墨电极上有铜析出 | ||||
| D、整个电解过程中,H+的浓度不断增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com