
【题目】将Mg、Cu组成的2.64 g混合物投入到100 mL稀硝酸中完全溶解,并收集还原产物NO气体(还原产物只有一种)。然后向反应后的溶液中逐滴加入2 mol·L-1NaOH溶液,下图是生成沉淀的质量与滴入NaOH溶液体积间的关系图。以下说法不正确的是( )
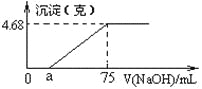
A. 稀硝酸的浓度为1.9 mol/L
B. 生成的NO在标况下的体积为0.896 L
C. a的值为15
D. Cu的物质的量为0.02 mol
【答案】D
【解析】试题分析:设Mg、Cu的物质的量分别为x mol、y mol,则有
![]()
解得x=0.03,y=0.03。故D错误;沉淀达最大值时,溶液中的溶质只有NaNO3,根据电荷守恒得n(![]() )=n(Na+)="2" mol·L-1×0.075 L="0.15" mol。根据电子得失守恒知0.03 mol×2+0.03 mol×2=n(NO)×3,解得n(NO)="0.04" mol,在标况下的体积为0.896 L,B项正确。根据N原子守恒得n(HNO3)="n(NO)+0.15" mol="0.19" mol,故c(HNO3)="1.9" mol·L-1,A项正确。由题意知a点溶液中存在Mg2+、Cu2+、Na+、
)=n(Na+)="2" mol·L-1×0.075 L="0.15" mol。根据电子得失守恒知0.03 mol×2+0.03 mol×2=n(NO)×3,解得n(NO)="0.04" mol,在标况下的体积为0.896 L,B项正确。根据N原子守恒得n(HNO3)="n(NO)+0.15" mol="0.19" mol,故c(HNO3)="1.9" mol·L-1,A项正确。由题意知a点溶液中存在Mg2+、Cu2+、Na+、![]() ,根据电荷守恒得0.03 mol×2+0.03 mol×2+2 mol·L-1×a×10-3L="0.15" mol,解得a=15
,根据电荷守恒得0.03 mol×2+0.03 mol×2+2 mol·L-1×a×10-3L="0.15" mol,解得a=15
,故C正确。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】①甲烷、②乙烷、③乙烯、④苯、⑤甲苯、⑥二甲苯、⑦乙醇、⑧乙酸,它们都是常见的重要化工原料。
(1)上述物质中,氢元素的质量分数最大的是______填分子式;
(2)分别写出⑦、⑧中所含官能团的名称____________、____________二者发生酯化反应的化学方程式为_________________________________________________,如果用4.6g乙醇和9.0g乙酸充分反应制得乙酸乙酯5.28g,则本实验的产率是:__________产率指的是目标生成物的实际产量与理论产量的比值。
(3)上述物质中,能发生加成反应的烃类物质有:__________________________填序号。
(4)下列物质中,不能通过乙烯加成反应得到的是______填序号。
a.CH3CH3b.CH3CHCl2c.CH3CH2Br
(5)苯、甲苯、二甲苯是用途广泛的有机溶剂。二甲苯的结构有______种,其中一种被称为“PX”,它的一氯代物只有两种,则“PX”的结构简式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=2的A、B两种酸溶液各1 mL,分别加水稀释到1000 mL,其中pH与溶液体积V的关系如图所示。下列说法正确的是( )
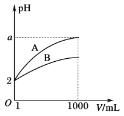
A. A、B两酸溶液的物质的量浓度一定相等
B. 稀释后,A酸溶液的酸性比B酸溶液强
C. a=5时,A是强酸,B是弱酸
D. 若a小于5,则A、B都是弱酸,且A的酸性弱于B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 等质量的 D2O和H2O中含有的质子数相同
B. 过氧化钠与水反应时,生成0.1 mol氧气转移的电子数为0.2NA
C. 2 L 0.5 mol·L-1亚硫酸溶液中含有的H+离子数为2NA
D. 密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,容器甲内充入0.1 mol NO气体。干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由D处向左移动,当移至C处时容器体积缩至最小,为原体积9/10,干燥管中物质的质量增加了2.24 g。随着CO2的继续通入,活塞又逐渐向右移动。下列说法中正确的是
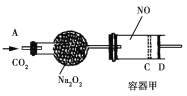
A. 活塞从D处移动到C处的过程中,通入的CO2气体为2.24 L(标准状况)
B. NO2转化为N2O4的转化率为20%
C. 容器甲中NO已反应完
D. 活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处,则a小于0.01
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学学习小组用酸性KMnO4溶液与H2C2O4(K1 = 5.4 × 10-2)的反应(此反应为放热反应)进行如下实验:
Ⅰ、探究“条件对化学反应速率的影响”,并设计了如下的方案记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 molL-1 H2C2O4溶液、0.010 molL-1 KMnO4 溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
物理量 | V(H2C2O4溶液)/mL | V(蒸馏水)/mL | V(KMnO4溶液)/mL | T/℃ | 乙 |
① | 2.0 | 0 | 4.0 | 50 | |
② | 2.0 | 0 | 4.0 | 25 | |
③ | 2.0 | a | 4.0 | 25 |
(1)完成该反应的实验原理: + MnO4- + = CO2↑ + Mn2+ + H2O_______________
(2)上述实验①、②是探究___________对化学反应速率的影响;若上述实验②、③是探究浓度对化学反应速率的影响,则 a 为___________;乙是实验需要测量的物理量,则表格中“乙”应填写_______________。
Ⅱ、测定H2C2O4xH2O中x值。已知:M(H2C2O4) = 90 gmol-1。①称取1.260 g 纯草酸晶体,将草酸制成 100.00 mL 水溶液为待测液; ②取 25.00 mL 待测液放入锥形瓶中,再加入适量的稀 H2SO4; ③用浓度为 0.05 000 molL-1的KMnO4标准溶液进行滴定。
(1)某学生的滴定方式(夹持部分略去)如下,最合理的是________(选填 a、b)。由图可知消耗 KMnO4 溶液体积为________ mL。

(2)滴定终点锥形瓶内现象为__________________________________________________。
(3)通过上述数据,求得 x =______________。
(4)下列操作会造成所测x偏大的是____________(填字母)。
A.滴定终点俯视读数
B.锥形瓶用待测溶液润洗
C.滴定前有气泡,滴定后没有气泡
D.配制100 mL待测溶液时,有少量溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和 铜片中无杂质,气体体积已转换为标准状况。下列说法正确的是 ( )
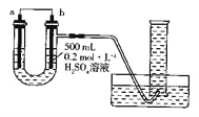
A. a 电极的电极材料是铜
B. 如果将稀硫酸换为 CuSO4 溶液,则不能达到实验目的
C. 锌与稀硫酸反应时放出的热量对实验测定不产生影响
D. 若量筒中收集到 a L H2,则电解质溶液中通过了![]() mol 电子
mol 电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解AgNO3溶液一段时间后,下列有关说法正确的是( )
A. 阳极质量增加
B. 向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况
C. 电解过程中溶液的pH不断升高
D. 电解后两极产生的气体体积比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种金黄色易挥发的液体,人们使用它作橡胶硫化剂,使橡胶硫化,改变生橡胶热发粘冷变硬的不良性能。在熔融的硫中通以氯气即可生成
是一种金黄色易挥发的液体,人们使用它作橡胶硫化剂,使橡胶硫化,改变生橡胶热发粘冷变硬的不良性能。在熔融的硫中通以氯气即可生成![]() 。有关物质的部分性质如下:
。有关物质的部分性质如下:
物质 | 熔点/ | 沸点/ | 化学性质 |
|
|
| 略 |
|
|
| 遇水生成
|
下图是实验室用![]() 和
和![]() 制备
制备![]() 的装置(夹持装置、加热装置均已略去)。
的装置(夹持装置、加热装置均已略去)。

(1)实验室中制备氯气,可以选用如下________(选填字母)装置。

(2)装置![]() 中应放试剂为___________________;装置
中应放试剂为___________________;装置![]() 的名称是__________________。图中
的名称是__________________。图中![]() 装置中应放置的试剂为______________________,其作用为________________________。
装置中应放置的试剂为______________________,其作用为________________________。
(3)该实验的操作顺序应为_____________________________________(用序号表示)。
①加热装置![]() ②通入
②通入![]() ③通冷凝水 ④停止通
③通冷凝水 ④停止通![]() ⑤停止加热装置
⑤停止加热装置![]()
(4)![]() 粗品中可能混有的杂质是(填写两种)_____________、____________,
粗品中可能混有的杂质是(填写两种)_____________、____________,![]() 粗品可以用___方法(填操作名称)进行提纯。
粗品可以用___方法(填操作名称)进行提纯。
(5)对提纯后的产品进行粗略测定。取![]() 产品,加入
产品,加入![]() 水充分反应(假设
水充分反应(假设![]() 全部逸出),过滤,洗涤沉淀并将洗涤液与滤液合并,用
全部逸出),过滤,洗涤沉淀并将洗涤液与滤液合并,用![]() 容量瓶定容,取
容量瓶定容,取![]() 溶液用浓度为
溶液用浓度为![]() 的硝酸银溶液滴定,三次测定结果如下:
的硝酸银溶液滴定,三次测定结果如下:
1 | 2 | 3 |
|
|
|
则产品中氯元素的质量分数为________(用含有![]() 的式子表示)。若锥形瓶用待测液润洗,对滴定结果的影响是__________(选填“偏大”、“偏小”或“不变”)。
的式子表示)。若锥形瓶用待测液润洗,对滴定结果的影响是__________(选填“偏大”、“偏小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com