
在一定温度下,已知有关某溶液的一些数据:①溶液的质量,②溶剂的质量,③溶液的体积,④溶质的摩尔质量,⑤溶质(气体)的体积(Vm已知),⑥溶液的密度,⑦溶液的质量分数.利用下列各组数据计算该溶液的物质的量浓度,不能算出的一组
A.③⑤ B.①④⑥ C.①④⑥⑦ D.①②③④
科目:高中化学 来源: 题型:
以NA表示阿伏伽德罗常数,下列说法中正确的是
A.58.5g氯化钠固体中含有NA个氯化钠分子
B.5.6 g铁粉与酸反应失去的电子数一定为0.2NA
C.6.0g金刚石中含有的共价键数为NA
D.标况下,11.2LSO3所含的分子数为0.5NA
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是( )

| 选项 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液变红 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液褪色 | Cl2具有酸性 |
| C | 紫色石蕊溶液先变红后褪色 | Cl2具有漂白性 |
| D | KI淀粉溶液变蓝色 | Cl2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
锌锰干电池由于其贮存和使用寿命较短,大都为一次性电池,用完之后被当作垃圾扔掉。这不仅浪费了宝贵的金属资源,而且还会产生严重的环境污染。下表是各类电池的综合成分分析结果:
| 元素 | 锌 | 锰 | 铁 | 铜 | 碳 | 其它 |
| 质量百分含量 | 13~27 | 14~28 | 23~26 | 0.5~0.7 | 5~6 | 13 |
通过简单的机械处理,将电池中各组分进行最大在限度的分离,从而使整个处理过程得到简化。再分别对锌皮和锰粉(MnO2)进行湿法处理,通过预处理、浸取、净化等工序制出产品。工艺流程如下图:
查阅资料知各离子沉淀完全的pH为
| 离子 | Fe3+ | Fe2+ | Cu2+ | Mn2+ |
| pH | 3.2 | 9.0 | 6.7 | 10.1 |
已知:锌元素与铝元素相似,具有两性。

1、市售锌锰干电池为碱性电池,电解质溶液为KOH,则其正极反应为 ;
电极总反应方程为 ;
2、在预处理中,分离铁皮和锌皮的方法是 ,洗液加(NH4)2CO3在pH=7.5沉淀出一种碱式盐,该物质的化学式为 。
3、二氧化锰生产中,写出加入30%盐酸溶解时的离子方程式 ;盐酸溶解后回收的渣是 ;
4、已知第二次加H2O2后调节pH≈9的目的为将Mn2+转化为MnO2,则第一次加H2O2后调节pH≈5,目的是 ;
5、实验室中用高锰酸钾溶液检验Mn2+时,产生黑色沉淀,该反应的离子方程式为
;
硫酸锰在高温条件下可以得到三种氧化物,该热分解的方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某稀有气体的相对分子质量为Mr,N表示阿伏加德罗常数的值,在一定的温度和压强下,体积为VL的该气体所含有的原子数为X.则 表示的是 ( )
表示的是 ( )
A.以g为单位 L该气体的质量 B.以g为单位1L该气体的质量
L该气体的质量 B.以g为单位1L该气体的质量
C.1L该气体中所含的分子数 D.以L为单位1mol该气体的体积
查看答案和解析>>
科目:高中化学 来源: 题型:
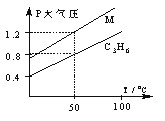
右图中两条曲线分别表示1g C3H6、1g M气体在相同体积
的容器中压强和温度的关系,试根据图判断M气体可能是
A.C3H4 B.CO2 C. CO D.H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)向NaHSO4溶液中逐滴加入Ba(OH)2溶液使SO42-恰好沉淀完全,请写出发生反应的离子方程式:______ 。
(2)在一定条件下,RO4n--和I-发生反应的离子方程式如下:
RO4n- +8I- +8H+=== R- +4I2 +4H2O中R元素的化合价为 .
(3)常温常压下,将CO与CH4的混合气体10L与25L氧气混合,点燃后充分反应,则剩余气体为24L(恢复为常温常压),则原来混合气体中CO与CH4的体积比为 。
(4)以物质的量之比为1:2相混合的Na2SO3和K2SO3的混合物共a g,与足量盐酸反应生成的SO2物质的量n(SO2)= mol(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
用一氧化碳在加热的条件下还原氧化铜,发现已制得的铜又很快变黑了,你推测产生这种现象的原因是( )
A. 温度太低
B. 试管口倾斜了
C. 反应开始时,没有把试管内的空气排干净
D. 铜没有在一氧化碳气流中冷却而又被空气中氧气所氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
在CO和CO2的混合气体中,含氧64%,将该混合气体10g通过足量的灼热的氧化铜,使其充分反应。求:(1)共得到多少克二氧化碳?(2)有多少克氧化铜被还原?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com