
下列关于水的离子积常数的叙述中,正确的是( )
A.因为水的离子积常数的表达式是KW=[H+][OH-],所以KW随溶液中H+和OH-浓度的变化而变化
B.水的离子积常数KW与水的电离平衡常数K是同一个物理量
C.水的离子积常数仅仅是温度的函数,随着温度的变化而变化
D.水的离子积常数KW与水的电离平衡常数K是两个没有任何关系的物理量
科目:高中化学 来源: 题型:
向一定量的Cu、Fe2O3的混合物中加入300 mL 1 mol/L的HCl溶液,恰好使混合物完全溶解,
 所得溶液中加入KSCN溶液后无红色出现,若用过量的CO在高温下还原相同质量的此混合物,固体的质
所得溶液中加入KSCN溶液后无红色出现,若用过量的CO在高温下还原相同质量的此混合物,固体的质
量减少了 ( )
A.6.4 g B.4.8 g C.2.4 g D.1.6 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下某无色混合气体可能由CH4、NH3 、H
、H 2、CO、CO2和HCl中的某几种气体组成。在恒温恒压条件下,将此混合气体通过浓H2SO4时,总体积基本不变;通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减少,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使CuSO4粉末变色。则原混合气体的成分是
2、CO、CO2和HCl中的某几种气体组成。在恒温恒压条件下,将此混合气体通过浓H2SO4时,总体积基本不变;通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减少,把剩余气体导出后,在O2中能够点燃,燃烧产物不能使CuSO4粉末变色。则原混合气体的成分是
A.CH4和NH3 B.HCl、H2和CO
C.HCl和CO  D.HCl、CO和CO2
D.HCl、CO和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z三种元素,已知:①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈 紫色。
紫色。
请回答:
(1)Y的最高价氧化物对应水化物的化学式是________。
(2)将ZY3溶液滴入沸水可得到红褐色液体,反应的离子方程式是_____________,此液体具有的性质是________(填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
(3)X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1 mol该气体被O2氧化放热98.0 kJ。若2 mol该气体与1 mol O2在此条件下发生反应,达到平衡时放出的热量是176.4 kJ,则该气体的转化率为____________。
②原无色有刺激性气味的气体与含1.5 mol Y的一种含氧酸该酸的某盐常用于实验室制取氧气的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转 移时,该反应的化学方程式是_______________。
移时,该反应的化学方程式是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式书写错误的是( )
A.NH3·H2O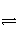
 NH
NH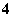 +OH-
+OH-
B.Ba(OH)2===Ba2++2OH-
C.H2SO4===2H++SO
D.NaHCO3===Na++H++CO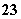
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.精炼铜时粗铜作阴极,纯铜作阳极
B.工业上利用电解饱和AlCl3溶液的方法生产金属铝
C.氯碱工业和金属钠的冶炼都用到了NaCl,阳极反应都是2Cl--2e-====Cl2↑
D.钢铁的腐蚀通常为电化学腐蚀,该腐蚀过程中负极反应为Fe-3e-====Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
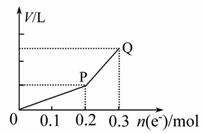 用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体的总体积的关系如下图所示(气体体积均在相同状况下测定),欲使电解质溶液恢复到起始状态,应向溶液中加入( )
用惰性电极电解硫酸铜溶液,整个过程转移电子的物质的量与产生气体的总体积的关系如下图所示(气体体积均在相同状况下测定),欲使电解质溶液恢复到起始状态,应向溶液中加入( )
A.0.1 mol CuO
B.0.1 mol CuCO3
C.0.1 mol Cu(OH)2
D.0.05 mol Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
下表的实验数据是在不同温度和压强下,平衡混合物中NH3含量的变化情况。达到平衡时平衡混合物中NH3的含量(体积分数)[入料V(N2)∶V(H2)=1∶3]
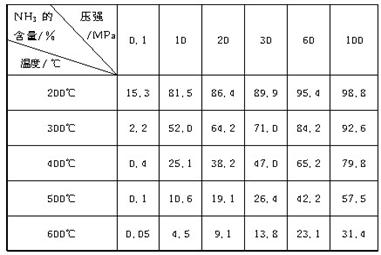
(1)比较200℃和300℃时的数据,可判断升高温度,平衡向____________方向移动,正反应方向为________(填“吸热”或“放热”)反应。
(2)根据平衡移动原理,合成氨适宜的条件是________。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(3)计算500℃,30 MPa时N2的转化率________。
(4)实际工业生产合成氨时,考虑浓度对化学平衡的影响,还采取了一些措施。请写出其中的一个措施:________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时,将2个铜电极插入到一定的Na2SO4饱和溶液中,通直流电电解并不断搅拌,当阴极上收集到a mol气体时,溶液中析出了b mol的结晶水合物Na2SO4·10H2O,若保持温度不变,则所剩溶液中溶质的质量分数是( )
A.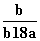 B.
B.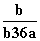 C.
C.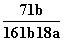 D.
D.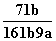
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com