
| A、盐酸溶液中的c(Cl-)与醋酸溶液中的c(CH3COO-)相等 |
| B、它们与NaOH完全中和时,醋酸溶液所消耗的NaOH多 |
| C、它们分别与足量CaCO3反应时,放出的CO2一样多 |
| D、分别用水稀释相同倍数时,n(Cl-)<n(CH3COO-) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、① | B、② | C、④ | D、③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁有良好的导热性,常用来制作炊具 |
| B、铜的化学性质不活泼,在潮湿的空气中不会生锈 |
| C、废旧电池中汞的回收可减少对环境的污染 |
| D、铝表面易形成致密的氧化膜可阻止铝进一步被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、无水乙醇:a=b |
| B、石灰水:a>b |
| C、NaHSO4溶液:a>b |
| D、盐酸:a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
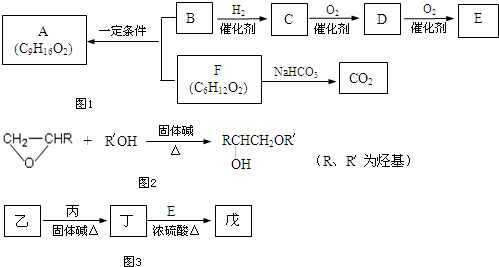
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、②③ | C、③④ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化合物 | 相对分子质量 | 密度/g?cm-3 | 沸点,/℃ | 溶解度/l00g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |

查看答案和解析>>
科目:高中化学 来源: 题型:
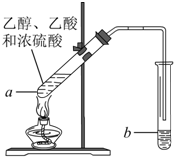 在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
在实验室可以用如图所示的装置制取乙酸乙酯,请回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com