
”¾ĢāÄæ”æĮņ¼°Ęä»ÆŗĻĪļÓŠŠķ¶ąÓĆĶ¾£¬Ļą¹ŲĪļÖŹµÄĪļĄķ³£ŹżČē±ķĖłŹ¾£ŗ
H2S | S8 | FeS2 | SO2 | SO3 | H2SO4 | |
ČŪµć/”ę | -85.5 | 115.2 | >600(·Ö½ā) | -75.5 | 16.8 | 10.3 |
·Šµć/”ę | -60.3 | 444.6 | -10.0 | 45.0 | 337.0 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©»łĢ¬SŌ×Óµē×ÓÕ¼¾Ż×īøßÄܼ¶µÄµē×ÓŌĘĀÖĄŖĶ¼ĪŖ___ŠĪ”£
£Ø2£©øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ£¬H2S”¢SO2”¢SO3µÄĘųĢ¬·Ö×ÓÖŠ£¬ÖŠŠÄŌ×Ó¼Ū²ćµē×Ó¶ŌŹż²»Ķ¬ĘäĖū·Ö×ӵďĒ__”£
£Ø3£©Ķ¼(a)ĪŖS8µÄ½į¹¹£¬ĘäĮņŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ___”£
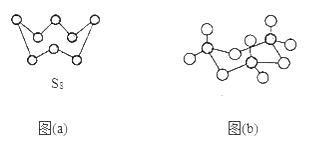
£Ø4£©ĘųĢ¬ČżŃõ»ÆĮņŅŌµ„·Ö×ÓŠĪŹ½“ęŌŚ£¬Ęä·Ö×ÓµÄĮ¢Ģå¹¹ŠĶĪŖ___ŠĪ£»¹ĢĢåČżŃõ»ÆĮņÖŠ“ęŌŚČēĶ¼(b)ĖłŹ¾µÄČż¾Ū·Ö×Ó£¬øĆ·Ö×ÓÖŠSŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖ__”£
”¾“š°ø”æŃĘĮåŠĪ H2S sp3 Ę½ĆęÕżČż½ĒŠĪ sp3
”¾½āĪö”æ
£Ø1£©»łĢ¬SŌ×Óµē×ÓÕ¼¾ŻµÄÄܼ¶ÓŠ1s”¢2s”¢2p”¢3s”¢3p£¬×īøßÄܼ¶ĪŖ3p£¬Ęäµē×ÓŌĘĀÖĄŖĶ¼ĪŖŃĘĮåŠĪ£»
£Ø2£©H2SÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=2+![]() =4”¢SO2ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=2+
=4”¢SO2ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=2+![]() =3”¢SO3ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=3+
=3”¢SO3ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=3+![]() =3£»
=3£»
£Ø3ČēĶ¼ĖłŹ¾£¬ĆæøöĮņŌ×ÓŠĪ³ÉĮ½øö¼ü£¬³É¼ü¶ŌŹżĪŖ2£¬ĮņŌ×ÓŗĖĶā×īĶā²ćÓŠ2¶Ō¹Āµē×Ó¶Ō£¬ŌņĮņŌ×Ó¼Ū²ćµē×Ó¶ŌŹż=2+2=4£»
£Ø4£©SO3ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=3+![]() =3£¬ĒŅ²»ŗ¬¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻĘäæռ乹ŠĶĪŖĘ½ĆęÕżČż½ĒŠĪ£»øĆ·Ö×ÓÖŠSOŌ×ÓÖ®¼ä“ęŌŚ¦ŅŗĶĄėÓņ“󦊼ü£¬ĖłŅŌ¹²¼Ū¼üĄąŠĶ2ÖÖ£»øĆ·Ö×ÓÖŠĆæøöSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż¶¼ŹĒ4£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻSŌ×ÓŌÓ»ÆĄąŠĶ”£
=3£¬ĒŅ²»ŗ¬¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻĘäæռ乹ŠĶĪŖĘ½ĆęÕżČż½ĒŠĪ£»øĆ·Ö×ÓÖŠSOŌ×ÓÖ®¼ä“ęŌŚ¦ŅŗĶĄėÓņ“󦊼ü£¬ĖłŅŌ¹²¼Ū¼üĄąŠĶ2ÖÖ£»øĆ·Ö×ÓÖŠĆæøöSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż¶¼ŹĒ4£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻSŌ×ÓŌÓ»ÆĄąŠĶ”£
£Ø1£©»łĢ¬SŌ×Óµē×ÓÕ¼¾ŻµÄÄܼ¶ÓŠ1s”¢2s”¢2p”¢3s”¢3p£¬×īøßÄܼ¶ĪŖ3p£¬Ęäµē×ÓŌĘĀÖĄŖĶ¼ĪŖŃĘĮåŠĪ£¬
“š°øĪŖ£ŗŃĘĮåŠĪ£»
£Ø2£©H2SÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=2+![]() =4”¢SO2ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=2+
=4”¢SO2ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=2+![]() =3”¢SO3ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=3+
=3”¢SO3ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=3+![]() =3£¬ÖŠŠÄŌ×Ó¼Ū²ćµē×Ó¶ŌŹż²»Ķ¬ÓŚĘäĖū·Ö×ӵďĒH2S£¬
=3£¬ÖŠŠÄŌ×Ó¼Ū²ćµē×Ó¶ŌŹż²»Ķ¬ÓŚĘäĖū·Ö×ӵďĒH2S£¬
“š°øĪŖ£ŗH2S£»
£Ø3£©ČēĶ¼ĖłŹ¾£¬ĆæøöĮņŌ×ÓŠĪ³ÉĮ½øö¼ü£¬³É¼ü¶ŌŹżĪŖ2£¬ĮņŌ×ÓŗĖĶā×īĶā²ćÓŠ2¶Ō¹Āµē×Ó¶Ō£¬ŌņĮņŌ×Ó¼Ū²ćµē×Ó¶ŌŹż=2+2=4£¬ĘäĮņŌ×ÓµÄŌӻƹģµĄĄąŠĶĪŖsp3£¬
“š°øĪŖ£ŗsp3£»
£Ø4£©SO3ÖŠSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż=3+![]() =3£¬ĒŅ²»ŗ¬¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻĘäæռ乹ŠĶĪŖĘ½ĆęÕżČż½ĒŠĪ£»øĆ·Ö×ÓÖŠSOŌ×ÓÖ®¼ä“ęŌŚ¦ŅŗĶĄėÓņ“󦊼ü£¬ĖłŅŌ¹²¼Ū¼üĄąŠĶ2ÖÖ£»øĆ·Ö×ÓÖŠĆæøöSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż¶¼ŹĒ4£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻSŌ×ÓŌÓ»ÆĄąŠĶĪŖsp3£¬
=3£¬ĒŅ²»ŗ¬¹Āµē×Ó¶Ō£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻĘäæռ乹ŠĶĪŖĘ½ĆęÕżČż½ĒŠĪ£»øĆ·Ö×ÓÖŠSOŌ×ÓÖ®¼ä“ęŌŚ¦ŅŗĶĄėÓņ“󦊼ü£¬ĖłŅŌ¹²¼Ū¼üĄąŠĶ2ÖÖ£»øĆ·Ö×ÓÖŠĆæøöSŌ×Ó¼Ū²ćµē×Ó¶ŌøöŹż¶¼ŹĒ4£¬øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪÅŠ¶ĻSŌ×ÓŌÓ»ÆĄąŠĶĪŖsp3£¬
“š°øĪŖ£ŗĘ½ĆęÕżČż½ĒŠĪ£»sp3£»


 ³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø
³å“Ģ100·Ö1ŗžķĻµĮŠ“š°ø ĘŚÄ©ŗĆ³É¼ØĻµĮŠ“š°ø
ĘŚÄ©ŗĆ³É¼ØĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøßĪĀĻĀ£¬³¬Ńõ»Æ¼Ų¾§Ģå³ŹĮ¢·½Ģå½į¹¹£¬¾§ĢåÖŠŃõµÄ»ÆŗĻ¼Ū²æ·ÖĪŖ0¼Ū£¬²æ·ÖĪŖ£2¼Ū”£ČēĶ¼ĖłŹ¾ĪŖ³¬Ńõ»Æ¼Ų¾§ĢåµÄŅ»øö¾§°ū£¬ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ

A£®³¬Ńõ»Æ¼ŲµÄ»ÆѧŹ½ĪŖKO2£¬Ćæøö¾§°ūŗ¬ÓŠ4øöK£«ŗĶ4øöO2-
B£®¾§ĢåÖŠĆæøöK£«ÖÜĪ§ÓŠ8øöO2-£¬ĆæøöO2-ÖÜĪ§ÓŠ8øöK£«
C£®¾§ĢåÖŠÓėĆæøöK£«¾ąĄė×ī½üµÄK£«ÓŠ8øö
D£®¾§ĢåÖŠÓėĆæøöK£«¾ąĄė×ī½üµÄK£«ÓŠ6øö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijČÜŅŗÖŠæÉÄÜŗ¬ÓŠH+”¢NH4+”¢Mg2+”¢Al3+”¢Fe3+”¢CO32£”¢SO42£”¢NO3£ÖŠµÄ¼øÖÖ”£¢ŁČō¼ÓČėŠæĮ££¬²śÉśĪŽÉ«ĪŽĪ¶µÄĘųĢ壻¢ŚČō¼ÓČėNaOHČÜŅŗ£¬²śÉś°×É«³Įµķ£¬ĒŅ²śÉśµÄ³ĮµķĮæÓė¼ÓČėNaOHµÄĪļÖŹµÄĮæÖ®¼äµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ŌņĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. ČÜŅŗÖŠŅ»¶Ø²»ŗ¬CO32©£¬æÉÄÜŗ¬ÓŠSO42£ŗĶNO3£
B. ČÜŅŗÖŠn(NH4+)="0.2" mol
C. ČÜŅŗÖŠµÄŃōĄė×ÓÖ»ÓŠH+”¢Mg2+”¢Al3+
D. n(H+)©Un(Al3+)©Un(Mg2+)=1©U1©U1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ7000CŹ±£¬ĻņČŻ»żĪŖ2LµÄĆܱÕČŻĘ÷ÖŠ³äČėŅ»¶ØĮæµÄCOŗĶH2O£¬·¢Éś·“Ó¦£ŗCO(g)+H2O(g)![]() CO2(g)+H2(g)£»·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ(±ķÖŠt2£¾t1)
CO2(g)+H2(g)£»·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ(±ķÖŠt2£¾t1)
·“Ó¦Ź±¼ä/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.80 | |
t2 | 0.20 |
ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
A.·“Ó¦ŌŚt1minÄŚµÄĘ½¾łĖŁĀŹĪŖ¦Ō(CO2)=![]() mol”¤L-1”¤min-1
mol”¤L-1”¤min-1
B.µ½t1minŹ±£¬·“Ó¦Ī““ļĘ½ŗāדĢ¬
C.±£³Ö7000C²»±ä£¬ĻņĘ½ŗāĢåĻµÖŠŌŁĶØČė0.60molCOŗĶ0.30 molH2O£¬“ļµ½ŠĀĘ½ŗāŹ±ÓėŌĘ½ŗāĻą±Č£¬CO×Ŗ»ÆĀŹŌö“ó£¬H2µÄĢå»ż·ÖŹżŌö“ó
D.ĪĀ¶ČÉżÖĮ8000CŹ±£¬ÉĻŹö·“Ó¦µÄĘ½ŗā³£ŹżĪŖ0.64£¬ŌņÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠ”×éĶ¬Ń§ÓūŌŚŹµŃéŹŅÖŠÓĆŅŅ“¼Öʱø1£¬2-¶žäåŅŅĶ锣
¼×Ķ¬Ń§Éč¼ĘµÄŹµŃé×°ÖĆČēĻĀĶ¼£ŗ
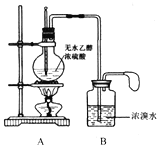
£Ø1£©ĒėŠ“³öAŗĶBÖŠ·¢ÉśµÄÖ÷ŅŖ·“Ó¦µÄ»Æѧ·½³ĢŹ½
A£ŗ________________________________________”£
B£ŗ________________________________________”£
£Ø2£©ŅŅĶ¬Ń§²éŌÄ׏ĮĻµĆÖŖ£ŗ
¢Ł“Ė·“Ó¦æÉÄÜ“ęŌŚµÄÖ÷ŅŖø±·“Ó¦ÓŠ£ŗŌŚÅØĮņĖįµÄ“ęŌŚĻĀ£¬ŅŅ“¼æÉ·¢ÉśČēĻĀ·“Ӧɜ³ÉŅŅĆŃ£¬ ![]()
¢ŚŅŅĆŃ²»ÓėäåĖ®·“Ó¦
ÓŠ¹ŲŹż¾ŻĮŠ±ķČēĻĀ£ŗ
ŅŅ“¼ | 1£¬2-¶žäåŅŅĶé | ŅŅĆŃ | |
ŃÕÉ«”¢×“Ģ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå |
·Šµć/”ę | 78.5 | 132 | 34.6 |
Čō×īÖÕ²śĪļÖŠ»ģÓŠÉŁĮæŅŅĆŃ£¬æÉÓĆ__________µÄ·½·Ø³żČ„”£
£Ø3£©±ūĶ¬Ń§¹Ū²ģµ½£ŗŌŚŹµŃéŗóĘŚAÖŠŅŗĢå±äŗŚ£¬ČĻĪŖÓ¦øĆŌŚ×°ÖĆAŗĶBÖ®¼ä¼ÓČė×°ÖĆ__________£ØĢīŠņŗÅ£©£¬“Ė×°ÖƵÄ×÷ÓĆŹĒ____________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓĆNA±ķŹ¾°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÖŠÕżČ·µÄŹĒ
A. l00g 9%µÄĘĻĢŃĢĒĖ®ČÜŅŗÖŠŃõŌ×ÓŹżĪŖ0.3 NA
B. ±ź×¼×“æöĻĀ£¬2.24L F2ĶØČė×ćĮ汄ŗĶŹ³ŃĪĖ®ÖŠæÉÖĆ»»³ö0.1NAøöCl2
C. ¹¤ŅµŗĻ³É°±Ćæ¶ĻĮŃNAøöN”ŌN¼ü£¬Ķ¬Ź±¶ĻĮŃ6NAøöN-H¼ü£¬Ōņ·“Ó¦“ļµ½Ę½ŗā
D. ³£ĪĀĻĀl LpH=7µÄ1mol/LCH3COONH4ČÜŅŗÖŠCH3COO-ÓėNH4+ŹżÄæ¾łĪŖNA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻąĶ¬ĪĀ¶ČĻĀ£¬Ģå»żĪŖ2LµÄĮ½øöŗćČŻČŻĘ÷ÖŠ·¢Éś£ŗ![]() ¾łĪŖĘųĢ¬ĪļÖŹ
¾łĪŖĘųĢ¬ĪļÖŹ![]() ÓŠĻĀ±ķĖłŹ¾ŹµŃ鏿¾Ż£ŗ
ÓŠĻĀ±ķĖłŹ¾ŹµŃ鏿¾Ż£ŗ
ČŻĘ÷±ąŗÅ | ĘšŹ¼Ź±ø÷ĪļÖŹµÄĪļÖŹµÄĮæ | “ļµ½Ę½ŗāŹ±ĢåĻµÄÜĮæµÄ±ä»Æ | ||
|
|
| ||
¢Ł | 1 | 3 | 0 |
|
¢Ś | 0 | 0 | 2 |
|
¢Ū |
|
|
|
|
ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ
A.![]()
B.¢ŚÖŠ![]() µÄ×Ŗ»ÆĀŹ“óÓŚ¢ŪÖŠ
µÄ×Ŗ»ÆĀŹ“óÓŚ¢ŪÖŠ![]() µÄ×Ŗ»ÆĀŹ
µÄ×Ŗ»ÆĀŹ
C.ČŻĘ÷¢ŁÓė¢Ū·Ö±š“ļµ½Ę½ŗāŹ±£¬Ę½ŗā³£ŹżĻąĶ¬£¬ĒŅ![]()
D.½«ČŻĘ÷¢ŁµÄ·“Ó¦Ģõ¼ž»»ĪŖŗćĪĀŗćŃ¹ÖŠ½ųŠŠ![]() Ķ¶ĮĻĮæ²»±ä
Ķ¶ĮĻĮæ²»±ä![]() £¬“ļµ½Ę½ŗāŹ±£¬ĘųĢåĘ½¾łÄ¦¶ūÖŹĮæ½ĻŗćĪĀŗćČŻŹ±¼õŠ”ĮĖ
£¬“ļµ½Ę½ŗāŹ±£¬ĘųĢåĘ½¾łÄ¦¶ūÖŹĮæ½ĻŗćĪĀŗćČŻŹ±¼õŠ”ĮĖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬ŌŚČżøöĢå»ż¾łĪŖ![]() ŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ
ŗćČŻĆܱÕČŻĘ÷ÖŠ·¢Éś·“Ó¦£ŗ
![]()
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ![]()
“°æŚ±ąŗÅ | ĪĀ¶Č | ĘšŹ¼ĪļÖŹµÄĮæ | Ę½ŗāĪļÖŹµÄĮæ | |
|
|
| ||
1 | 380 |
|
|
|
2 | 380 |
| ||
3 | 230 |
|
|
|
A.øĆ·“Ó¦µÄÕż·“Ó¦ĪŖ·ÅČČ·“Ó¦
B.“ļµ½Ę½ŗāŹ±£¬ČŻĘ÷1ÖŠµÄ![]() Ģå»ż·ÖŹż±ČČŻĘ÷2ÖŠµÄŠ”
Ģå»ż·ÖŹż±ČČŻĘ÷2ÖŠµÄŠ”
C.ČŻĘ÷1ÖŠ·“Ó¦“ļµ½Ę½ŗāĖłŠčµÄŹ±¼ä±ČČŻĘ÷3ÖŠµÄ³¤
D.ČōĘšŹ¼Ź±ĻņČŻĘ÷¢óÖŠ³äČė![]()
![]()
![]() Ӣ
Ӣ![]()
![]()
![]() ŗĶ
ŗĶ![]()
![]() £¬Ōņ·“Ó¦ĻņÄę·“Ó¦·½Ļņ½ųŠŠ
£¬Ōņ·“Ó¦ĻņÄę·“Ó¦·½Ļņ½ųŠŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ×ćĮæĶÓėŅ»¶ØĮæÅØĻõĖį·“Ó¦µĆµ½ĻõĖįĶČÜŅŗŗĶ NO2”¢N2O4”¢NO µÄ»ģŗĻĘųĢ壬ÕāŠ©ĘųĢåÓė 4.48 L O2£Ø±ź×¼×“æö£©»ģŗĻŗóĶØČėĖ®ÖŠ£¬ĘųĢåĒ”ŗĆĶźČ«±»Ė®ĪüŹÕÉś³ÉĻõĖį”£ČōĻņĖłµĆĻõĖįĶČÜŅŗÖŠ¼ÓČė 400 mL NaOHČÜŅŗ£¬“ĖŹ± Cu2+Ē”ŗĆ³ĮµķĶźČ«£¬ĖłÓĆ NaOH ČÜŅŗµÄÅØ¶ČŹĒ£Ø £©
A.2 mol/LB.4 mol/LC.6 mol/LD.0.8 mol/L
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com