
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
分析 (1)根据电离平衡常数的表达式解答;
(2)根据亚硫酸和碳酸的K1比较二者的酸性强弱;H2SO3和H2CO3均属于二元酸,要想通过比较二者的pH来验证二者的酸性强弱,必需使二者的浓度相同,但是SO2和CO2气体溶于水后的饱和溶液其浓度显然不相等(因为二者的溶解度不同);
(3)利用强酸制取弱酸的原理设计实验.
解答 解:(1)亚硫酸氢根离子的电离平衡常数为:K=$\frac{c(S{{O}_{3}}^{2-})•c({H}^{+})}{c(HS{{O}_{3}}^{-})}$,
故答案为:$\frac{c(S{{O}_{3}}^{2-})•c({H}^{+})}{c(HS{{O}_{3}}^{-})}$;
(2)根据表中数据可知,亚硫酸的K1可以碳酸的K1,则亚硫酸的酸性大于碳酸;
H2SO3和H2CO3均属于二元酸,要想通过比较二者的pH来验证二者的酸性强弱,必需使二者的浓度相同,但是SO2和CO2气体溶于水后的饱和溶液其浓度显然不相等(因为二者的溶解度不同),所以该实验设计不正确,
故答案为:大于;用于比较pH的两种溶液的物质的量浓度不相等;
(3)亚硫酸的酸性大于大于碳酸,将碳酸钠溶液滴入亚硫酸溶液中会生成无色无味的二氧化碳气体,据此可证明二者酸性大小,
故答案为:向盛有亚硫酸溶液的试管中滴加碳酸钠溶液;试管中有无色无味的气体产生.
点评 本题考查了弱电解质的电离平衡及其影响,题目难度中等,注意掌握电力平衡常数的表达式、酸性强弱的判断方法,试题培养了学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 热的浓盐酸可以除去烧瓶内残留的MnO2 | |
| B. | 过量的铜与浓硝酸反应会有一氧化氮生成 | |
| C. | 稀硝酸可除去试管内壁的银镜 | |
| D. | 白磷在空气中加热到一定温度能转化成红磷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过滤 | B. | 分液 | C. | 萃取 | D. | 蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=1.5 mol•L-1•s-1 | B. | v(C)=0.5 mol•L-1•s-1 | ||
| C. | v(D)=0.6 mol•L-1•s-1 | D. | v(B)=0.4 mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
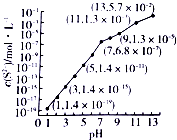 研究硫元素及其化合物的性质具有重要意义.
研究硫元素及其化合物的性质具有重要意义.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol/L的(NH4)2SO4溶液中:c (SO42-)>c (NH4+ )>c (H+)>c (OH-) | |
| B. | 0.2 mol/L的Na2CO3溶液中:c (OH-)=c (HCO3-)+c (H+)+c (H2CO3) | |
| C. | 0.1 mol/L的NH4Cl溶液与0.05 mol•L-1的NaOH溶液等体积混合,其混合溶液中:c (Cl-)>c (NH4+ )>c (Na+ )>c (H+)>c (OH-) | |
| D. | c (NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4C1溶液中:c[(NH4)2SO4]<c[(NH4)2CO3]<c (NH4C1) 第Ⅱ卷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | △H=-484kJ/mol | B. | △H=+484kJ/mol | C. | 吸收484kJ 能量 | D. | 放出484kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molCH3+(甲基正离子)中含有电子数为10NA | |
| B. | 1mol-CH3(甲基)中含有电子数为10NA | |
| C. | 1mol-OH(羟基)与1molOH-所含有电子数相同,均为10NA | |
| D. | 1.8gNH4+中含有的电子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com