
【题目】对Na2C2O4溶液进行研究,下列说法不正确的是(室温下0.1mol· L—1H2C2O4的pH=1.3)
A.Na2C2O4溶液中离子关系:c(C2O42-)+ c(HC2O4-)+ c(H2C2O4) = c (Na+)
B.向Na2C2O4溶液中加入酚酞,溶液变红:C2O42-+H2O![]() HC2O4-+OH-
HC2O4-+OH-
C.向Na2C2O4溶液中加入酸性高锰酸钾溶液,紫色褪去:2MnO4 -+ 5C2O42-+16 H += 2Mn 2+ +10CO2↑+8 H2O
D.向Na2C2O4溶液中加入足量稀硫酸制备草酸:C2O42-+2H+= H2 C2O4
【答案】A
【解析】
A.该溶液中存在物料守恒式为2[c(C2O42-)+c(HC2O4-)+c(H2C2O4)]═c(Na+),故A错误;
B.酚酞变红色,说明溶液呈碱性,草酸根离子水解导致溶液呈碱性,水解方程式为C2O42-+H2OHC2O4-+OH-,故B正确;
C.向草酸钠溶液中加入酸性高锰酸钾溶液紫色褪去,二者发生氧化还原反应生成锰离子、二氧化碳和水,离子方程式为2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O,故C正确;
D.向草酸钠溶液中加入足量稀硫酸生成草酸,二者发生复分解反应,离子方程式为C2O42-+2H+═H2C2O4,故D正确;
故选:A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】 常温下,向20 mL 0.01mol/L CH3COOH溶液中逐滴加入0.01mol/L 的NaOH溶液,溶液中水所电离出的c(H+)随加入NaOH溶液的体积变化示意图如图所示,下列说法不正确的是
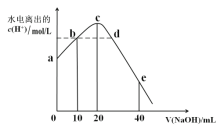
A.从a到c,醋酸的电离始终受到促进
B.a、d对应的纵坐标数值分别是:>10-12、>10-7
C.b点:2c(Na+)=c(CH3COO-)+c(CH3COOH)
D.从b→c的过程中,既存在着pH=7的点,也存在着溶液中水所电离出的c(H+)=10-7的点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 铅蓄电池充电时,阳极质量增大
B. 0.1mol ·L-lCH3COONa溶液加热后,溶液的pH减小
C. 标准状况下,11.2L苯中含有的碳原子数为3×6.02×1023
D. 室温下,稀释0.1mol·L-1氨水,c(H+)·c(NH3·H2O)的值减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.常温下,![]() 的碱性溶液中不可能存在
的碱性溶液中不可能存在![]() 分子
分子
B.常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
C.![]() 溶液加水稀释,溶液的pH和
溶液加水稀释,溶液的pH和![]() 的电离度均增大
的电离度均增大
D.将![]() 溶液滴入含酚酞的
溶液滴入含酚酞的![]() 溶液,红色褪去,说明
溶液,红色褪去,说明![]() 溶液显酸性
溶液显酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列表格中信息填写
有机物A | 有机物B | 有机物C | 有机物D |
1.该物质的产量是衡量一个国家石油化工水平的标志 2.比例模型: | 1.该物质为天然气的主要成分 2.比例模型: | 1.该物质由碳,氢,氧三种元素组成 2.75%的该物质的水溶液可做医用消毒剂 | 1.分子式为C2H4O2 2.该物质的水溶液显酸性,是家庭常用调味剂 |
(1)有机物A的结构简式为_________________,它与溴水反应的化学方程式为___________________。
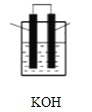
(2)有机物B的空间构型为_______________________将有机物B与氧气分别通入如图装置的两极组成燃料电池,该电池的负极反应为____________________________正极反应为_____________________________。
(3)有机物D在水溶液中的电离方程式为_______________________。 将pH=3的D溶液加水稀释10倍,所得溶液的pH_____4(填“大于”,“小于”),0.1molD与等量的NaOH溶液恰好完全反应的生成物显__________性(填“酸”或“碱”),该溶液中存在的电荷守恒关系式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L的密闭容器中充入2 molX(g)和1 mol Y(g),发生反应2X(g) +Y(g) ![]() 3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是

A.升高温度.平衡常数增大
B.W点Y的正反应速率等于M点Y的正反应速率
C.Q点时,Y的转化率最大
D.平衡时充入3molZ,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇 广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。
广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。
(1)能够跟1 mol该化合物起反应的Br2或H2的最大用量分别是________。
A.1 mol,1 mol
B.3.5 mol,7 mol
C.3.5 mol,6 mol
D.6 mol,7 mol
(2)下列不能与白藜芦醇反应的是________。
A.Na2CO3溶液
B.FeCl3溶液
C.NaHCO3溶液
D.酸性KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,用0. 100 mol·L—1盐酸滴定50. 0mL Na2CO3溶液(不考虑CO2从溶液中逸出).滴定曲线如图所示:
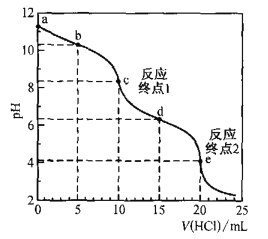
下列说法错误的是
A.a点溶液中:c(Na2CO3)=0.020 mol·L—1
B.b点溶液中:c(Na+)>c(HCO3— )>c(CO32—)
C.c点溶液中:c(Na+)+c(H+)=2c(CO32—) +c(HCO32—)+c(OH—)
D.室温时,H2CO3的一级电离平衡常数Kal的数量级为10—7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com