
分析 (1)反应生成硫酸钡和KCl;
(2)反应生成硝酸钠和水;
(3)反应生成硫酸铜和水;
(4)反应生成氯化钡、水、二氧化碳,结合离子反应中保留化学式的物质来解答.
解答 解:(1)BaCl2溶液与K2SO4溶液的反应生成硫酸钡和氯化钾,离子方程式为Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓;
(2)NaOH溶液与硝酸的反应生成硝酸钠和水,离子方程式为OH-+H+═H2O,故答案为:OH-+H+═H2O;
(3)氢氧化铜与硫酸反应生成硫酸铜和水,离子方程式为Cu(OH)2+2H+=Cu2++H2O,故答案为:Cu(OH)2+2H+=Cu2++H2O;
(4)碳酸钡难溶于水,与盐酸反应生成氯化钡和二氧化碳气体,反应的离子方程式为BaCO3+2H+═Ba2++H2O+CO2↑,
故答案为:BaCO3+2H+═Ba2++H2O+CO2↑.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电荷守恒,注重离子反应的综合训练,题目难度不大.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:实验题
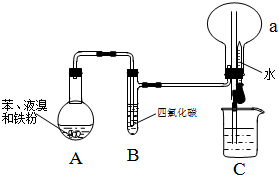 某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应.
某同学设计了如图所示的实验装置(夹持装置已略去)来研究苯和溴发生的反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油中含有1~50个碳原子的烷烃、环烷烃及芳香烃 | |
| B. | 石油通过催化裂化可以获得较多的轻质油 | |
| C. | 石油通过催化裂解可以获得烯烃 | |
| D. | 对石油催化重整是获得芳香烃的主要途径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4与Cl2光照 | B. | (CH3)2C=C(CH3)2和氯化氢加成 | ||
| C. | 氯乙烯加聚 | D. | CH3CHBrC2H5与NaOH的醇溶液共热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸氢钠溶液中滴加Ba(OH)2溶液恰好至中性:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O | |
| B. | 等物质的量浓度的FeI2溶液与溴水等体积混合:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| C. | 用惰性电极电解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+O2↑+4H+ | |
| D. | 硫氢化钠水解:HS-+H2O?H2S+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两个原子之间的相互作用叫化学键 | |
| B. | 共价化合物中只含有共价键 | |
| C. | 离子化合物中只含有离子键 | |
| D. | 完全由非金属元素形成的化合物一定是共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷消去制环己烯;由丙烯加溴制1,2-二溴丙烷 | |
| D. | 由乙酸和乙醇制乙酸乙酯;苯酚与浓溴水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用灼烧的方法可以区分蚕丝和人造纤维 | |
| B. | 食用油反复加热会产生稠环芳香烃等有害物质 | |
| C. | 医用消毒酒精中乙醇的浓度为95% | |
| D. | 加热能杀死流感病毒是因为蛋白质受热变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com