
【题目】石油裂解可获得A。已知A在通常状况下是一种相对分子量为28的气体,A通过加聚反应可以得到F,F常作为食品包装袋的材料。有机物A、B、C、D、E、F有如下图的关系。
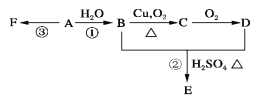
(1)A的分子式为________________。
(2)写出:反应①的化学方程式: ;该反应的类型是_______________。反应③的化学方程式:_____________________________________。
(3)G是E的同分异构体,且G能与NaHCO3反应,则G的可能结构简式分别为:
____________________________________________________________
(4)标况下,将A与某烃混合共11.2 L,该混合烃在足量的氧气中燃烧,生成CO2体积为17.92 L,生成H2O 18.0 g,则该烃的结构式为_____________;A与该烃的体积比为_____________。
【答案】(1)C2H4 (1分);
(2)CH2=CH2+H2O![]() CH3CH2OH(1分);加成反应(1分);
CH3CH2OH(1分);加成反应(1分);
nCH2=CH2→![]() (2分);
(2分);
(3)CH3CH2CH2COOH、(CH3)2CHCOOH(各1分);
(4)![]() (1分); 3∶2(2分);
(1分); 3∶2(2分);
【解析】
试题分析:石油裂解可获得A,A在通常状况下是一种相对分子量为28的气体,则A为CH2=CH2,A发生加聚反应生成F为![]() ,A与水发生加成反应生成B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,C进一步氧化生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成E为CH3COOCH2CH3,
,A与水发生加成反应生成B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,C进一步氧化生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成E为CH3COOCH2CH3,
(1)由上述分析可知,A为乙烯,分子式为C2H4,故答案为:C2H4;
(2)反应①是乙烯与水发生加成反应生成乙醇,反应化学方程式为:CH2=CH2+H2O ![]() CH3CH2OH,反应③是乙烯发生加聚反应生成聚乙烯,反应化学方程式为:nCH2=CH2
CH3CH2OH,反应③是乙烯发生加聚反应生成聚乙烯,反应化学方程式为:nCH2=CH2![]()
![]() ;(3)G是E(CH3COOCH2CH3)的同分异构体,且G能与NaHCO3反应,含有羧基,则G的可能结构简式分别为:CH3CH2CH2COOH、(CH3)2CHCOOH,故答案为:CH3CH2CH2COOH、(CH3)2CHCOOH;
;(3)G是E(CH3COOCH2CH3)的同分异构体,且G能与NaHCO3反应,含有羧基,则G的可能结构简式分别为:CH3CH2CH2COOH、(CH3)2CHCOOH,故答案为:CH3CH2CH2COOH、(CH3)2CHCOOH;
(4)标况下,将乙烯与某烃混合共11.2L,物质的量为11.2/22.4=0.5mol,燃烧生成CO2体积为17.92L,物质的量为17.92/22.4=0.8mol,生成H2O 18.0g,其物质的量为18/18=1mol,故平均分子式为C1.6H4,故另外的烃为甲烷,结构式为![]() ,令乙烯与甲烷的物质的量分别为xmol、ymol,则:(2x+y):(x+y)=1.6,整理得x:y=3:2,相同条件下,气体体积之比等于物质的量之比,故乙烯与甲烷的体积之比为3:2,故答案为:
,令乙烯与甲烷的物质的量分别为xmol、ymol,则:(2x+y):(x+y)=1.6,整理得x:y=3:2,相同条件下,气体体积之比等于物质的量之比,故乙烯与甲烷的体积之比为3:2,故答案为:![]() ;3:2.
;3:2.


 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源: 题型:
【题目】在浓度为0.01mol/L Mg(HCO3)2,0.02mol/LCaCl2的水溶液1L中,要同时除去Mg2+,Ca2+应选用的试剂是( )
A. NaHCO3 B. Na2CO3 C. Ca(OH)2 D. NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是实现科学探究的重要途径。
(1)下列关于教材实验的叙述中正确的是
A.Cu片加入冷的浓硫酸中没有变化,说明Cu在浓硫酸中也会钝化
B.石油分馏时,控制温度,收集到的汽油为纯净物
C.用激光笔照射肥皂水,有丁达尔效应,说明肥皂水是胶体
D.淀粉水解液中加入银氨溶液,水浴加热后无银镜,说明淀粉未水解
E.鸡蛋白溶液中分别加入饱和硫酸铵、硫酸钾溶液时,都发生了盐析
(2)某兴趣小组设计出下图装置(气密性已检查),验证铜与稀硝酸反应的产物。
已知:FeSO4+NO=[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
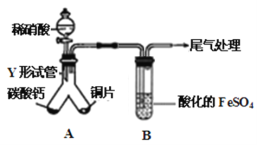
①实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 。
②由分液漏斗向Y形试管右侧加入稀硝酸,反应的离子方程式是
。
③本实验A生成的气体中,若有NO2,B的实验现象为 ;若只有NO生成,B的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A.氯化铝溶液中加入过量氨水:Al3++3NH3.H2O=Al(OH)3↓+3NH4+
B.碳酸钙和盐酸反应:CO32﹣+2H+=CO2↑+H2O
C.三氯化铁溶液与氢氧化钠溶液反应:FeCl3+3OH﹣=Fe(OH)3↓+3Cl﹣
D.铜加入稀硝酸中:Cu+4H++NO3﹣=Cu2++NO↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将MnO2与FeSO4溶液、硫酸充分反应后过滤,将滤液加热至60℃后,再加入Na2CO3溶液,最终可制得碱式碳酸锰[aMnCO3·bMn(OH)2·cH2O]。
(1)用废铁屑与硫酸反应制备FeSO4溶液时,所用铁屑需比理论值略高,原因是 ,反应前需将废铁屑用热Na2CO3溶液浸泡,其目的是 。
(2)为测定碱式碳酸锰组成,取7.390 g样品溶于硫酸,生成CO2 224.0 mL(标准状况),并配成500 mL溶液。准确量取10.00 mL该溶液,用0.0500 mol·L-1 EDTA(化学式Na2H2Y)标准溶液滴定其中的Mn2+(原理为Mn2+ +H2Y2-=MnY2-+2H+),至终点时消耗EDTA标准溶液28.00 mL。通过计算确定该样品的化学式。(写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中存在XO3―,且X为短周期元素,则一定能在该溶液中大量共存的离子组是( )
A.Na+、H+、SO42-、I-
B.Na+、Ca2+、CO32-、Al3+
C.Na+、K+、Fe2+、H+
D.K+、SO42-、Cl-、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向有机物X中加入合适的试剂(可以加热),检验其官能团。下列有关结论不正确的是:( )
选项 | 试剂 | 现象 | 结论 |
A | 金属钠 | 有气体产生 | 含羟基 或羧基 或羟基和羧基 |
B | 银氨溶液 | 产生银镜 | 含有醛基 |
C | 碳酸氢钠溶液 | 产生气泡 | 含有羧基 |
D | 溴水 | 溶液褪色 | 含有碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气常用作致冷剂及制取铵盐和氮肥,是一种用途广泛的化工原料。
(1)下表是当反应器中按n(N2):n(H2)=1:3投料后,在200℃、400℃、600℃下,反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线。
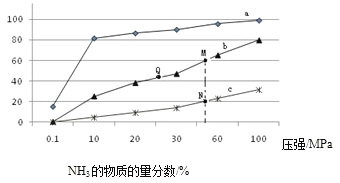
①曲线a对应的温度是 。
②关于工业合成氨的反应,下列叙述正确的是 (填字母)。
A. 及时分离出NH3可以提高H2的平衡转化率
B. 加催化剂能加快反应速率且提高H2的平衡转化率
C. 上图中M、N、Q点平衡常数K的大小关系是K(M)= K(Q) >K(N)
③ M点对应的H2转化率是 。
(2)工业制硫酸的尾气中含较多的SO2,为防止污染空气,回收利用SO2,工业上常用氨水吸收法处理尾气。
① 当氨水中所含氨的物质的量为3 mol ,吸收标准状况下44.8 L SO2时,溶液中的溶质为 。
② NH4HSO3溶液显酸性。用氨水吸收SO2,当吸收液显中性时,溶液中离子浓度关系正确的是 (填字母)。
a.c(NH4+) = 2c(SO32-) + c(HSO3-)
b.c(NH4+)> c(SO32-)> c(H+)= c(OH-)
c.c(NH4+)+ c(H+)= c(SO32-)+c(HSO3-)+c(OH-)
(3)氨气是一种富氢燃料,可以直接用于燃料电池,下图是供氨水式燃料电池工作原理:
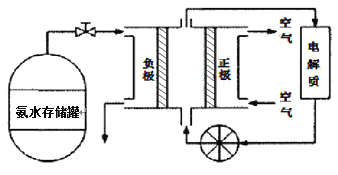
①氨气燃料电池的电解质溶液最好选择 (填“酸性”、“碱性”或“中性”)溶液。
②空气在进入电池装置前需要通过过滤器除去的气体是 。
③氨气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池正极的电极反应方是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列转化不属于煤或石油的综合利用的是 ( )
A. 将煤干馏制得煤焦油和焦炭 B. 在一定条件下将煤与氢气转化为液体燃料
C. 将煤变为煤饼作燃料 D. 将石油裂解制得乙烯等化工原料
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com