
【题目】如图是一种叶绿素分子(左)和血红蛋白分子(右)的局部结构简图,下列说法不正确的是( )

A.合成叶绿素和血红蛋白分别需要镁和铁
B.植物体缺氮会影响光合作用
C.人体缺铁会影响血红蛋白对氧的运输
D.Mg和Fe分别存在于植物和动物细胞中
科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液,某同学设计如下实验方案:

(1)操作①为______。
(2)操作②~④加入的试剂可以为____________。
(3)如何判断SO42-已除尽,简述实验操作____________。
(4)该同学设计的实验方案______(填“合理”或“不合理”),理由是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是:__________

(2)实验室制备氯气时要在通风橱内完成,并且为了防止氯气污染空气,要有尾气处理装置,一般用_________溶液吸收多余的氯气,原理是(用化学方程式表示)_________________
(3)根据这一原理,工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白粉,反应的化学方程式是__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaH2PO2(次磷酸钠)易溶于水,水溶液近中性,具有强还原性,可用于化学镀银、镍、铬等。一种利用泥磷(含P4和少量CaO、Fe2O3、Al2O3、CaCl2等)为原料制备NaH2PO2·H2O的工艺流程如下:

已知P4与两种碱的反应主要有:
Ⅰ. 2Ca(OH)2+P4+4H2O=2Ca(H2PO2)2+2H2↑ Ⅱ. 4NaOH + P4+8H2O = 4NaH2PO2·H2O+2H2↑
Ⅲ. 4NaOH + P4+2H2O = 2Na2HPO3 +2PH3↑ Ⅳ. NaH2PO2+NaOH = Na2HPO3+H2↑
(1) 已知H3PO2是一元中强酸,NaH2PO2是___________(填“正盐”或“酸式盐”)。
(2)尾气中的PH3被NaClO溶液吸收可生成NaH2PO2,从吸收液中获得NaH2PO2·H2O的操作为______________、______________过滤、洗涤和干燥。
(3) 用NiCl2、NaH2PO2溶液化学镀Ni,同时生成H3PO4和氯化物的化学方程式为:______________________。
(4) “反应”在温度和水量一定时,混合碱总物质的量与P4的物质的量之比[n(碱)/ n(磷)]与NaH2PO2产率的关系如图所示。当n(碱)/ n(磷)>2.6时,NaH2PO2的产率随n(碱)/ n(磷)的增大而降低的可能原因是______。

(5) 滤渣2主要成分为___________________ (填化学式)。
(6) “过滤2”的滤液须用Ag2SO4、Ba(OH) 2及Na2S溶液除去其中Cl-及Fe2+等,其中加入的Ag2SO4溶液不宜过量太多,其主要原因是_________________。
(7)在工业上,可以用惰性电极电解NaH2PO2溶液制取磷酸,请写出其阳极反应式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)基态Cl原子中,电子占据的最高能层具有的原子轨道数为____。
(2)NH4CuSO3中金属阳离子的价电子排布式为________。N、O、S三种元素的第一电离能由大到小的顺序为________ (填元素符号)。
(3)氨基乙酸钠(H2NCH2COONa)中中心原子N原子的价层电子对数为________,C原子的杂化方式为________,1 mol氨基乙酸钠中含有σ键的数目为________。
(4)向CuSO4溶液中加入过量氨水,可生成[Cu(NH3)4]SO4溶液,在[Cu(NH3)4]2+中配原子为________。
(5)MgO和CaO均为离子晶体,两者的熔融混合物冷却时,先析出的晶体是____,原因是________
(6)BN的熔点是3000℃,密度为d g·cm-3,其晶胞结构如图所示,晶体中一个B原子周围距离最近的N原子有________个;若原子半径分别为rN pm和rB pm,阿伏加德罗常数值为NA,则BN晶胞中原子的体积占晶胞体积的百分率为__________(用含d、rN 、rB、NA的式子表示)

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上由乙苯生产苯乙烯的反应如下,有关说法正确的是
![]()
A. 该反应的类型为取代反应
B. 可用溴水鉴别乙苯和苯乙烯
C. 乙苯分子中所有原子可能在同一平面
D. 比乙苯多一个碳原子的同系物R的同分异构体(包含R)共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某无色透明溶液中仅含有包括Na+和CH3COO-在内的四种离子。
请回答下列问题。
(1)该溶液中的溶质可能有三种情况,请分别写出各种情况的化学式:
①_____________________;②________________________;③____________________ 。
(2)25℃,若由0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合,测得混合溶液的pH=8,则c(CH3COOH)+c(H+)的精确值为___________________mol/L。
(3)若该溶液的pH=8,则c(Na+)-c(CH3COO-)的精确值为___________________mol/L。
(4)当溶液中各离子浓度大小的顺序为c(CH3COO-)>c(Na+)>c(H+)>c(OH-)时,则该溶液可能是____(填序号);
A.由0.1 mol/L的CH3COONa溶液与0.1 mol/L的CH3COOH溶液等体积混合而成
B.由0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合而成
C.由0.2 mol/L的CH3COONa溶液与0.1 mol/L的HCl溶液等体积混合而成
D.由0.2 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液等体积混合而成
(5)常温下,将a mol/L的CH3COOH溶液与0.01 mol/L的NaOH溶液等体积混合,反应平衡后溶液中c(Na+)=c(CH3COO-),用含a的代数式表示CH3COOH的电离平衡常数Ka=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计并进行了以下实验(苯,一种不溶于水,密度比水小的液体):
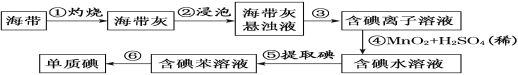
请回答下列问题:
(1)步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是________(填标号)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥器
(2)步骤③的实验操作名称是________;步骤⑥的目的是从含碘苯溶液中分离出单质碘和回收苯,该步骤的实验操作名称是________。
(3)步骤⑤是萃取、分液,某学生选择用苯来提取碘的理由是___________________。
在分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
A.直接将含碘苯溶液从分液漏斗上口倒出
B.直接将含碘苯溶液从分液漏斗下口放出
C.先将水层从分液漏斗的下口放出,再将含碘苯溶液从下口放出
D.先将水层从分液漏斗的下口放出,再将含碘苯溶液从上口倒出
(4)请设计一种检验提取碘后的水溶液中是否还含有单质碘的简单方法:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出如图中序号①~④仪器的名称:
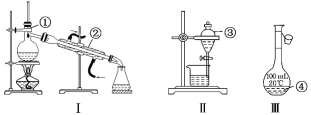
(1)①_____;②____;③_____;④_____。
(2)仪器①~④中,使用时必须检查是否漏水的有____(填仪器序号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com