
【题目】下列各组中两溶液间的反应,均可用同一离子方程式表示的是
A.CH3COOH和Na2CO3与CH3COOH和NaHCO3
B.AgNO3和HCl与Ag2SO4和HCl
C.BaCl2和Na2SO4 与Ba(OH)2与H2SO4
D.KOH和CH3COONH4与Ba(OH)2与NH4Cl
【答案】D
【解析】本题考查离子方程式的书写。醋酸与碳酸钠反应的离子方程式为:![]() +2CH3COOH
+2CH3COOH![]() H2O+CO2↑+2CH3COO,醋酸与碳酸氢钠反应的离子方程式为:HCO3+CH3COOH
H2O+CO2↑+2CH3COO,醋酸与碳酸氢钠反应的离子方程式为:HCO3+CH3COOH![]() H2O+CO2↑+CH3COO,两个离子方程式不同,A错误;AgNO3和HCl反应的离子方程式为Ag++Cl
H2O+CO2↑+CH3COO,两个离子方程式不同,A错误;AgNO3和HCl反应的离子方程式为Ag++Cl![]() AgCl↓,Ag2SO4和HCl反应的离子方程式为Ag2SO4+2Cl
AgCl↓,Ag2SO4和HCl反应的离子方程式为Ag2SO4+2Cl![]() 2AgCl↓+
2AgCl↓+![]() ,两个离子方程式不同,B错误;氯化钡与硫酸钠反应的离子方程式为:
,两个离子方程式不同,B错误;氯化钡与硫酸钠反应的离子方程式为:![]() +Ba2+
+Ba2+![]() BaSO4↓,而氢氧化钡与硫酸反应的离子方程式为:2H++
BaSO4↓,而氢氧化钡与硫酸反应的离子方程式为:2H++![]() +Ba2++2OH
+Ba2++2OH![]() BaSO4↓+2H2O,两个离子方程式不同,C错误;KOH和CH3COONH4与Ba(OH)2和NH4Cl,实质都是铵离子与氢氧根离子的反应,反应方程式为:
BaSO4↓+2H2O,两个离子方程式不同,C错误;KOH和CH3COONH4与Ba(OH)2和NH4Cl,实质都是铵离子与氢氧根离子的反应,反应方程式为:![]() +OH
+OH![]() NH3H2O,故D正确;故选D。
NH3H2O,故D正确;故选D。


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案科目:高中化学 来源: 题型:
【题目】已知CuS和Cu2S均为黑色,常温下都不溶于稀盐酸,在氧气中加热,最后都转化为CuO和SO2。某黑色固体样品的成分可能是CuO、CuS和Cu2S的一种或几种。某课外研究小组为探究其成分,设计以下实验测定该样品与氧气反应前后的质量变化,同时检测其气体产物。
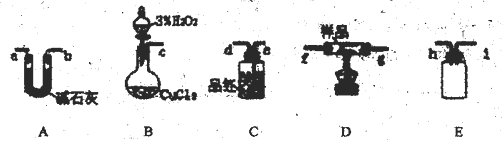
(1)获得氧气的反应方程式为__________。硫化亚铜与氧气反应的方程式为__________。
(2)利用上述装置(可重复使用)进行实验,气流经导管的顺序为__________。
(3)实验测得样品质量为m1,与氧气充分反应后的固体质量为m2,m1 =m2,且C装置中品红褪色,则样品的成分(写出所有可能情况)_________。
(4)该实验小组为了控制实验中氧气的产生速率,设计了如下图所示的实验装置继续探究不同的催化剂对H2O2分解的催化效率。
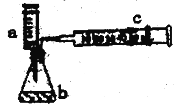
①实验时可以通过测量_________来体现H2O2的分解速率的大小。
②请设计实验比较Fe3+含 Cu2+对H2O2分解的催化效率(完成以下实验方案):_______,最后,比较两个实验的氧气的体积。(试剂仪器不限,装置用上图)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质转化在一定条件下不能实现的是( )
A. Al2O3→Al(OH)3→Al B. Cu→CuO→CuSO4
C. Na→NaOH→Na2CO3 D. Fe(OH)3→Fe2O3→Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
A. 先加入BaCl2溶液,产生白色沉淀,再加入足量的HNO3溶液,沉淀不溶解。则溶液中一定含有![]()
B. 加入足量的HCl溶液,产生了无色无味的气体。则溶液中一定含有![]()
C. 先加入足量稀盐酸无沉淀,再加入BaCl2溶液产生白色沉淀。则溶液中含有![]() 。
。
D. 先加盐酸将溶液酸化,再加AgNO3溶液,产生白色沉淀。溶液中一定含有Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂一铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O==2Cu+2Li++2OH-,下列说法不正确的是
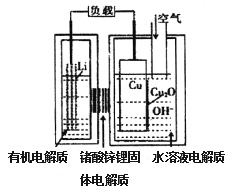
A. 放电时,正极的电极反应式为Cu2O+H2O+2e-=2OH-+2Cu
B. 放电时,电子透过固体电解质向Li极移动
C. 通空气时,铜电极被腐蚀,表面产生Cu2O
D. 整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C2H5OH(l)+3O2(g)![]() 2CO2(g)+3H2O(g) ΔH=1 367.0 kJ·mol1(燃烧热)
2CO2(g)+3H2O(g) ΔH=1 367.0 kJ·mol1(燃烧热)
B.NaOH(aq)+HCl(aq)![]() NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol1(中和热)
NaCl(aq)+H2O(l) ΔH=+57.3 kJ·mol1(中和热)
C.S(s)+O2(g)![]() SO2(g) ΔH=297.2 kJ·mol1(反应热)
SO2(g) ΔH=297.2 kJ·mol1(反应热)
D.2NO2![]() 2NO+O2 ΔH=+116.2 kJ·mol1(反应热)
2NO+O2 ΔH=+116.2 kJ·mol1(反应热)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是( )
A. Na2O2、Fe3O4、CuO均为碱性氧化物
B. 盐酸、水玻璃、氨水均为混合物
C. 烧碱、冰醋酸、四氯化碳均为电解质
D. 稀豆浆、硅酸、氯化铁溶液均为胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BaCl2·xH2O是用途广泛的基础化工产品。我国目前主要是用盐酸和硫化钡(含少量Mg2+、Fe3+等)反应生产BaCl2·xH2O,工艺流程如下图所示。
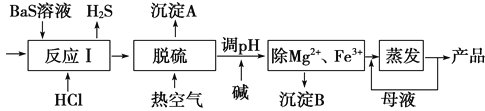
已知:室温时Ksp[Mg(OH)2]=1.8×10-11 , Ksp[Fe(OH)3]=4.0×10-38 ,请回答下列问题:
(1)反应Ⅰ中生成的H2S用足量氨水吸收,一定条件下向所得溶液中通入空气,又可得到单质硫并使吸收液再生,再生反应的化学方程式为______________________________。
(2)所得氯化钡粗液中含硫化合物(H2S、HS-等)影响产品质量,可鼓入预热后的空气吹除,预热空气的目的是_______________;沉淀A的主要成分是_______________。
(3)热空气吹除时会有部分HS-转变为S2O![]() ,使产品仍达不到纯度要求,可再进行酸化脱硫,酸化脱硫时的离子方程式为____________________________________________。
,使产品仍达不到纯度要求,可再进行酸化脱硫,酸化脱硫时的离子方程式为____________________________________________。
(4)室温时,若加碱调溶液pH调至9,则完全沉淀的离子是__________,另一离子浓度为______mol/L (当溶液中离子浓度小于1×10-5 mol/L时认为该离子完全沉淀) 。若向0.1 mol/L FeCl3溶液中加入一定量等浓度的Na2CO3溶液,出现的现象________,发生反应的离子方程式___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室制取CO2的离子反应方程式:_______________________;
(2)氢氧化钡和硫酸镁溶液混合反应的离子方程式:_______________________;
(3)氢氧化铁胶体制备的离子反应:___________________________。
(4)同温同压条件下,等质量的CO和CO2的密度比为:____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com