
| ʵ������ | ʵ������ | ���ͼ����� |
| �۲���ˮ����ɫ��״̬ | �ʻ���ɫ | �� C |
| ����ˮ�е��뼸����������Һ | �а�ɫ���� | �� A |
| �ò�����պȡ��ˮ��������ɫʯ����ֽ�� | ������ˮ����ֽ�м��ף���Ȧ��� | �� B |
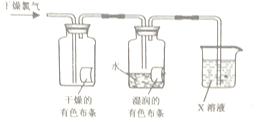
���� ��1������Ϊ����ɫ���壬����ˮ�е��뼸����������Һ���ɵİ�ɫΪAgCl��HCl����ʹʪ����ɫʯ����ֽ���ɫ��HClO����ǿ�����ԣ�����Ư����ɫ���ʣ�
��2��ͨ��ʵ������뷴Ӧ�����о���ˮ���ʣ���ȡʵ�鷨��۲취��
��3���ٸ������ɫ��������ɫ��ʪ�����ɫ������ɫ��˵����������û��Ư���ԣ�
�����������Һ��Ӧ������������������Һ���գ���ֹ��Ⱦ������
��� �⣺��1���۲���ˮ����ɫ��״̬���ʻ���ɫ��˵����ˮ�д���Cl2���ӣ�
����ˮ�е��뼸����������Һ�����ɵİ�ɫΪAgCl��˵���Ȼ��д���Cl-��
�ò�����պȡ��ˮ��������ɫʯ����ֽ�ϣ�HCl����ʹʪ����ɫʯ����ֽ���ɫ��HClO����ǿ�����ԣ�����Ư����ɫ���ʣ�
�ʴ�Ϊ����C����A����B��
��2��ͨ��ʵ������뷴Ӧ�����о���ˮ���ʣ���ȡʵ�鷨��۲취��
�ʴ�Ϊ��AD��
��3���ٸ������ɫ��������ɫ��ʪ�����ɫ������ɫ��˵����������û��Ư���ԣ�
�ʴ�Ϊ����������û��Ư���ԣ�
�����������Һ��Ӧ������������������Һ���գ���ֹ��Ⱦ������
�ʴ�Ϊ��NaOH��
���� ���⿼����ˮ����̽��ʵ�飬��Ŀ�����˻�ѧ����ʵ��Ϊ������ѧ�ƣ���ǿ��ѧѧϰ��ʵ����ʶ��


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgCl2 | B�� | NaOH | C�� | HBr | D�� | N2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
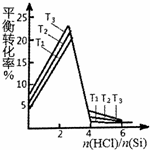 ������裨SiHCl3���������ྦྷ�����Ҫԭ�ϣ��ɴֹ����������ķ�Ӧ���£�
������裨SiHCl3���������ྦྷ�����Ҫԭ�ϣ��ɴֹ����������ķ�Ӧ���£�| ��Ӧ���Ȼ�ѧ����ʽ | ƽ�ⳣ����300�棩 | |
| ����Ӧ | Si��s��+3HCl��g��?SiHCl3��g��+H2��g����H=-210kJ•mol-1 | K1��mol•L-1��-1 |
| ����Ӧ | Si��s��+4HCl��g��?SiHCl4��g��+2H2��g����H=-240kJ•mol-1 | K2��mol•L-1��-1 |
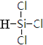 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl | B�� | MgO | C�� | SO3 | D�� | CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������Ʊ�����ú���� | |
| B�� | Ũ�������ڹ���Լ�ƿ�� | |
| C�� | FeSO4��Һ����ڼ����������۵��Լ�ƿ�� | |
| D�� | ��ˮӦװ����ɫϸ��ƿ���ܷ�ܹⱣ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Fe2+��H+��Cl-��NO3- | B�� | Na+��Ba2+��OH-��NO3- | ||
| C�� | OH-��K+��NO3-��HCO3- | D�� | Fe3+��NH4+��SO42-��SCN- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
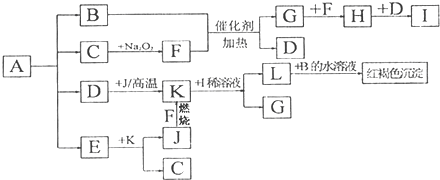
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO3��H2SO4 | B�� | HNO3��NO | C�� | Fe��FeCl2 | D�� | Cl2��HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com