
(15分)电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
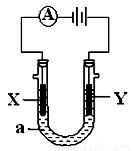
(1)若X、Y都是惰性电极,a是NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:
① Y电极上的电极反应式为 。
在X极附近观察到的现象是 。
②电解总反应离子方程式为 。
(2)要在铁件的表面镀铜防止铁被腐蚀,则:
① Y电极的材料是 (选填纯铁、纯铜或纯锌),电极反应式是 。电解液a选用 溶液,电解过程中其浓度 (选填增大、减小或不变)。
② 若电镀前X、Y两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为 mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:
。
(1)①2Cl--2e-=Cl2↑(2分) 有气泡产生,溶液变红(2分)
②2Cl- +2H2O电解2OH-+Cl2↑+H2↑(2分)
(2)①纯铜 (1分)Cu-2e-=Cu2+ (2分) CuSO4(其他合理答案也给分) (1分)不变(1分)② 0.08mol(2分)
③铁比铜活泼,镀层破坏后,在潮湿的环境中形成原电池,加速铁的腐蚀(其他合理答案也给分) (2分)
【解析】(1)由图,得:电子从外加电源的负极流向电解池的阴极X,溶液中的阴离子(Cl-、OH-)从阴极X移向阳极Y,再阳极Y发生失电子的反应,电子流回外加电源的正极;则溶液中的阳离子(Na+、H+)从阳极Y移向阴极X;
①故两极反应为:Y:2Cl--2e-=Cl2↑(放电能力:Cl->OH-),X:2H++2e-= H2↑(放电能力:H+>Na+)因为消耗了H+,则水的电离平衡(H2O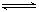 H++ OH-)正向移动,使C(OH-)增大,即C(OH-)>C(H+),故溶液变红;
H++ OH-)正向移动,使C(OH-)增大,即C(OH-)>C(H+),故溶液变红;
②总化学方程式为2 NaCl +2H2O电解2NaOH+Cl2↑+H2↑
(2)要在铁件的表面镀铜,则铁件作阴极,可用纯铜作阳极,故两极反应为:
①阳极:Cu-2e-= Cu2+,Cu2++2e-= Cu,故电解过程中溶液中C(Cu2+)不变;
②设电镀前X、Y两电极的质量均为m g,依据电极反应式判断:设电解过程中阳极减少a g,则阴极就增加a g,即:(m+a)-(m-a)= 5.12 g,则a=2.56 g,n(Cu)=2.56 g/64g.mol-1=0.04 mol,Cu——2e-,则n(e-)=2 n(Cu)=0.08mol;
③镀层破损后,镀铜铁中,铁比铜活泼,故加速铁的腐蚀;
镀层破损后,镀锌铁中,锌比铁活泼,故加速锌的腐蚀;


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:

| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | Fe(NO3)3 |
| D | 铁 | 银 | AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 (I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(I)Li-SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4-SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.查看答案和解析>>
科目:高中化学 来源: 题型:
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X,Y是两块电极板,通过导线与直流电源相连.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com