
【题目】一定温度下,向一容积为10 L的恒容密闭容器中充入2 mol SO2和1mol O2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196 kJ/mol。当反应进行10分钟时达到平衡状态,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) ΔH=-196 kJ/mol。当反应进行10分钟时达到平衡状态,容器内压强变为起始时的0.7倍。请回答下列问题:
(1)SO2的转化率为______________________。
(2)从开始到10分钟,用氧气表示该反应的平均反应速率v(O2)=______________________。
(3)达到平衡时反应放出的热量为______________________。
【答案】 90% 9×10-3mol/(L·min) 176.4kJ
【解析】(1)根据转化率概念等于变化量比上初始量进行解答;(2)根据化学反应速率公式进行计算;(3)依据热化学方程式定量关系和实际消耗二氧化硫的物质的量计算反应放出的热量进行解答。
(1)设SO2的变化量是x,则根据三段式有:
2SO2(g)+O2(g)2SO3(g)
初始物质的量(mol): 2 1 0
变化物质的量(mol): x 0.5x x
平衡物质的量(mol):2 -x 1-0.5x x
当反应达到平衡时,容器内压强变为起始时的0.7倍,则(2-x+1-0.5x+x)/(2+1)=0.7,x=1.8 mol。SO2的转化率为=变化量 /初始量×100%=90%
(2)结合上述分析知,从开始到10分钟,氧气的变化量为0.9 mol,氧气浓度变化为c(O2)=0.09 mol/L,反应的平均反应速率v(O2)= 0.009 mol/(L.min)。答案:9×10-3mol/(L·min)
(3)2SO2(g)+O2(g)2SO3(g)△H=196kJ/mol,反应过程中消耗二氧化硫物质的量2mol放196KJ,根据上述分析消耗二氧化硫物质的量为1.8mol,放出热量=1.8mol×196KJ/2mol =176.4kJ,答案:176.4kJ。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法正确的是( )

A. 简单阳离子半径:X>R
B. X与Y可以形成正四面体结构的分子
C. M的氢化物常温常压下为液体
D. 最高价氧化物对应水化物的酸性:Z<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种有机物的结构简式如图,关于它的性质不正确的说法是( )
A.它有酸性,1 mol该物质最多能与6 mol H2发生加成反应
B.它可以水解,水解产物为两种有机物
C.在一定条件下,1 mol该物质最多能和8 mol NaOH反应
D.该有机物能发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度
C.氯离子存在时铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液都出现沉淀,表明二者均可使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小明体检的血液化验单中,葡萄糖为5.9×10﹣3mol/L.表示该体检指标的物理量是( )
A.溶解度(s)
B.物质的量浓度(c)
C.质量分数(w)
D.摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW , 该温度下,将浓度为a mol/L的一元酸HA与b mol/L一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A.混合溶液的pH=7
B.混合溶液中,c(H+)= ![]() mol/L
mol/L
C.a=b
D.混合溶液中,c(H+)+c(B+)=c(OH﹣)+c(A﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫氧化物易引起环境行染,需要悉心研究。
(1)二氧化硫可用于催化氧化制硫酸。硫酸工业中,作为催化剂的V2O5对反应I的催化循环过程经历了Ⅱ、Ⅲ两个反应阶段,如图所示:

下列分子中1mol化学键断裂时需要吸收的能量数据如下:
化学键 | S=O(SO2) | S=O(SO3) | O=O(O2) |
能量/kJ | 535 | a | 496 |
反应Ⅰ的△H=-98 kJ ·mol-1,则 a=____________。反应Ⅲ的化学方程式为______________。将2molSO2和1molO2充入密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。平衡时SO3的体积分数(% )随温度和压强的变化如表所示:下列判断正确的是(_____________)
2SO3(g)。平衡时SO3的体积分数(% )随温度和压强的变化如表所示:下列判断正确的是(_____________)
压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
350 | 5.0 | a | b |
415 | c | 40.0 | d |
550 | e | f | 36.0 |
A.b >e
B.415℃、2.0MPa时O2的转化率为60%
C.在一定温度和压强下,加入V2O5作催化剂能加快反应速率,提高SO3的体积分数
D.平衡常数K(550℃)>K(350℃)
(2)较纯的SO2,可用于原电池法生产硫酸。图中离子交换膜是________离子交换膜(填“阴”、“阳”)。

(3)研究发现,含碱式硫酸铝的溶液与SO2结合的方式有2种:其一是与溶液中的水结合。其二是与碱式硫酸铝中的活性Al2O3结合,通过酸度计测定吸收液的pH变化,结果如右图所示:

请解释曲线如图变化的原因_______________________________。
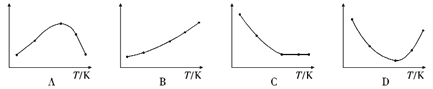
(4)取五等份SO3,分别加入温度不同、容积相同的恒容密闭容器中,发生反应:3SO3(g)![]() (SO3)3(g) △H<0,反应相同时间后,分别测定体系中SO3的百分含量,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是(_____)
(SO3)3(g) △H<0,反应相同时间后,分别测定体系中SO3的百分含量,并作出其随反应温度(T)变化的关系图。下列示意图中,可能与实验结果相符的是(_____)
(5)用Na2SO3溶液作为吸收液吸收SO2时,产物为NaHSO3,已知亚硫酸的两级电离平衡常数分别为Ka1、Ka2。则常温下NaHSO3溶液显酸性的充要条件为_____________。(用含为Ka1、Ka2的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com