

���� I��������Һ���ڽ��壬���ж����ЧӦ��
���������ھƻ�ø�������������л���AΪCH3CH2OH��A������ȥ��Ӧ����BΪCH2=CH2��A��������������C����������Ϣ֪��CΪCH3COOH��DΪCH3COOCH=CH2��D�����Ӿ۷�Ӧ����EΪ ��
��
��� �⣺I�����û�ѧ�Լ������õ�ˮ������ۣ�Ҳ����������Һ���������ǣ��粻�û�ѧ�Լ����ɿ��ǵ������뾶�ϴ�����Һ���н�������ʣ��ɽ�һ������ͨ������Һ���ܹ۲쵽һ������ͨ·��Ϊ������Һ����֮Ϊ��������Һ��
�ʴ�Ϊ���ɽ�һ������ͨ������Һ���ܹ۲쵽һ������ͨ·��Ϊ������Һ����֮Ϊ��������Һ��
���������ھƻ�ø�������������л���AΪCH3CH2OH��A������ȥ��Ӧ����BΪCH2=CH2��A��������������C����������Ϣ֪��CΪCH3COOH��DΪCH3COOCH=CH2��D�����Ӿ۷�Ӧ����EΪ ��
��
���Ҵ�������ȥ��Ӧ������ϩ����Ӧ����ʽΪ��CH3CH2OH$��_{Ũ����}^{170��}$CH2=CH2��+H2O��
�ʴ�Ϊ��CH3CH2OH$��_{Ũ����}^{170��}$CH2=CH2��+H2O��
��ͨ�����Ϸ���֪��DΪCH3COOCH=CH2���ʴ�Ϊ��CH3COOCH=CH2��
��2�������ǵĽṹ��ʽΪ��HOCH2��CHOH��4CHO��F�����弡��ϸ���е���������ȱ�������½������������IJ����F��CH3CH��OH��COOH������Ϊ���ᣬ
�ʴ�Ϊ��HOCH2��CHOH��4CHO�����ᣮ
���� ���⿼���л����ƶϼ��л�����𣬸��ݷ�Ӧ���������ƶϣ�ע��������Ϣ�����ã���Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4 L CCl4����4nA��Clԭ�� | |
| B�� | 7.8 g Na2O2������ˮ��Ӧת��0.2nA������ | |
| C�� | 0.1 mol•L-1NaCl��Һ�к���0.1nA��Na+ | |
| D�� | ���³�ѹ�£�23 gNO2��N2O4��������к���nA����ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �ȷ� | B�� | 1-�ȱ��� | C�� | 2-���� | D�� | 2-��-2-����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16.51 g | B�� | 23.82 g | C�� | 24.84 g | D�� | 17.02 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
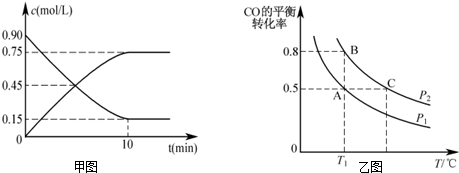
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
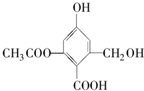
| A�� | X�Ļ�ѧʽΪC10H10O6 | |
| B�� | X��һ������������FeCl3��Һ������ɫ��Ӧ | |
| C�� | 1mol X�ֱ���������Na��NaOH��Һ��NaHCO3��Һ��Ӧ���������������ʵ����ʵ����ֱ�Ϊ3mol��5mol��1mol | |
| D�� | X�ȿ��Ժ��Ҵ��ֿ��Ժ����ᷢ��������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����һ����C��ƽ�������ƶ� | |
| B�� | �����¶Ȳ��䣬�����ݻ�ѹ����ԭ����һ�룬����B��Ũ�ȱ�Ϊԭ����1.8������ƽ�������ƶ� | |
| C�� | ���º�ѹ���ٳ���1mol�����������뷴Ӧ����A��ת����������m��n | |
| D�� | ���º�ѹ���ټ���2mol��A�������ƽ����Է���������Ϊԭ����2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ�ǻ�ԭ���� | B�� | Fe��OH��3������ԭ��Ӧ | ||
| C�� | Cl2�������� | D�� | ÿ����1mol K2FeO4ת��2mol���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com