
|
将H2、C2H5OH、O2的混合蒸气通入Na2O2密闭容器中,用电火花引燃,反应完全后,体系内的压强为零帕斯卡,则气体的混合比可能为 | |
A. |
3∶4∶2 |
B. |
3∶2∶2 |
C. |
7∶2∶1 |
D. |
9∶3∶4 |
科目:高中化学 来源: 题型:
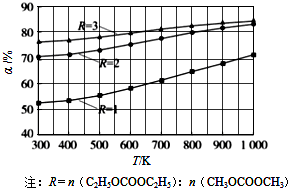 (2012?广州一模)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1
(2012?广州一模)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.请回答:
某同学设计了如图所示装置(部分夹持装置已略去)进行实验研究.请回答:| 序号 | V(H2SO4)/mL | C(H2SO4)/mol?L-1 | t/s |
| I | 40 | 1 | t1 |
| II | 40 | 4 | t2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl和NaOH反应的中和热△H=-57.3kJ/mol.则H2SO4和Ba(OH)2反应的中和热△H=2×(-57.3)kJ/mol | B、已知C2H5OH(l) 的燃烧热是1366.8KJ/mol,则C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)反应的△H=-1366.8kJ/mol | C、一定条件下2SO2(g)+O2(g)?2SO3(g)△H1,2SO2(g)+O2(g)?2SO3(l)△H2则△H1>△H2 | D、在一定温度和压强下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放出热量19.3kJ,则其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com