
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,元素W的一种单质是熔点高硬度大的宝石,Y的原子半径在所有短周期主族元素中最大。X和Z同主族,由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有刺激性气体产生。回答下列问题:
(1)Y元素位于周期表中的位置是_____________________。
(2)Z元素是______,由X和Z两种元素形成的化合物是______________。
(3)四种元素中的_______________元素是形成化合物最多的元素。
(4)某同学做同周期元素性质递变规律实验时,自己设计一套实验方案,并记录了有关实验现象如下表。

填写下列空格﹕
①实验目的:____________________________ 。
②与实验方案相对应的实验现象是:实验方案2对应的实验现象是___________(填上表中的符号A.......F);实验方案3对应的实验现象是__________________________。
③得出规律:同周期元素从左到右_________________________________。
【答案】 第三周期第ⅠA族 硫(S) SO2 SO3 碳(C) 探究同周期元素的金属性和非金属性的递变规律 F A 金属性逐渐减弱非金属性逐渐增强
【解析】短周期主族元素W、X、Y、Z的原子序数依次增大,元素W的一种单质是熔点高硬度大的宝石则为C元素,Y的原子半径在所有短周期主族元素中最大则为钠元素。X和Z同主族,由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有刺激性气体产生。故X为氧元素、Z为硫元素。(1)Y为钠元素,位于周期表中的位置是第三周期第ⅠA族;(2)Z元素是硫(S),由X和Z两种元素形成的化合物是SO2 SO3;(3)四种元素中的碳(C)元素是形成化合物最多的元素,有机物的种类繁多;(4)①根据表中信息可知,实验目的为:探究同周期元素的金属性和非金属性的递变规律;②与实验方案相对应的实验现象是:实验方案2向硫化钠溶液中滴加新制氯水,反应置换出硫单质,故对应的实验现象是生成淡黄色沉淀,答案选F;实验方案3钠与滴有酚酞试液的冷水反应,对应的实验现象是浮在水面,熔成一个小球,在水面上无定向移动,随之消失,溶液变红色,答案选A;③得出规律:同周期元素从左到右金属性逐渐减弱非金属性逐渐增强。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某无色溶液中含有H+、Al3+、Mg2+三种阳离子,逐滴加入0.1moLL﹣1NaOH溶液,消耗NaOH溶液体积(X轴)和生成沉淀(Y轴)之间的函数关系如图所示,则溶液中H+、Al3+、Mg2+三种阳离子的物质的量浓度之比为( ) 
A.1:1:1
B.2:2:1
C.2:1:1
D.1:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】参考如图,按要求回答下列问题: 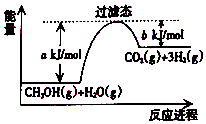
(1)甲醇质子交换膜燃料电池将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O反应生成CO2和H2 . 若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是(填“增大”、“减小”、“不变”),反应热△H的变化是(填“增大”、“减小”、“不变”).请写出CH3OH(g)和H2O(g)反应的热化学方程式 .
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的另一种反应原理是:
CH3OH(g)+ ![]() O2(g)CO2(g)+2H2(g)△H=﹣c kJ/mol
O2(g)CO2(g)+2H2(g)△H=﹣c kJ/mol
又知H2O(g)H2O(l)△H=﹣d kJ/mol.
则甲醇燃烧热的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下面的方案进行某些离子的检验,其中方案设计严密的是( )
A. 检验试液中的SO42-:试液![]() 无沉淀
无沉淀![]() 白色沉淀
白色沉淀
B. 检验试液中的SO32-:试液![]() 气体
气体![]() 褪色
褪色
C. 检验试液中的I-:试液![]() 棕黄色溶液
棕黄色溶液![]() 蓝色溶液
蓝色溶液
D. 检验试液中的CO32-:试液![]() 白色沉淀
白色沉淀![]() 沉淀溶解
沉淀溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物中,在铜的作用下催化氧化,又能发生消去反应,且消去生成物中存在同分异构体的是( )
A.CH3 CH2C(OH)(CH3)2
B.(CH3)2CHOH
C.CH3CH(OH)CH2 CH3
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将少量的铝投入过量的氢氧化钠溶液中充分反应,下列有关所得混合溶液的叙述正确的是( ) 
A.该溶液中,Ag+、K+、NH4+、SO42﹣可以大量共存
B.该溶液中,Na+、OH﹣、NO3﹣、CO32﹣不能大量共存
C.向该溶液中逐滴加入AlCl3溶液,生成沉淀与加入AlCl3溶液关系如图
D.向该溶液中逐滴加入稀盐酸,生成沉淀与加入稀盐酸关系如图
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图1为实验室制取氨气的实验装置。
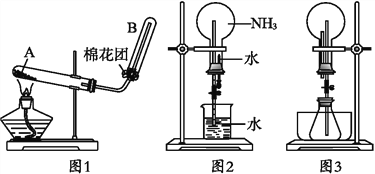
(1)写出A中所发生反应的化学方程式_______________________。要收集干燥的氨气,可以用____________________作干燥剂。
(2)在收集氨气时试管口棉花的作用是___________。
(3)一位学生用制得的氨气,按图2装置进行喷泉实验,烧瓶已充满干燥的氨气,引发喷泉实验的操作是___________。
(4)另一学生积极思考产生喷泉的其他方法,设计了图3装置。首先在锥形瓶中分别加入足量的下列物质,反应后能产生喷泉的是___________。
A.CaCO3粉末和浓盐酸 B.NH4HCO3溶液与稀NaOH溶液
C.HCl和AgNO3溶液 D.HCl和无色酚酞溶液
该同学又向锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是___。
A.硝酸铵 B.食盐 C.浓硫酸 D.硫酸铜
(5)检验氨气已充满试管B的方法是______________.
(6)如制得标准状况下的氨气2.24L,则反应中至少需要熟石灰______g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期元素,其相关信息如下表:
元素 | 相关信息 |
X | X的单质为密度最小的气体 |
Y | Y的氢化物的水溶液呈碱性 |
Z | Z是地壳中含量最高的元素 |
W | W的一种核素的质量数为35,中子数为18 |
(1)W在元素周期表中的位置_________________。
(2)X与Y可形成一种化合物Y2X4,请写出该化合物的电子式__________,工业合成Y的简单氢化物的化学方程式为________________。
(3)X和Z组成的既含有极性共价键又含有非极性共价键的化合物的结构式是______________;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为______________
(4)写出铜和Y的最髙价氧化物的水化物的稀溶液反应的离子方程式______________。
(5)W最高价氧化物的水化物的浓溶液不稳定,受热可分解,产物之一是黄绿色气体,且当有28 mol电子发生转移时,共产生9 mol气体,写出该反应的化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D、E为原子序数依次增大的短周期元素,已知A、B、E 3种原子最外层共有11个电子,且这3种元素的最高价氧化物的水化物两两皆能发生反应生成盐和水,C元素的最外层电子数比次外层电子数少4,D元素原子次外层电子数比最外层电子数多3。
(1)A在空气中燃烧生成原子个数比为1:1的化合物,写出其电子式为_______,写出E元素的同族短周期元素的单质与水反应的化学方程式______________。
(2)写出D、E两元素最高价氧化物对应水化物的酸性强弱_________(用化学式表示)。
Ⅱ.在遭遇冰雪灾害时,常使用一种融雪剂,其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2含有54 mol电子。
(1)该融雪剂XY2的形成过程是________________,X元素在周期表的位置是_______。
(2)元素Q、W原子的最外层电子数是其电子层数的2倍,Q与Y相邻,则Q的离子结构示意图是_______;Q与W能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,该分子的电子式为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com