
���Т�CH3COOH����HCl����H2SO4������Һ��ѡ����գ�
A���٣��ڣ��� B���٣��ڣ��� C����=��=�� D����=�ۣ���
E���٣���=�� F���٣���=�� G����=�ڣ��� H����=�ڣ���
(1)������pH��ͬʱ�������ʵ���Ũ�ȹ�ϵ�� ��
(2)��������ʵ���Ũ����ͬ�Ģ١��ڡ�������Һ���ֱ���ͬŨ�ȵ��ռ���Һ��Ӧ��Ҫʹ��Ӧ�����Һ�����ԣ������ռ���Һ�������ϵΪ ��
(3)������pH��ͬ�������ͬʱ���ֱ��������п����ͬ״���²������������ϵΪ ��
(4)��pH��ͬ���������ϡ��10����pH��ϵΪ ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij��Һ���ܺ���Cl����SO42����CO32����NH4+��Fe3+��Fe2+��Al3+ ��Na+��ijͬѧΪ��ȷ����ɷ֣�ȡ������Һ����Ʋ����������ʵ�飺
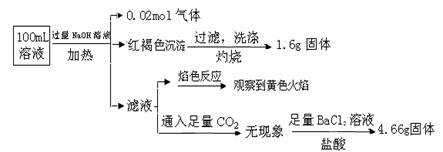
�ɴ˿�֪ԭ��Һ��
A��ԭ��Һ��c��Fe3+��=0.2 mol��L-1
B����Һ��������4�����Ӵ��ڣ�����Cl��һ�����ڣ���c��Cl������0.2 mol��L-1
C��SO42����NH4+ ��Na+һ�����ڣ�CO32����Al3+һ��������
D��ȡ����ԭ��Һ���Թ���,����KSCN��Һ����Һ��Ѫ��ɫ��˵������Һһ��û��Fe2+��ֻ��Fe3+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����ʵ��������ȷ����
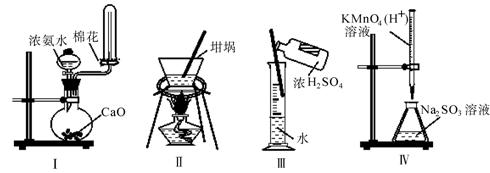
A��ʵ��I���ư��� B��ʵ��II��������Ũ�����ᾧ
C��ʵ��III������1��1��ϡ���� D��ʵ��IV����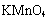 ����Һ�ζ�δ֪Ũ�ȵ�Na2SO3��Һ
����Һ�ζ�δ֪Ũ�ȵ�Na2SO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����£����и���������ָ����Һ���ܴ���������� (����)
A��pH��1����Һ�У�Fe2����NO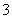 ��SO
��SO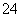 ��Na��
��Na��
B����ˮ�����c(H��)��1��10��14 mol·L��1����Һ�У�Ca2����K����Cl����HCO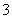
C��c(H��)/c(OH��)��1012����Һ�У�NH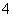 ��Al3����NO
��Al3����NO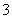 ��Cl��
��Cl��
D��c(Fe3��)��0.1 mol·L��1����Һ�У�K����ClO����SO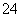 ��SCN��
��SCN��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�����£�Ũ�Ⱦ�Ϊ0.1 mol��L��1��4��������ҺpH���±���
| ���� | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 5.2 |
����˵���У���ȷ���� (����)
A������ˮ�м���NaHCO3������������ˮ�д������Ũ��
B��������Һ�У�ˮ�ĵ���̶�������NaClO
C�������£���ͬ���ʵ���Ũ�ȵ�H2SO3��H2CO3��HClO��pH������H2SO3
D��NaHSO3��Һ������Ũ�ȴ�С˳��Ϊc(Na��)>c(H��)>c(HSO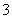 )>c(SO
)>c(SO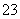 )>c(OH��)
)>c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Դ��ڻ�ѧƽ�����ϵ���ɻ�ѧƽ���뻯ѧ��Ӧ���ʵĹ�ϵ��֪
A����ѧ��Ӧ���ʱ仯ʱ����ѧƽ��һ�������ƶ�
B����ѧƽ�ⷢ���ƶ�ʱ����ѧ��Ӧ����һ���仯
C������Ӧ���еij̶ȴ�����Ӧ����һ����
D��ֻ���ڴ������������£��Żᷢ����ѧ��Ӧ���ʱ仯����ѧƽ�ⲻ�ƶ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ݵ���������Ӧ���Ȼ�ѧ����ʽ
(i) I2(g)+H2(g) 2HI(g) ��H= - 9.48kJ/mol
2HI(g) ��H= - 9.48kJ/mol
(ii) I2(s)+H2(g) 2HI(g) ��H=+ 26.48kJ/mol
2HI(g) ��H=+ 26.48kJ/mol
�����ж���ȷ����
A��254g I2(g)��ͨ��2g H2(g)����Ӧ����9.48 kJ
B��1 mol��̬����1mol��̬���������������l7.00 kJ
C����Ӧ(i)�IJ���ȷ�Ӧ(ii)�IJ����ȶ�
D����Ӧ(i) ��1mol I-I����1mol H-H����Ҫ��������С�ڲ�2mol H-I����Ҫ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1����֪��K2Cr2O7����Һ�д�������ƽ�⣺ Cr2O72-(��ɫ)+H2O 2CrO42-(��ɫ)+2H+����5mL0.1mol/L K2Cr2O7��Һ�еμ�3-10��ŨH2SO4���۲쵽������Ϊ__________���ڴ˻������ٵμ�5-10��6mol/LNaOH��Һ����Һ��ɫ�仯Ϊ__________��
2CrO42-(��ɫ)+2H+����5mL0.1mol/L K2Cr2O7��Һ�еμ�3-10��ŨH2SO4���۲쵽������Ϊ__________���ڴ˻������ٵμ�5-10��6mol/LNaOH��Һ����Һ��ɫ�仯Ϊ__________��
��2���ѽ���ƽ���ij���淴Ӧ�����ı�����ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����__________(�����)��
��������IJ���һ������ ����������������һ�����ӡ�
�۷�Ӧ���Ũ��һ�����͡� �ܷ�Ӧ���ת����һ�����ӡ�
������Ӧ����һ�������淴Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��һС������Ƴ���¶���ڿ����з���һϵ�б仯�����ղ�����(����)
A��NaOH������������������ B��Na2O
C��Na2O2 D��Na2CO3
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com