

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
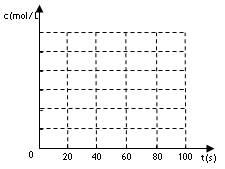
 N2O4”£ĆæøōŅ»¶ØŹ±¼ä¾Ķ¶ŌøĆČŻĘ÷ÄŚµÄĪļÖŹ½ųŠŠ·ÖĪö£¬µĆµ½ČēĻĀ±ķŹż¾Ż£ŗ
N2O4”£ĆæøōŅ»¶ØŹ±¼ä¾Ķ¶ŌøĆČŻĘ÷ÄŚµÄĪļÖŹ½ųŠŠ·ÖĪö£¬µĆµ½ČēĻĀ±ķŹż¾Ż£ŗ| Ź±¼ä/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®NaOH(s) | B£®NaCl(s) | C£®CuSO4 (s) | D£®H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®a > b | B£®a =" b" | C£®a < b | D£®ĪŽ·ØÅŠ¶Ļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 2AB3£¬ĻĀĮŠø÷ĻīĖł±ķŹ¾µÄ·“Ó¦ĖŁĀŹÖŠ£¬·“Ó¦×īæģµÄŹĒ£Ø £©
2AB3£¬ĻĀĮŠø÷ĻīĖł±ķŹ¾µÄ·“Ó¦ĖŁĀŹÖŠ£¬·“Ó¦×īæģµÄŹĒ£Ø £©| A£®VA2="0.4mol" / L”¤min | B£®VB2="0.8" mol / L”¤min |
| C£®VAB3="0.6" mol / L”¤min | D£®VA2="0.01mol" / L”¤S |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®ĪļÖŹČ¼ÉÕ²»Ņ»¶ØŹĒ·ÅČČ·“Ó¦ |
| B£®·ÅČČ·“Ó¦²»ŠčŅŖ“ÓĶā½ēĪüŹÕČĪŗĪÄÜĮæ¾ĶÄÜ·¢Éś |
| C£®ŌŚŅ»øöČ·¶ØµÄ»Æѧ·“Ó¦ÖŠ£¬·“Ó¦Īļ×ÜÄÜĮæ×ÜŹĒøßÓŚÉś³ÉĪļ×ÜÄÜĮæ |
| D£®·ÅŌŚ±łĻäÖŠµÄŹ³Ę·±£ÖŹĘŚ½Ļ³¤£¬ÕāÓėĪĀ¶Č¶Ō·“Ó¦ĖŁĀŹµÄÓ°ĻģÓŠ¹Ų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®¼ÓČėKHSO4¹ĢĢå | B£®²»ÓĆĢśĘ¬£¬øÄÓĆĢś·Ū |
| C£®µĪ¼ÓÉŁĮæĮņĖįĶČÜŅŗ”””” | D£®¼ÓČėKNO3¹ĢĢå |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Õż”¢Äę·“Ó¦ĖŁĀŹĶ¬Ź±Ōö“ó£¬Ę½ŗāŹ±ĆÜ¶Č¼õŠ” |
| B£®Õż·“Ó¦ĖŁĀŹŌö¼Ó±¶Źż“óÓŚÄę·“Ó¦ĖŁĀŹŌö¼Ó±¶Źż£¬NH3µÄĢå»ż°Ł·Öŗ¬Įæ½µµĶ”£ |
| C£®Äę·“Ó¦ĖŁĀŹŌö¼Ó±¶Źż“óÓŚÕż·“Ó¦ĖŁĀŹŌö¼Ó±¶Źż£¬N2×Ŗ»ÆĀŹ½µµĶ”£ |
| D£®ÖŲŠĀĘ½ŗāŹ±£¬N2£¼ 0.3mol, NH3£¾0.7mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
 O2(g)+2SO2(g)£¬ŌŚŅ»¶ØĢõ¼žĻĀn(SO3)ŗĶn(O2)Ėꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ £Ø £©
O2(g)+2SO2(g)£¬ŌŚŅ»¶ØĢõ¼žĻĀn(SO3)ŗĶn(O2)Ėꏱ¼ä±ä»ÆµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ £Ø £©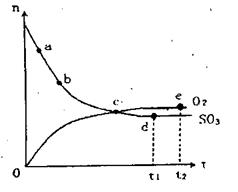
| A£®µćc“¦·“Ó¦“ļµ½Ę½ŗā |
B£®µćd£Ø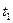 Ź±æĢ£©ŗĶe£Ø Ź±æĢ£©ŗĶe£Ø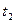 Ź±æĢ£©“¦n£ØSO2£©Ņ»Ńł Ź±æĢ£©“¦n£ØSO2£©Ņ»Ńł |
| C£®µćcµÄÄę·“Ó¦ĖŁĀŹ±Čµće“ó |
| D£®µćbµÄÕż·“Ó¦ĖŁĀŹ±Čµća“ó |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com