
分析 (1)先将物质的按照碱、盐、酸的顺序分类,再根据盐的水解和弱电解质的电离特点比较pH;
(2)CH3COONa的水解平衡常数Kh=$\frac{c(C{H}_{3}COOH)•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$=$\frac{c(CHCOOH)•c({H}^{+})•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}$=$\frac{Kw}{Ka}$;
(3)pH=3的醋酸和pH=11的氢氧化钠溶液中,醋酸浓度大于氢氧化钠,二者等体积混合,醋酸过量,溶液中存在物料守恒和电荷守恒;
(4)醋酸钠是强碱弱酸盐,其溶液呈碱性,要使醋酸和氢氧化钠混合溶液呈中性,则醋酸应该稍微过量,溶液中存在物料守恒.
解答 解:(1)盐酸和醋酸为酸,氢氧化钡为碱,碳酸钠、氯化钾和氯化铵为盐,碳酸钠为强碱弱酸盐,其溶液呈碱性,氯化钾为强酸强碱盐,为中性,氯化铵为强酸弱碱盐,其溶液为酸性,相同浓度的盐酸和醋酸,醋酸中氢离子浓度小于盐酸,所以pH盐酸小于醋酸,则这几种溶液的pH由小到大的顺序是①②⑥⑤④③,
故答案为:①②⑥⑤④③;
(2)CH3COONa的水解平衡常数Kh=$\frac{c(C{H}_{3}COOH)•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})}$=$\frac{c(CHCOOH)•c({H}^{+})•c(O{H}^{-})}{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}$=$\frac{Kw}{Ka}$=$\frac{1{0}^{-14}}{1.7×1{0}^{-5}}$=5.9×10-10,故答案为:5.9×10-10;
(3)pH=3的醋酸和pH=11的氢氧化钠溶液中,醋酸浓度大于氢氧化钠,二者等体积混合,醋酸过量,导致混合溶液呈酸性,溶液中存在物料守恒和电荷守恒,根据电荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),
故答案为:酸性;c(Na+)+c(H+)=c(CH3COO-)+c(OH-);
(4)醋酸钠是强碱弱酸盐,其溶液呈碱性,要使醋酸和氢氧化钠混合溶液呈中性,则醋酸应该稍微过量,所以m>n,二者混合时溶液体积增大一倍,溶液中存在物料守恒,根据物料守恒得c(CH3COO-)+c(CH3COOH)=0.5mmol/L,
故答案为:0.5mmol/L;>.
点评 本题考查了弱电解质的电离,涉及pH大小的判断、酸碱混合溶液定性判断等知识点,明确物质的性质及弱电解质电离特点是解本题关键,难点是(2),会根据微粒间的关系进行公式转换,难度较大.


 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案科目:高中化学 来源: 题型:解答题
| 序号 | 反应 | 化学平衡常数 |
| 1 | Au+6HNO3(浓)?Au(NO3)3+3NO2↑+3H2O | <<1 |
| 2 | Au3++4Cl-=AuCl4- | >>1 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18s | B. | 12s | C. | 30s | D. | 10s |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2Br-CH2Br 二溴乙烷 | B. | CH3OOCCH3甲酸乙酯 | ||
| C. | 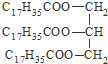 硬脂酸甘油脂 硬脂酸甘油脂 | D. | 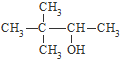 3,3-二甲基-2-丁醇 3,3-二甲基-2-丁醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们都属于混合物 | B. | 它们都是乙烯的同系物 | ||
| C. | 它们的分子都不含氢原子 | D. | 聚四氟乙烯分子中含有双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2通入水中:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 一小块钠投入水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 用氢氧化钠溶液吸收过量二氧化碳 OH-+CO2═HCO3- | |
| D. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 电解铝时阴极材料需要定期更换 | |
| B. | 炼钢中添加硅、锰、铝等作为脱氧剂,调整钢水的成分,制成多种性能优良的钢材 | |
| C. | 炼钢主要目的是在高温下用还原剂将过多的碳和其他杂质还原成气体或炉渣除去 | |
| D. | 工业上一般以铁矿石、焦炭、石灰石和空气等原料在高炉中冶炼生铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中Na+浓度增大,有H2放出 | |
| B. | 溶液中Na+数目减少,有H2放出 | |
| C. | 溶液中Na+与OH-浓度都增大,有H2放出 | |
| D. | 溶液中OH-数目增大,有H2放出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com