
��������� �׳ƴ��մ��������ɫ��ɫ�ᾧ���ܷ绯�ͳ��⣬��Ʒ�������ඨӰ����ȥ�ȼ��ͷ����Լ���������Ƥ���֯�ȹ�ҵ��
�׳ƴ��մ��������ɫ��ɫ�ᾧ���ܷ绯�ͳ��⣬��Ʒ�������ඨӰ����ȥ�ȼ��ͷ����Լ���������Ƥ���֯�ȹ�ҵ��
(1)��ҵ����ȡ��������� ����
���� �������ˮ��Һ�м��ȷ�Ӧ���õ������ڻ��ǰ��һ�����������Ҵ�������ԭ����ʲô��
�������ˮ��Һ�м��ȷ�Ӧ���õ������ڻ��ǰ��һ�����������Ҵ�������ԭ����ʲô��
(2)��֪�� ͨ������������ʿ���˵����Ӧ���ʵĿ��������ж����м�������£����ȿ�������������
ͨ������������ʿ���˵����Ӧ���ʵĿ��������ж����м�������£����ȿ�������������
[����]

(3)����������Ӧ������¶�ÿ����10����Ӧ��������Ϊԭ����3������ô20��ʱ����������ʼ������ʱ����54s�������¶���ߵ�50�棬����������ʼ������ʱ����______s��
|
(1) ������ˮ��������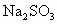 ��Һ�Ӵ�����Ӧ�������Ҵ�ʪ������Ҵ�������ˮ�������������ˮ�ĽӴ�������Ӷ�����ӷ�Ӧ���ʣ������� ��Һ�Ӵ�����Ӧ�������Ҵ�ʪ������Ҵ�������ˮ�������������ˮ�ĽӴ�������Ӷ�����ӷ�Ӧ���ʣ�������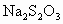 ���ղ����� ���ղ�����
(2)C ��(3)2���� (1)�����Ҵ�ʪ������Ҵ�������ˮ�������������ˮ�ĽӴ�������Ӷ�����˷�Ӧ�ٶȣ����� (2)��Ӧ�������Ŀ϶����¶���ߡ���Ӧ��Ũ������һ�飮��������C�飮���� (3)�����ҪŪ��������ϵ����ʱ�������ʵĹ�ϵ���ٶ����¶ȵĹ�ϵ����20������50�棬������30�棬�������ӵ�ԭ����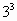 �����ʺ�ʱΪ2s�� �����ʺ�ʱΪ2s�� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� ��� |
T/K | c��Na2S2O3��/mol?L-1 | c��H2SO4�� /mol?L-1 |
ʵ��Ŀ�� |
| �� | 298 | 0.1 | 0.1 | ʵ��ٺ͢�̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죻ʵ��١��ۺ͢�̽����Ӧ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�죮 |
| �� | 308 | |||
| �� | 0.2 | |||
| �� | 0.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | T/K | c��Na2S2O3��/mol?L-1 | c��H2SO4��/mol?L-1 | ʵ��Ŀ�� |
| �� | 298 | 0.1 | 0.1 | ʵ��ٺ͢�̽���¶ȶԸ÷�Ӧ���ʵ�Ӱ�죻ʵ��١��ۺ͢�̽����Ӧ��Ũ�ȶԸ÷�Ӧ���ʵ�Ӱ�� |
| �� | 308 | |||
| �� | 0.2 | |||
| �� | 0.1 |
| O | 2- 4 |
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡ�����������Թ��У�������ˮ�ܽ� | |
| ����2�� | |
| ����3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡ�����������Թ�A�У�������ˮ�ܽ� | / |
| ����2�����Թ�A���� | |
| ����3��ȡ����2�������ϲ���Һ���Թ�B�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������������ ���ͣ�058
���������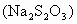 �׳ƴ��մ��������ɫ��ɫ�ᾧ���ܷ绯�ͳ��⣬��Ʒ�������ඨӰ����ȥ�ȼ��ͷ����Լ���������Ƥ���֯�ȹ�ҵ��
�׳ƴ��մ��������ɫ��ɫ�ᾧ���ܷ绯�ͳ��⣬��Ʒ�������ඨӰ����ȥ�ȼ��ͷ����Լ���������Ƥ���֯�ȹ�ҵ��
(1)��ҵ����ȡ���������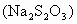 ����
����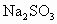 �������ˮ��Һ�м��ȷ�Ӧ���õ������ڻ��ǰ��һ�����������Ҵ�������ԭ����ʲô��
�������ˮ��Һ�м��ȷ�Ӧ���õ������ڻ��ǰ��һ�����������Ҵ�������ԭ����ʲô��
(2)��֪��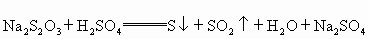 ͨ������������ʿ���˵����Ӧ���ʵĿ��������ж����м�������£����ȿ�������������
ͨ������������ʿ���˵����Ӧ���ʵĿ��������ж����м�������£����ȿ�������������
[����]
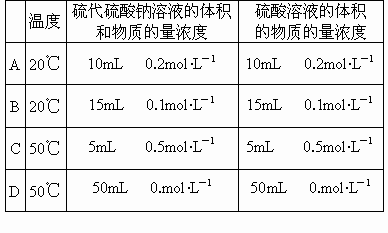
(3)����������Ӧ������¶�ÿ����10����Ӧ��������Ϊԭ����3������ô20��ʱ����������ʼ������ʱ����54s�������¶���ߵ�50�棬����������ʼ������ʱ����______s��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com