

| A. | 元素X的单质是一种常见的半导体材料 | |
| B. | M和Y的最高价氧化物对应的水化物之间能互相反应 | |
| C. | Y的最高价氧化物对应水化物的酸性比X 的弱 | |
| D. | Z的气态氢化物比Y的气态氢化物稳定 |
分析 由四种短周期元素在周期表中的位置,可知M为第三周期元素,且只有M为金属元素,则M为Al,结合位置可知X为Si,Y为N,Z为O,
A.Si位于金属与非金属元素的交界处;
B.M和Y的最高价氧化物对应的水化物分别为氢氧化铝、硝酸;
C.非金属性越强,对应最高价氧化物的水化物的酸性越强;
D.非金属性越强,对应氢化物越稳定.
解答 解:由四种短周期元素在周期表中的位置,可知M为第三周期元素,且只有M为金属元素,则M为Al,结合位置可知X为Si,Y为N,Z为O,
A.Si位于金属与非金属元素的交界处,则元素X的单质是一种常见的半导体材料,故A正确;
B.M和Y的最高价氧化物对应的水化物分别为氢氧化铝、硝酸,二者可发生复分解反应生成盐和水,故B正确;
C.非金属性N>Si,Y的最高价氧化物对应水化物的酸性比X 的强,故C错误;
D.非金属性O>N,Z的气态氢化物比Y的气态氢化物稳定,故D正确;
故选C.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.


科目:高中化学 来源: 题型:实验题
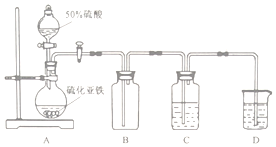
| 硫质量分数/% | 总铁质量分数/% | 亚铁质量分数/% | 硫化亚铁质量分数/% |
| 22.00 | 44.60 | 38.50 | x |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电池的电解液可为LiCl水溶液 | |
| B. | 放电时负极反应式为:Li-e-+Cl-=LiCl | |
| C. | 放电时正极反应式为:2SOCl2+4e-=4Cl-+S+SO2 | |
| D. | 放电时电子从负极经外电路流向正极,再从正极经电解质流向负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 预期结果 |
| A | 将湿润的NH3通过盛有无水CaCl2的干燥管 | 可得到干燥的NH3 |
| B | 将乙烯、乙醇蒸气分别通入酸性KMnO4溶液中 | 两者均能使KMnO4溶液褪色 |
| C | Na2O2与湿润的红色石蕊试纸接触 | 试纸只变蓝不褪色 |
| D | 将CO2通入CaCl2溶液中 | 可得到白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:1 | C. | 2:3 | D. | 4:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准情况下,22.4L CH4与18gH2O含有的分子数均为NA | |
| B. | 0.1mol•L-1的FeCl3溶液中含有Fe3+的数目小于0.1NA | |
| C. | 0.1molNa2O2中含有的阴离子的数目为0.2NA | |
| D. | 0.1mol铁粉与足量水蒸气在高温下反应,生成的H2分子数为0.15NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若8>m>3,则X必定为P区元素 | |
| B. | 若Y的气态氢化物化学式为YHn,且b<4,则该氢化物一定为极性分子 | |
| C. | 若a=b=3,8>m>n>b,则元素非金属性:X>Y | |
| D. | 若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y<X |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com