
����Ŀ��������Ʒ�������п�����������������Ʒ�ı�������һ�����ܵ�Fe3O4��ijѧϰС��Ϊ���о�������Ƭ���ֱ����������ʵ�������
�ٰ�һ����������Ƭ�ӹ��ɾ��ȷ�ĩ��
��ȡm g�÷�ĩ������28.00 mL 1 mol/L�������У�ǡ����ȫ��Ӧ�����ɱ�״���µ�����134.4 mL������Һ�е���KSCN��Һ������������
����ȡ���ݲ�ͬ�����ķ�ĩ���ּӼӵ���ͬ���(V)�����ʵ���Ũ�Ⱦ�Ϊl0.00 mol/L������������Һ�У���ַ�Ӧ����ȫ���ܽ⣬�йص�ʵ���������±���ʾ(����NO�������Ψһ��ԭ����)��
ʵ����� | �� | �� | �� |
�����ĩ����/g | 13.68 | 27.36 | 34.20 |
����������������״����/L | 2.912 | 5.824 | 6.720 |
������и��⣺
��1��ʵ���������Һ�е�������_______(д��ѧʽ)����Ʒ��n(Fe)��n(Fe3O4)=________��m��____________��
��2������ʵ�����ÿ��������Һ�����(V)��mL��_________��
��3������ʵ���������Һ�м�������ͭ�ۣ�Ҫʹ��Һ��Cu2ʮ��Fe2+��Fe3+ͬʱ���ڣ������ͭ�۵����ʵ����ķ�Χ___________��
���𰸡�FeCl2 4��1 0.912 g 180 mL 0.105mol��n(Cu)��0.315mol
��������
��1����������Һ�е���KSCN��Һ�������������֪��Ӧ�����ɵ�����ΪFeCl2�����ڷ����������Ϊ28.00 mL�� 1 mol/L=0.028mol���ʲ���FeCl2�����ʵ���Ϊ0.028/2=0.014mol�����е������ֱ������ᡢFe3O4���߷�����Ӧ���������ɱ�״���µ�����134.4 mL(0.006mol)�����ݵ���غ��֪��������������ᷢ����������ĵ�����Ϊ0.006mol����Fe3O4��Fe��HCl��ͬ��Ӧ���ڸ÷�Ӧ����Ԫ������Ϊ��0.014mol-0.006mol=0.008mol���Ҹ÷�Ӧ����ʽΪFe3O4+8HCl+Fe=4FeCl2+4H2O��ͨ���÷�Ӧ����ʽ��֪Fe3O4Ϊ0.002mol�������÷�Ӧ�ĵ�����Ϊ0.002mol�����ܵ�Fe���ʵ���Ϊ0.008mol��Fe3O4Ϊ0.002mol���ʱ���Ϊ4��1������Ϊ0.002mol��232g/mol +0.008mol��56g/mol =0.912g��
��2����������ʵ�飬ͨ��Ͷ���ĩ�����������������������ϵ��֪����Ϊ�����������Ϊ��ĩ��������ͨ��ʵ��������������������ڼ���NO�������Ψһ��ԭ����Ҳ�������������ʵ���Ϊ6.720L/22.4L��mol-1=0.3mol����NԪ�صõ�������Ϊ0.3mol��3=0.9mol�����ڢ��л��������Ϊ34.2g����n(Fe)��n(Fe3O4)=4:1����FeΪ0.3mol��Fe3O4Ϊ0.075mol�����ڵ�Ԫ�صõ���������Ϊ0.9mol������Һ��ΪFe(NO3)2��Fe(NO3)3�������ʣ������֪Fe(NO3)2Ϊ0.075mol��Fe(NO3)3Ϊ0.45mol������Һ�����������Ϊ0.075mol��2+0.45mol��3=1.5mol����÷�Ӧ��NԪ�������ʵ���Ϊ1.5mol+0.3mol=1.8mol������������Ϊ180mL��
��3��27.36g ��ĩ������n(Fe)��n(Fe3O4)=4:1��֪����Ԫ��0.42mol�������������������Ϊ����������II��Ӧ��������1.52 mol(���Ṳ1.8mol)����II��Һ����Fe3+0.42 mol����������0.28mol��

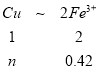
nmin=0.105mol n=0.21mol nmax =0.21mol+0.105mol=0.315mol���ʴ�Ϊ��0.105mol��n(Cu)��0.315mol��


 ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ����ͭ���õĺ�ɫ���������ͭ��������ͭ�Ļ�����֪Cu2O��������Һ�пɷ�������������ԭ��Ӧ������Cu2+�͵���ͭ��
��1������8������ͭ��������ԭ�õ���ɫ����6.8�ˣ����к�����ͭ��������ͭ�����ʵ���֮����_________��
��2������6.8�������������������ϡ�����ַ�Ӧ����ˣ��ɵõ�����__________�ˣ�
��3������6.8�������������һ������Ũ�����ַ�Ӧ��
�����ɱ�״����1.568�������壨������NO2���ܽ⣬Ҳ������NO2��N2O4��ת�������������ijɷ���___________�������ʵ���֮����_____________��
�ڰѵõ�����ҺС������Ũ�����������ľ�����ˣ��þ���23.68�ˣ���������ԭ��Һ�е�Cu2+��20%������ĸҺ�У������þ���Ļ�ѧʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���A ��ũҩ�����е�һ���м��壬�ṹ��ʽ����ͼ��ʾ��������������ȷ����
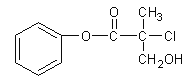
A��1mol A�������4mol H2�����ӳɷ�Ӧ
B���л���A������һ����������HBr������Ӧ
C���л���A��Ũ�����ϼ��ȣ����Է�����ȥ��Ӧ
D��1mol A��������NaOH��Һ��Ӧ������������2mol NaOH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͨ����н�������ʵ�飺
���� |
|
| |
���� | Fe�������������ɫ���ݣ�Һ���Ϸ���Ϊ����ɫ | Fe���������������ɫ���ݺ�Ѹ��ֹͣ | Fe��Cu�Ӵ�����������������ɫ���� |
����˵������ȷ����
A. I����������ɫ�����ɫ�Ļ�ѧ����ʽ��2NO+O2��2NO2
B. II�е�����˵��Fe�����γ����ܵ������㣬��ֹFe��һ����Ӧ
C. �Ա�I��II������˵��ϡHNO3��������ǿ��ŨHNO3
D. ��Ԣ���������Fe��Cu֮�����ӵ����ƣ����ж�Fe�Ƿ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ƣ�Na2S2O5���dz��õ�ʳƷ��������֮һ��ij�о�С���������ʵ�飺
ʵ��һ ���������Ƶ���ȡ
������ͼװ��(ʵ��ǰ�ѳ���װ���ڵĿ���)��ȡNa2S2O5��װ�â�����Na2S2O5���������������ķ�ӦΪ��Na2SO3��SO2��Na2S2O5

��1��װ��I�в�������Ļ�ѧ����ʽΪ__________________��
��2��Ҫ��װ�â��л���������ľ��壬�ɲ�ȡ�ķ��뷽����_________��
��3��װ�â����ڴ���β������ѡ�õ������װ��(�г���������ȥ)Ϊ________(�����)��

ʵ��� ���������Ƶ�����
Na2S2O5����ˮ������NaHSO3��
��4��֤��NaHSO3��Һ��HSO3���ĵ���̶ȴ���ˮ��̶ȣ��ɲ��õ�ʵ�鷽����________(�����)��
a���ⶨ��Һ��pH b������Ba(OH)2��Һ c����������
d������Ʒ����Һ e������ɫʯ����ֽ���
��5������Na2S2O5�����ڿ������ѱ�������ʵ�鷽����____________��
ʵ���� ���Ѿ��п��������������IJⶨ
��6�����ѾƳ���Na2S2O5�������������ⶨij���Ѿ��п��������IJ�����(������SO2����)�ķ������£�

(��֪���ζ�ʱ��Ӧ�Ļ�ѧ����ʽΪSO2��I2��2H2O��H2SO4��2HI)
�ٰ���������ʵ�飬���ı�I2��Һ25.00 mL���ô�ʵ������Ʒ�п��������IJ�����(������SO2����)Ϊ________________g��L��1��
��������ʵ������У����в���HI���������������ý��____(�ƫ�ߡ���ƫ�͡����䡱)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������廯����C�ķ���ʽΪC9H9OCl��C��������һ�����ұ�����ֻ��һ��������һ��������C�ܷ���������Ӧ��
C����������֮���ת������ͼ��ʾ��
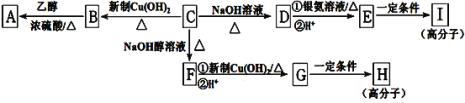
(1)C�Ľṹ��ʽ��__________________��
(2)E�к��������ŵ�������___________�� C��F�ķ�Ӧ������___________��
(3)д�����л�ѧ����ʽ��G��һ�������ºϳ�H�ķ�Ӧ________________________��
(4)D��һ��ͬϵ��W(����ʽΪC8H8O2)�ж���ͬ���칹�壬�������������W��ͬ���칹����________�֣�д�����к˴Ź���������4����Ľṹ��ʽ____________��
�����ڷ����廯�������FeCl3��Һ������ɫ��������NaOH��Һ������Ӧ��������ˮ�ⷴӦ
(5)����ƺ���������![]() �ϳ�
�ϳ�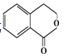 __________(���Լ���ѡ���÷�Ӧ����ͼ��ʾ����ע����Ӧ����)��
__________(���Լ���ѡ���÷�Ӧ����ͼ��ʾ����ע����Ӧ����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�к��е����ӿ�����K+��Ba2+��Al3+��Mg2+��A1O2-��CO32-��SiO32-��Cl-�еļ��֣��ֽ�������ʵ�飺
��ȡ������Һ������������Һ�������������ɣ�
����ȡ����ԭ��Һ����μ���5 mL 0.2 mol L-1�����ᣬ�����������ǿ�ʼ���������������࣬���������������������壬��������������ʧ��
���������ڳ�����ʧ�����Һ�У��ټ�����������������Һ�ɵõ�����0.435 g��
����˵������ȷ����
A.����Һ��һ��������Ba2+��Mg2+��Al3+��SiO32-��Cl-
B.����Һ��һ������K+��AlO2-��CO32-��Cl-
C.����Һ���Ƿ���K+������ɫ��Ӧ������ɫ�ܲ���Ƭ��
D.���ܺ���Cl-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о����������������ڴ����к������ӵ������ʱ���漰���·�Ӧ��
2NO2��g��+NaCl��s��NaNO3��s��+ClNO��g��+Q1 K1 ����
2NO��g��+Cl2��g��2ClNO��g��+Q2 K2 ����
��1��4NO2��g��+2NaCl��s��2NaNO3��s��+2NO��g��+Cl2��g����ƽ�ⳣ��K=____���ú�K1��K2�Ĵ���ʽ��ʾ����
��2��Ϊ�о���ͬ�����Է�Ӧ����Ӱ�죬�ں��������£���2L�����ܱ������м���0.2mol NO��0.1mol Cl2��10minʱ��Ӧ���ﵽƽ�⣮�����10min��v��ClNO��=7.5��10��3molL��1min��1����ƽ���n��Cl2��=_____mol��NO��ת������1=____�������������ֲ��䣬��Ӧ�����ں�ѹ�����½��У�ƽ��ʱNO��ת������2____��1��������������������=������ƽ�ⳣ��K2____����������������С������������������ҪʹK2��С���ɲ��õĴ�ʩ��____��
��3��ʵ���ҿ���NaOH��Һ����NO2����ӦΪ2NO2+2NaOH��NaNO3+NaNO2+H2O����0.2mol NaOH��ˮ��Һ��0.2mol NO2ǡ����ȫ��Ӧ��1L��ҺA����ҺBΪ0.1molL��1��CH3COONa��Һ��������Һ��c��NO3������c��NO2������c��CH3COO�����ɴ�С��˳��Ϊ____������֪HNO2�ĵ��볣��Ka=7.1��10��4molL��1��CH3COOH�ĵ��볣��Ka=1.7��10��5molL��1����ʹ��ҺA����ҺB��pH��ȵķ�����____��
a ����ҺA�м�����ˮ b ����ҺA�м�����NaOH
c ����ҺB�м�����ˮ d ��ҺB�м�����NaOH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ж����й����ʱ��˵����ȷ���ǣ� ��
A.��ͬ�����·�Ӧ2SO2(g)+O2(g)![]() 2SO3(g)��4SO2(g)+2O2(g)
2SO3(g)��4SO2(g)+2O2(g)![]() 4SO3(g)����H���
4SO3(g)����H���
B.����ı�ȼ����Ϊ-890.3kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ���Ա�ʾΪ��CH4(g)+2O2(g)�TCO2(g)+2H2O(g) ��H=-890.3kJ��mol-1
C.��һ���¶Ⱥ�ѹǿ�£���0.5molN2��1.5molH2�����ܱ������г�ַ�Ӧ����NH3(g)���ų�����19.3kJ�������Ȼ�ѧ����ʽΪN2(g)+3H2(g)![]() 2NH3(g) ��H=-38.6kJ��mol-1
2NH3(g) ��H=-38.6kJ��mol-1
D.һ������2SO2(g)+O2(g)![]() 2SO3(g) ��H1��2SO2(g)+O2(g)
2SO3(g) ��H1��2SO2(g)+O2(g)![]() 2SO3(l) ��H2������H1����H2
2SO3(l) ��H2������H1����H2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com