
(1)配平氧化还原反应方程式:
____C2O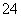 +____MnO
+____MnO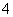 +____H+===____CO2↑+____Mn2++____H2O
+____H+===____CO2↑+____Mn2++____H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25.00 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1 NaOH溶液至20.00 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为________mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
A.KMnO4溶液在滴定过程中作________(填“氧化剂”或“还原剂”),该滴定过程________(填“需要”或“不需要”)另加指示剂。滴至16.00 mL时反应完全,此时溶液颜色由________变为__________。
B.若在接近终点时,用少量蒸馏水将锥形瓶冲洗一下,再继续滴定至终点,则所测结果__________(填“偏大”、“偏小”或“无影响”)。
C.若在达到滴定终点时俯视读数,则所得结果________(填“偏大”、“偏小”或“无影响”)。③原试样中H2C2O4·2H2O的质量分数为________,KHC2O4的质量分数为__________。
答案 (1)5 2 16 10 2 8
(2)①0.005 ②A.氧化剂 不需要 无色 浅紫红色
B.无影响 C.偏小 ③21% 64%
解析 (1)C:+3―→+4,改变量(4-3)×2=2,Mn:+7―→+2,改变量(7-2)×1=5,根据化合价升降总数相等,所以在C2O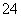 前配5,MnO
前配5,MnO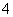 前配2,根据C和Mn原子守恒,分别在CO2和Mn2+前配10和2,再由电荷守恒在H+前配16,最后根据离子方程式两边的H原子个数相等在H2O前面配8,经检验离子方程式的氧原子个数相等。
前配2,根据C和Mn原子守恒,分别在CO2和Mn2+前配10和2,再由电荷守恒在H+前配16,最后根据离子方程式两边的H原子个数相等在H2O前面配8,经检验离子方程式的氧原子个数相等。
(2)①由H++OH-===H2O知,n(H+)=n(OH-)=0.25 mol·L-1×0.02 L=0.005 mol。②原溶液无色,而KMnO4为紫红色,所以当溶液中的H2C2O4和KHC2O4反应完全时,溶液呈浅紫红色。由电子守恒得n(还)×2=0.10 mol·L-1×0.016 L×5,n(还)=0.004 mol。③设6.0 g 试样中H2C2O4·2H2O、KHC2O4的物质的量分别为n(H2C2O4·2H2O)、n(KHC2O4),由①得:2n(H2C2O4·2H2O)+n(KHC2O4)=0.05 mol,由②得:n(H2C2O4·2H2O)+n(KHC2O4)=0.04 mol,解上述两个方程式得:n(H2C2O4·2H2O)=0.01 mol,n(KHC2O4)=0.03 mol,H2C2O4·2H2O的质量分数为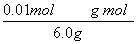 ×100%=21%,KHC2O4的质量分数为
×100%=21%,KHC2O4的质量分数为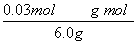 ×100%=64%。
×100%=64%。


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3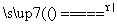 2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28 g N2时,转移的电子数目为3.75NA
查看答案和解析>>
科目:高中化学 来源: 题型:
有关物质性质及用途的说法,正确的是
A.甲烷与氯气在光照的条件下可以制取纯净的一氯甲烷
B.将溴水加入苯中,溴水的颜色变浅,这是由于发生了加成反应
C.牡丹籽油是一种优良的植物油脂,它可使酸性高锰酸钾溶液褪色
D.等质量的乙烯和聚乙烯充分燃烧所需氧气的量不相等
查看答案和解析>>
科目:高中化学 来源: 题型:

去。经检测发现滤液中仍含有一定量的SO42—,其原因是
。【已知:Ksp(BaSO4)= 1.1 ×10—10 Ksp(BaCO3)= 5.1 ×10—9】
②该法工艺原理如右。其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。
工艺中可以利用的单质有 (填化学式),发生器中生成ClO2的化学方程式为 。
(2)纤维素还原法制ClO2是一种新方法,其原理是:纤维素水解得到的最终产物D与NaClO3反应生成ClO2。完成反应的化学方程式:
 (D) +24NaClO3+12H2SO4=
(D) +24NaClO3+12H2SO4= ClO2↑+
ClO2↑+ CO2↑+18H2O+
CO2↑+18H2O+
(3)ClO2和Cl2均能将电镀废水中的CN—氧化为无毒的物质,自身被还原为Cl—。 处理含CN—相同时的电镀废水,所需Cl2的物质的量是ClO2的 倍
查看答案和解析>>
科目:高中化学 来源: 题型:
由于用氯气对饮用水消毒,会使水中的有机物发生氯代,生成有机含氯化合物,于人体有害,世界环保联盟即将全面禁止这种消毒方法,建议采用广谱性具有强氧化性的高效消毒剂二氧化氯(ClO2).C102极易爆炸,生产和使用时尽量用稀有气体稀释,避免光照、震动或加热.
(1)在C102分子中,氯元素的化合价
(2)欧洲一些国家用NaClO3氧化浓盐酸来制 C102,同时有Cl2生成,且Cl2的体积为ClO2体积的一半,表示这一反应的化学方程式是 。
(3)我国广泛采用将经干燥空气稀释的氯气,通入有固体亚氯酸钠(NaClO2)的柱内制得C102,这一反应的学方程式是 ,和欧洲的方法相比,我国这一方法的主要优点是 。
(4)在酸性溶液中,用草酸钠(Na2C204)还原NaClO3也可制得C102,表示这一反应的离子方程式是 ,此法的优点是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列溶液中,各组离子一定能够大量共存的是( )
A.含Fe3+的溶液中:K+、H+、Cl-、MnO4-
B.使石蕊试液变红的溶液:Na+、I-、SO42-、Fe3+
C.含有大量ClO-的溶液:H+、Mg2+、I-、SO42-
D.c(H+)=10-12 mol·L-1的溶液:K+、Ba2+、Cl-、Br-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应:KCl03+6HCl=KCl+3C12↑+3H20,若用K35C103和H37Cl作用,下列说法正确的是( ) A.KCl中只含35C1 B. KCl中只含37Cl
C. KCl中既含35C1又含37Cl D.被氧化和被还原的氯原子个数比为6 ∶ 1
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20.0%,与反应前的体积相比,反应后体积缩小的百分率是( )
A.16.7% B.20.0% C.80.0% D.83.3%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com