
分析 (1)原子利用率目标产物的原子质量占反应物原子质量的百分比,当为100%时最高,即化学反应反应物全部转化为生成物;
(2)①Ni能与氧气反应也会导致其中毒,据此解答即可;
②利用盖斯定律进行计算即可,
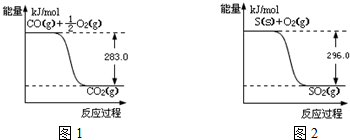
由图I可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
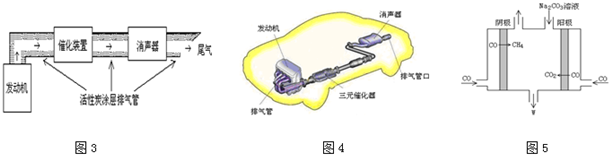
由图II可知,S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
(i)-(ii)得;
(3)①依据此反应特点判断即可,C(s)+2NO(g)?N2(g)+CO2 (g)△H=-a kJ•mol-1,此反应为放热反应,且为气体体积不变的反应,据此分析判断;
②根据反应物、生成物和反应条件及质量守恒定律的两个原则,写出正确的化学方程式;
(4)根据燃料电池为燃料作负极失电子发生氧化反应,结合电解质溶液书写负极电极反应式;
(5)由此电解原理可知,阳极失去电子生成二氧化碳气体,加入碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,阴极CO得到电子生成甲烷气体,据此解答即可.
解答 解:(1)观察四个反应方程式可见,只有反应d中参加反应的物质全部转化为一种物质,故原子利用率最高,
故答案为:d;
(2)①Ni能与氧气反应也会导致其中毒,故答案为:避免O2与Ni反应再使其失去催化作用;
②由图I可知,O2(g)+2CO(g)=2CO2(g)△H=(-2×283)kJ•mol-1=-566kJ•mol-1,(i)
由图II可知,S(s)+O2(g)=SO2(g)△H=-296kJ•mol-1,(ii)
(i)-(ii)得:SO2(g)+2CO(g)=S(s)+2CO2(g)△H=-563-(-298)=-270kJ•mol-1,
故答案为:-270kJ/mol;
(3)①C(s)+2NO(g)?N2(g)+CO2 (g)△H=-a kJ•mol-1,此反应为放热反应,且为气体体积不变的反应,
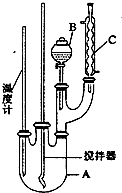
a.增加排气管长度,不能改变NO的转化率,故a错误;
b.增大尾气排放口,相当于移出部分氮气和二氧化碳气体,利于平衡右移,故b正确;
c.添加合适的催化剂,只改变化学反应速率,不会增加NO的转化率,故c错误;
d.升高排气管温度,温度升高,平衡左移,不利于NO转化,故d错误;
故选b,
故答案为:b;
②反应物是一氧化碳和NOx,生成物无毒,故生成物之一是氮气和二氧化碳,根据反应前后元素种类不变,化学方程式为:2xCO+2NOx $\frac{\underline{\;催化剂\;}}{\;}$2xCO2+N2,
故答案为:2xCO+2NOx $\frac{\underline{\;催化剂\;}}{\;}$2xCO2+N2;
(4)燃料电池为燃料作负极失电子发生氧化反应,又电解质溶液为KOH,所以负极电极反应式为:CH3OCH3-12e-+16OH-=2CO32-+11H2O,
故答案为:CH3OCH3-12e-+16OH-=2CO32-+11H2O;
(5)由此电解原理可知,阳极失去电子生成二氧化碳气体,加入碳酸钠,碳酸钠与二氧化碳反应生成碳酸氢钠,阴极CO得到电子生成甲烷气体,据此离子反应方程式为:4CO+3CO32-+5H2O=6HCO3-+CH4↑,
故答案为:NaHCO3;4CO+3CO32-+5H2O=6HCO3-+CH4↑.
点评 本题主要考查的是绿色化学的概念、盖斯定律的应用、原电池反应原理与电极方程式的书写、氧化还原反应等,综合性较强,难度较大.


科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③⑤ | C. | ①④⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在空气中敞口久置的浓硫酸,溶液质量增大(难挥发性) | |
| B. | 在加热条件下铜与浓硫酸反应(强氧化性、酸性) | |
| C. | 蔗糖与浓硫酸反应中有海绵状的炭生成(吸水性) | |
| D. | 浓硫酸与少量胆矾晶体混合,晶体由蓝色变成白色(脱水性) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 实验室制备硝基苯的反应原理和实验装置如下:
实验室制备硝基苯的反应原理和实验装置如下: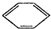 +HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$
+HO-NO2$→_{50-60℃}^{H_{2}SO_{4}}$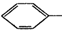 NO2+H2O△H<0
NO2+H2O△H<0| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二销基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡含有食品添加剂的食物对人体健康均有害 | |
| B. | 使用含钙离子浓度较大的地下水洗衣服,肥皂去污能力减弱 | |
| C. | 施肥时,农家肥草木灰(有效成分K2CO3)不能与氮肥NH4Cl混合使用 | |
| D. | 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
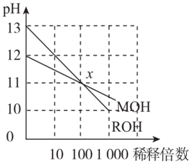
| A. | ROH是一种强碱,MOH是一种弱碱 | |
| B. | 等浓度的MOH与盐酸反应,所得溶液呈中性,则V(MOH)>V(盐酸) | |
| C. | 在x点,c(M+)=c(R+) | |
| D. | 稀释前,c(ROH)=10c(MOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
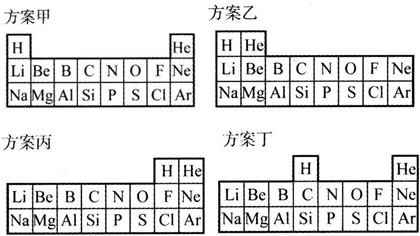
| “合理”的理由 | |
| 方案甲 | |
| 方案乙 | |
| 方案丙 | |
| 方案丁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属表面的氧化膜都很致密,能对金属起到保护作用 | |
| B. | 金属表面的氧化膜的形成都需要金属暴露在空气中很长时间才会形成 | |
| C. | 金属表面的氧化膜薄层的厚度会随着金属暴露在空气中的时间增长而加厚 | |
| D. | 某些金属表面氧化膜的形成对这些金属的广泛应用起到关键作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 漂白粉溶液中加入少许食醋可以增强其漂白效果 | |
| B. | 用二氧化硫漂白米粉是违法行为,因为二氧化硫有毒 | |
| C. | 铝制品在生活中非常普遍,这是因为铝不活泼 | |
| D. | 氢氧化铝可用于治疗胃酸过多,但不宜长期服用 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com